化合物X是一种由三种元素组成的重要化工原料,其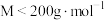 ,进行如图所示操作,已知B、D含有一种相同的元素且在常温下均为气态化合物,其中气体B可使品红溶液褪色(部分反应条件省略),C可由两种组成元素的单质直接反应得到。请回答:
,进行如图所示操作,已知B、D含有一种相同的元素且在常温下均为气态化合物,其中气体B可使品红溶液褪色(部分反应条件省略),C可由两种组成元素的单质直接反应得到。请回答:
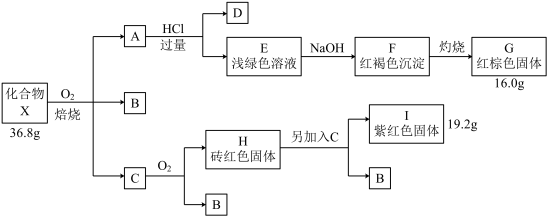
(1)组成X的元素有_______ ,化合物X的化学式是_______ 。
(2)溶液E中溶质的主要成分是_______ (用化学式表示)。
(3)写出砖红色固体H与C反应生成I和B的化学方程式:_______ 。
(4)请设计实验检验E溶液中的金属阳离子:_______ 。
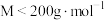 ,进行如图所示操作,已知B、D含有一种相同的元素且在常温下均为气态化合物,其中气体B可使品红溶液褪色(部分反应条件省略),C可由两种组成元素的单质直接反应得到。请回答:
,进行如图所示操作,已知B、D含有一种相同的元素且在常温下均为气态化合物,其中气体B可使品红溶液褪色(部分反应条件省略),C可由两种组成元素的单质直接反应得到。请回答:
(1)组成X的元素有
(2)溶液E中溶质的主要成分是
(3)写出砖红色固体H与C反应生成I和B的化学方程式:
(4)请设计实验检验E溶液中的金属阳离子:
22-23高一下·浙江·期中 查看更多[1]
(已下线)【2023】【高一下】【期中考】【学军紫金港】【高中化学】【洪翔峰收集】
更新时间:2023-05-12 12:35:53
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】物质A、B、C、D、E、F、G、H、I、J、K存在下图转化关系,其中气体D为单质,试回答问题。

(1)写出下列物质的化学式:
A是__________ ,D是__________ ,K是__________ 。
(2)写出反应“C→F”的离子方程式:__________________________ 。
(3)写出反应“F→G”的化学方程式:_____________________________ 。
(4)在溶液I中滴入NaOH溶液,可观察到先生成白色絮状沉淀,而后迅速变为灰绿色,最后变为红褐色沉淀,请写出白色絮状沉淀变为红褐色沉淀的化学方程式__________________ 。
(5)请写出实验室制备黄绿色气体E的化学方程式:_____________________ 。
(6)溶液I中通入气体E发生的离子方程式为:_________________________ 。

(1)写出下列物质的化学式:
A是
(2)写出反应“C→F”的离子方程式:
(3)写出反应“F→G”的化学方程式:
(4)在溶液I中滴入NaOH溶液,可观察到先生成白色絮状沉淀,而后迅速变为灰绿色,最后变为红褐色沉淀,请写出白色絮状沉淀变为红褐色沉淀的化学方程式
(5)请写出实验室制备黄绿色气体E的化学方程式:
(6)溶液I中通入气体E发生的离子方程式为:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】在一定条件下,下列各物质可发生如图所示的变化(反应中生成的水没有写出)
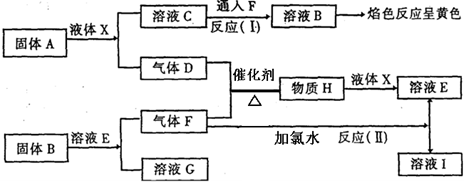
(1)B的化学式是_____________________
(2)A的电子式是_____________________
(3)已知气体F是一种漂白剂,写出D和F反应的化学方程式:____________________
(4)写出反应II的离子方程式:____________________

(1)B的化学式是
(2)A的电子式是
(3)已知气体F是一种漂白剂,写出D和F反应的化学方程式:
(4)写出反应II的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】有甲、乙、丙、丁、戊五种短周期元素,原子序数依次增大,其常见化合价依次为+1、-2、+1、+3、-1。它们形成的物质间的转化关系如下图所示。常温下用惰性电极电解(有阳离子交换膜)1L l mol/L的A溶液。
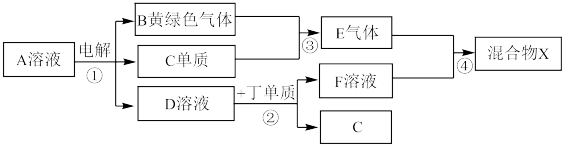
请按要求回答下列问题:
(1)己元素与丙元素同主族,比丙原子多2个电子层,则己的原子序数为______ ;推测相同条件下丙、己单质分别与水反应剧烈程度的依据是_________ 。
(2)甲、乙、戊按原子个数比1:1:1形成的化合物Y具有漂白性,其电子式为______ 。
(3)上图转化关系中不属于氧化还原反应的有(填编号)______ 。
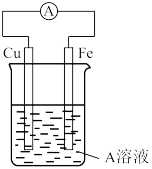
(4)接通如图电路片刻后,向烧杯中滴加一种试剂即可检验铁电极被腐蚀,此反应的离子方程式为___________ 。
(5)写出反应③的化学方程式_________ ;反应②的离子方程式为___________ 。
(6)若上图中各步反应均为恰好完全转化,则混合物X中含有的物质(除水外)有___________ 。

请按要求回答下列问题:
(1)己元素与丙元素同主族,比丙原子多2个电子层,则己的原子序数为
(2)甲、乙、戊按原子个数比1:1:1形成的化合物Y具有漂白性,其电子式为
(3)上图转化关系中不属于氧化还原反应的有(填编号)
(4)接通如图电路片刻后,向烧杯中滴加一种试剂即可检验铁电极被腐蚀,此反应的离子方程式为

(5)写出反应③的化学方程式
(6)若上图中各步反应均为恰好完全转化,则混合物X中含有的物质(除水外)有
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】某小组同学探究盐对Fe3+ +3SCN- Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。
实验I:探究KCl对Fe3+和SCN-平衡体系的影响
将已用稀盐酸酸化的0.005 mol·L-1 FeCl3溶液和0.01 mol·L-1 KSCN溶液等体积混合,静置至体系平衡,得红色溶液X,分别取3 mL溶液X放入比色皿中,分别滴加0.1 mL的试剂①~④,并测定各溶液的透光率随时间的变化,结果如图所示。
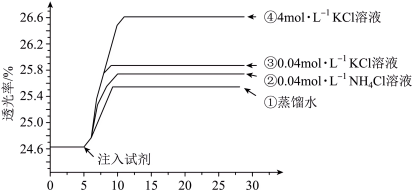
已知:i.Cl-与Fe3+能发生络合反应:Fe3+ +4C1- [FeCl4]-(黄色);
[FeCl4]-(黄色);
ii.Fe3+与NO 不能形成配位化合物;
不能形成配位化合物;
iii.溶液的透光率与溶液颜色深浅有关,颜色越深,透光率越低,忽略[FeCl4]-对透光率的影响。
(1)本实验配制溶液时用到的玻璃仪器除烧杯、量筒、玻璃棒、容量瓶外,还需要___________ ,用稀盐酸酸化FeCl3溶液的目的是___________ 。
(2)注入试剂①后溶液透光率升高,甲同学认为是溶液稀释导致颜色变浅,乙同学认为还可能是稀释的过程中,Fe3+ +3SCN- Fe(SCN)3平衡向
Fe(SCN)3平衡向___________ (填“正”或“逆”)反应方向移动。
(3)注入试剂④后的溶液透光率比注入试剂①后高,结合平衡移动原理分析其原因___________ 。
(4)注入试剂③后的溶液透光率比注入试剂②后高,可能是___________ 导致的(答出一种影响因素即可,不需详细说明理由)。
实验II:探究不同盐对Fe3+和SCN-平衡体系的影响
取2 mL溶液X,分别加入下列试剂进行实验,一段时间后测得各溶液的透光率如下表。
(5)丙同学发现A3>A2>A1,查阅资料认为可能的原因:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。推断盐效应较强的金属阳离子为___________ (填离子符号),试分析该离子盐效应对Fe3+和SCN-平衡体系有影响的原因___________ 。
(6)拓展应用:盐效应对多种平衡体系有影响。
分析c(Na2SO4)在0~0.20 mol·L-1范围内,PbSO4溶解度发生变化的原因:___________ 。
(7)FeCl3用途十分广泛,请写出一种其在生活中的用途___________ 。
 Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。实验I:探究KCl对Fe3+和SCN-平衡体系的影响
将已用稀盐酸酸化的0.005 mol·L-1 FeCl3溶液和0.01 mol·L-1 KSCN溶液等体积混合,静置至体系平衡,得红色溶液X,分别取3 mL溶液X放入比色皿中,分别滴加0.1 mL的试剂①~④,并测定各溶液的透光率随时间的变化,结果如图所示。

已知:i.Cl-与Fe3+能发生络合反应:Fe3+ +4C1-
 [FeCl4]-(黄色);
[FeCl4]-(黄色);ii.Fe3+与NO
 不能形成配位化合物;
不能形成配位化合物;iii.溶液的透光率与溶液颜色深浅有关,颜色越深,透光率越低,忽略[FeCl4]-对透光率的影响。
(1)本实验配制溶液时用到的玻璃仪器除烧杯、量筒、玻璃棒、容量瓶外,还需要
(2)注入试剂①后溶液透光率升高,甲同学认为是溶液稀释导致颜色变浅,乙同学认为还可能是稀释的过程中,Fe3+ +3SCN-
 Fe(SCN)3平衡向
Fe(SCN)3平衡向(3)注入试剂④后的溶液透光率比注入试剂①后高,结合平衡移动原理分析其原因
(4)注入试剂③后的溶液透光率比注入试剂②后高,可能是
实验II:探究不同盐对Fe3+和SCN-平衡体系的影响
取2 mL溶液X,分别加入下列试剂进行实验,一段时间后测得各溶液的透光率如下表。
| 序号 | 加入试剂 | 溶液透光率 |
| 1 | 1 mL蒸馏水 | A1 |
| 2 | 1 mL 3 mol·L-1 KNO3 | A2 |
| 3 | 1 mL 3 mol·L-1 NaNO3 | A3 |
(5)丙同学发现A3>A2>A1,查阅资料认为可能的原因:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。推断盐效应较强的金属阳离子为
(6)拓展应用:盐效应对多种平衡体系有影响。
| c(Na2SO4)/(mol·L-1) | 0 | 0.01 | 0.02 | 0.04 | 0.10 | 0.20 |
| PbSO4溶解度/mg | 4.5 | 0.48 | 0.42 | 0.39 | 0.48 | 0.69 |
(7)FeCl3用途十分广泛,请写出一种其在生活中的用途
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】某小组在验证H2O2氧化Fe2+时发现异常现象,并对其进行深入探究。
实验I:
(1)实验I中溶液变红是因为Fe3+与SCN-发生了反应,其离子方程式是__ 。
(2)探究实验I中红色褪去的原因:取反应后溶液,___ (填实验操作和现象),证明溶液中有Fe3+,而几乎无SCN-。
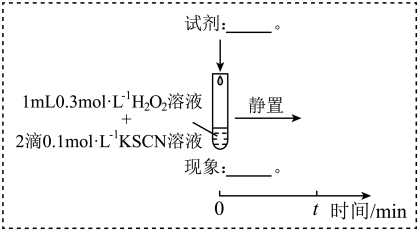
(3)研究发现,酸性溶液中H2O2能氧化SCN-,但反应很慢且无明显现象,而实验I中褪色相对较快,由此推测Fe3+能加快H2O2与SCN-的反应。通过实验II和III得到了证实。参照实验II的图例,在虚线框内补全实验III:__ 。
实验II:
i.Fe3++H2O2=Fe2++HO2·+H+
ii.Fe2++H2O2=Fe3++·OH+OH-
iii.OH(羟基自由基)具有强氧化性,能直接氧化SCN-
为探究Fe2+对H2O2与SCN-反应速率的影响,设计实验如图:
实验IV:___ 。
②结合资料和(1)~(4)的研究过程,从反应速率和化学平衡的角度解释实验I中溶液先变红后褪色的原因:____ 。
③实验I~IV中均有O2生成,小组同学推测可能是HO2·与溶液中其他微粒相互作用生成的,这些微粒有___ 。
实验I:
| 装置与操作 | 现象 |
| 溶液立即变红,继续滴加H2O2溶液,红色变浅并逐渐褪去 |
(2)探究实验I中红色褪去的原因:取反应后溶液,
(3)研究发现,酸性溶液中H2O2能氧化SCN-,但反应很慢且无明显现象,而实验I中褪色相对较快,由此推测Fe3+能加快H2O2与SCN-的反应。通过实验II和III得到了证实。参照实验II的图例,在虚线框内补全实验III:
实验II:
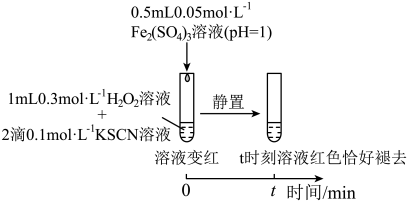
i.Fe3++H2O2=Fe2++HO2·+H+
ii.Fe2++H2O2=Fe3++·OH+OH-
iii.OH(羟基自由基)具有强氧化性,能直接氧化SCN-
为探究Fe2+对H2O2与SCN-反应速率的影响,设计实验如图:
实验IV:

②结合资料和(1)~(4)的研究过程,从反应速率和化学平衡的角度解释实验I中溶液先变红后褪色的原因:
③实验I~IV中均有O2生成,小组同学推测可能是HO2·与溶液中其他微粒相互作用生成的,这些微粒有
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】七水合硫酸镁(MgSO4·7H2O)用于饲料添加剂中微量元素镁的补充。一种以硼镁泥(主要成分为MgCO3,此外还含有MnO、Fe2O3、CaO、FeO、Al2O3、SiO2等杂质)为原料制备高纯七水合硫酸镁的工艺流程如图所示:

已知:相关金属离子形成氢氧化物沉淀的pH范围如下表所示。
回答下列问题:
(1)“酸溶”工序中生成气体的电子式为_______ 。
(2)“氧化”工序中加入NaClO有两个作用:
①将Mn2+氧化为MnO2,反应的离子方程式为_______ 。
②_______ 。
(3)请设计实验方案检验“过滤”后所得滤液中铁元素已被除尽:_______ 。
(4)已知CaSO4的溶解度随温度升高而降低,则操作a、操作b分别为_______ (填“蒸发浓缩、趁热过滤”或“冷却结晶、过滤”,下同)、_______ 。
(5)MgSO4·7H2O含量的测定:准确称取0.5g试样配成100mL溶液,用_______ (填“酸式”或“碱式”)滴定管量取20.00mL溶液于250mL锥形瓶中,加入10mL氨性缓冲溶液和3~4滴EBT指示剂,用0.02mol·L-1EDTA标准溶液滴定(EDTA与Mg2+按物质的量之比1:1反应),至溶液由紫红色变为蓝色,且半分钟内不变色。平行滴定3次,平均消耗EDTA标准溶液体积为19.00mL,则所得试样的纯度为_______ %。

已知:相关金属离子形成氢氧化物沉淀的pH范围如下表所示。
| 金属离子 | Fe3+ | Fe2+ | Ca2+ | Al3+ | Mg2+ |
| 开始沉淀的pH | 2.3 | 7.5 | 11.3 | 4.0 | 9.4 |
| 沉淀完全的pH | 4.1 | 9.7 | 12.3 | 5.2 | 12.4 |
回答下列问题:
(1)“酸溶”工序中生成气体的电子式为
(2)“氧化”工序中加入NaClO有两个作用:
①将Mn2+氧化为MnO2,反应的离子方程式为
②
(3)请设计实验方案检验“过滤”后所得滤液中铁元素已被除尽:
(4)已知CaSO4的溶解度随温度升高而降低,则操作a、操作b分别为
(5)MgSO4·7H2O含量的测定:准确称取0.5g试样配成100mL溶液,用
您最近一年使用:0次




