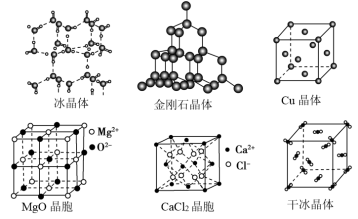
I.下图为几种晶体或晶胞的示意图,请回答下列问题:___________ 。
(2)冰、金刚石、 、干冰4种晶体的熔点由高到低的顺序为
、干冰4种晶体的熔点由高到低的顺序为___________ 。
(3) 晶胞中,每个
晶胞中,每个 晶胞中平均占有
晶胞中平均占有___________ 个 ,由与
,由与 最近的
最近的 围成的空间几何构型为
围成的空间几何构型为___________ 。
(4)铜晶体中一个 周围紧邻的
周围紧邻的 有
有___________ 个, 晶体中
晶体中 的配位数是
的配位数是___________ 。
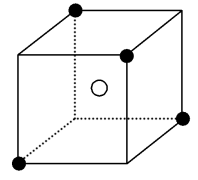
Ⅱ.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
(5)一个晶胞中有___________ 个 ,找出距离
,找出距离 最近的
最近的
___________ (用分数坐标表示)。 晶体中与单个
晶体中与单个 键合的
键合的 有
有___________ 个。
(2)冰、金刚石、
 、干冰4种晶体的熔点由高到低的顺序为
、干冰4种晶体的熔点由高到低的顺序为(3)
 晶胞中,每个
晶胞中,每个 晶胞中平均占有
晶胞中平均占有 ,由与
,由与 最近的
最近的 围成的空间几何构型为
围成的空间几何构型为(4)铜晶体中一个
 周围紧邻的
周围紧邻的 有
有 晶体中
晶体中 的配位数是
的配位数是Ⅱ.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
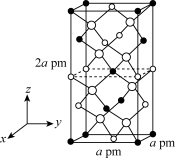
| 坐标原子 | x | y | z |
 | 0 | 0 | 0 |
 | 0 | 0 | 0.5 |
 | 0.25 | 0.25 | 0.125 |
 ,找出距离
,找出距离 最近的
最近的
 晶体中与单个
晶体中与单个 键合的
键合的 有
有
22-23高二下·广东广州·期中 查看更多[3]
更新时间:2023-05-15 21:11:57
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】人类文明的发展历程,也是化学物质的认识和发现历程。
(1)基态O原子中能量最高的电子所占据的原子轨道形状为___________ ,高温下 比
比 更稳定,试从核外电子排布的角度解释其原因:
更稳定,试从核外电子排布的角度解释其原因:___________ 。
(2) 分子中C元素的化合价为
分子中C元素的化合价为___________ 。类卤素 对应的酸有两种,理论上硫氰酸
对应的酸有两种,理论上硫氰酸 的沸点低于异硫氰酸
的沸点低于异硫氰酸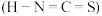 的沸点,其原因是
的沸点,其原因是___________ 。
(3) 中
中 的键角比
的键角比 的键角小,其原因为
的键角小,其原因为___________ 。
(4)在高温超导领域中,有一种化合物叫钙钛矿,其晶胞结构如图所示。
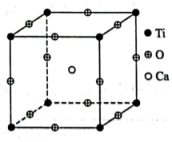
①钙钛矿的化学式为___________ ,距每个钛离子最近的氧离子的数目有___________ 个。
②设阿伏加德罗常数的值为 ,晶胞的边长为
,晶胞的边长为 ,则该晶胞的密度为
,则该晶胞的密度为
___________ 。
(1)基态O原子中能量最高的电子所占据的原子轨道形状为
 比
比 更稳定,试从核外电子排布的角度解释其原因:
更稳定,试从核外电子排布的角度解释其原因:(2)
 分子中C元素的化合价为
分子中C元素的化合价为 对应的酸有两种,理论上硫氰酸
对应的酸有两种,理论上硫氰酸 的沸点低于异硫氰酸
的沸点低于异硫氰酸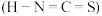 的沸点,其原因是
的沸点,其原因是(3)
 中
中 的键角比
的键角比 的键角小,其原因为
的键角小,其原因为(4)在高温超导领域中,有一种化合物叫钙钛矿,其晶胞结构如图所示。

①钙钛矿的化学式为
②设阿伏加德罗常数的值为
 ,晶胞的边长为
,晶胞的边长为 ,则该晶胞的密度为
,则该晶胞的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知锰的某种氧化物的晶胞如图所示,该氧化物的化学式为_____ ,锰离子的配位数为_____ 。(替代)

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】硒( )是人体必需微量元素之一,含硒化合物在材料和药物等领域具有重要应用。
)是人体必需微量元素之一,含硒化合物在材料和药物等领域具有重要应用。
(1) 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为_______ 。
(2) 的沸点低于
的沸点低于 ,其原因是
,其原因是_______ 。
(3)硒的两种含氧酸的酸性强弱为
_______  (填“>”或“<”)。
(填“>”或“<”)。 的空间结构为
的空间结构为_______ 。比较键角大小:气态 分子
分子_______  离子(填“>”“<”或“=”)。
离子(填“>”“<”或“=”)。

(4)关于Ⅰ~Ⅲ三种反应物,下列说法正确的有_______ 。
a.Ⅰ中仅有 键 b.Ⅰ中的
键 b.Ⅰ中的 键为非极性共价键 c.Ⅱ易溶于水 d.Ⅱ中原子的杂化轨道类型只有
键为非极性共价键 c.Ⅱ易溶于水 d.Ⅱ中原子的杂化轨道类型只有 与
与 e.Ⅰ~Ⅲ含有的元素中,O电负性最大
e.Ⅰ~Ⅲ含有的元素中,O电负性最大
(5)Ⅳ中具有孤对电子的原子有_______ 。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为_______ 。
②设X的化学式的式量为 ,晶胞边长为
,晶胞边长为 ,则晶体的密度为
,则晶体的密度为_______  (列出计算式)。
(列出计算式)。
 )是人体必需微量元素之一,含硒化合物在材料和药物等领域具有重要应用。
)是人体必需微量元素之一,含硒化合物在材料和药物等领域具有重要应用。(1)
 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为(2)
 的沸点低于
的沸点低于 ,其原因是
,其原因是(3)硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。
(填“>”或“<”)。 的空间结构为
的空间结构为 分子
分子 离子(填“>”“<”或“=”)。
离子(填“>”“<”或“=”)。
(4)关于Ⅰ~Ⅲ三种反应物,下列说法正确的有
a.Ⅰ中仅有
 键 b.Ⅰ中的
键 b.Ⅰ中的 键为非极性共价键 c.Ⅱ易溶于水 d.Ⅱ中原子的杂化轨道类型只有
键为非极性共价键 c.Ⅱ易溶于水 d.Ⅱ中原子的杂化轨道类型只有 与
与 e.Ⅰ~Ⅲ含有的元素中,O电负性最大
e.Ⅰ~Ⅲ含有的元素中,O电负性最大(5)Ⅳ中具有孤对电子的原子有
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为
②设X的化学式的式量为
 ,晶胞边长为
,晶胞边长为 ,则晶体的密度为
,则晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】黑火药是我国古代的四大发明之一,距今已有1000多年的历史,其成分是木炭(C)、硫粉(S)和硝酸钾(KNO3)。回答下列有关问题:
(1)黑火药爆炸生成无毒的气体和K2S,该反应的化学方程式为________________ 。
(2)Se与S同主族,则Se原子的核外电子排布式为〔Ar〕________ ,有____ 对成对电子。
(3)C、N、O、K的电负性由大到小的顺序是_________________ 。
(4)黑火药爆炸除生成K2S外,还生成少量K2S2,其结构类似于Na2O2。则K2S2中含有的化学键类型为_______________ 。
(5)K2S遇酸生成H2S,H2S分子中,S原子的杂化轨道类型是_________ ;KNO3可电离出NO3-,NO3-的空间构型是______________ 。
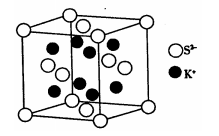
(6)K2S的晶胞结构如图所示。其中K+的配位数为_______ ,若K2S晶体的密度为ρg·cm-3,则晶胞中距离最近的两个S2-核间距为_________ cm(用NA表示阿伏伽德罗常数的值)
(1)黑火药爆炸生成无毒的气体和K2S,该反应的化学方程式为
(2)Se与S同主族,则Se原子的核外电子排布式为〔Ar〕
(3)C、N、O、K的电负性由大到小的顺序是
(4)黑火药爆炸除生成K2S外,还生成少量K2S2,其结构类似于Na2O2。则K2S2中含有的化学键类型为
(5)K2S遇酸生成H2S,H2S分子中,S原子的杂化轨道类型是
(6)K2S的晶胞结构如图所示。其中K+的配位数为
您最近一年使用:0次
【推荐3】常见离子晶体的结构
(1)NaCl晶胞
NaCl晶胞如图所示,每个Na+周围距离最近的Cl-有_______ 个(上、下、左、右、前、后各1个),构成正八面体,每个Cl-周围距离最近的Na+有_______ 个,构成正八面体,由此可推知晶体的化学式为NaCl。回答下列问题:
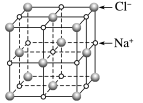
①每个Na+(Cl-)周围距离相等且最近的Na+(Cl-)是_______ 个。
②每个晶胞中实际拥有的Na+数是_______ 个,Cl-数是_______ 个。
③若晶胞参数为apm,则氯化钠晶体的密度为________ g•cm-3。
(2)CsCl晶胞
CsCl晶胞如图所示,每个Cs+周围距离最近的Cl-有_______ 个,每个Cl-周围距离最近的Cs+有_______ 个,它们均构成正六面体,由此可推知晶体的化学式为CsCl。回答下列问题:

①每个Cs+(Cl-)周围距离最近的Cs+(Cl-)有_______ 个,构成正八面体。
②每个晶胞中实际拥有的Cs+有_______ 个,Cl-有_______ 个。
③若晶胞参数为apm,则氯化铯晶体的密度为________ g•cm-3。
(1)NaCl晶胞
NaCl晶胞如图所示,每个Na+周围距离最近的Cl-有

①每个Na+(Cl-)周围距离相等且最近的Na+(Cl-)是
②每个晶胞中实际拥有的Na+数是
③若晶胞参数为apm,则氯化钠晶体的密度为
(2)CsCl晶胞
CsCl晶胞如图所示,每个Cs+周围距离最近的Cl-有

①每个Cs+(Cl-)周围距离最近的Cs+(Cl-)有
②每个晶胞中实际拥有的Cs+有
③若晶胞参数为apm,则氯化铯晶体的密度为
您最近一年使用:0次