X、Y、Z、M、Q五种短周期元素,原子序数依次增大,X的基态原子有2个未成对电子,Y的族序数为周期数的3倍,Z、M、Q在同一周期,三者的最外层电子数之和为11,Z是同周期元素中电负性最小的元素,M的价电子是Z的3倍。下列说法不正确的是
| A.Y与Z可形成含非极性共价键的化合物 |
| B.同周期中第一电离能介于M与Q之间的元素有4种 |
C.电负性: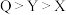 |
D.最高价氧化物对应水化物的酸性: |
22-23高二下·浙江宁波·期中 查看更多[3]
更新时间:2023-04-27 21:38:18
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】A元素最高正价和负价绝对值之差为6,B元素次外层有8个电子,BA2在水溶液中能电离出相差一个电子层结构的离子,则BA2是
| A.MgCl2 | B.MgF2 | C.NO2 | D.CO2 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】短周期元素W、X、Y、Z的原子序数依次增加,W-与Ne具有相同的电子层结构,X的族序数等于周期数,Y与Z最外层电子数之和为10。下列说法不正确的是
| A.原子半径:X>Y>Z>W | B.单质沸点:W>Y>Z |
| C.气态氢化物的稳定性:W>Z>Y | D.简单离子半径大小:Z>W>X |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】W、X、Y、Z 是原子序数依次增大的短周期主族元素,W 的氢化物水溶液能蚀刻玻璃,X、Y处于相邻位置,Y的最高正价与最低负价代数和为零,W、X 原子的最外层电子数之和与Y、Z 原子的最外层电子数之和相等。下列说法错误的是
| A.原子 半 径 :X> Y >Z >W |
| B.最高正价:W>Z>Y>X |
| C.简单氢化物的热稳定性:W>Z>Y |
| D.简单离子的电子层结构:W 与X相同 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】含有共价键的离子化合物是
| A.NaOH | B.MgF2 | C.H2O2 | D.N2 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】反应(NH4)2SiF6+4NH3•H2O═SiO2↓+6NH4F+2H2O可制纳米SiO2,下列说法正确的是
| A.NH3是极性分子 | B.NH4F是共价化合物 |
C.H2O的电子式为 | D.基态Si原子的电子排布式为[Ne]3s13p3 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列排序不正确的是
| A.酸性:HClO4>H2SO4>H3PO4 | B.热稳定性:HF>HCl>HBr |
| C.微粒半径:K+>Na+>Mg2+ | D.第一电离能:Na<Mg<Al |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】X、Y、Z、W是原子序数依次增大的短周期不同主族元素,X的2p轨道有两个未成对电子,Y元素原子半径在同周期中最大,X与Y最外层电子数之和与Z的最外层电子数相等,W元素单质常温下是淡黄色固体。下列说法正确的是
| A.第一电离能:Z>W>Y | B.Y在元素周期表中位于p区 |
| C.X、Z、W形成的单质均属于分子晶体 | D.最高价含氧酸的酸性:Z>W |
您最近半年使用:0次
【推荐3】下列叙述中,事实与对应解释不正确的是
| 事实 | 解释 | |
| A | 第一电离能:N>O | N的价层电子排布是2s22p3,为半充满较稳定 |
| B | 在氯化钠晶体中,每个Na+周围与它最近且等距的Cl-有6个 | 离子键具有饱和性 |
| C | 熔点:晶体硅<碳化硅 | 晶体硅和碳化硅均属于共价晶体,原子半径:Si>C,键长:Si-Si>Si-C,键能:Si-Si<Si-C |
| D | 酸性:HCOOH>CH3COOH | H3C-是推电子基团,使羧基中羟基的极性减小 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】硫和氮是两种常见的“明星元素”,其化合物是现代无机化学研究的最为活跃的领域之一。如图是已经合成的某硫氮化合物的分子结构,下列说法错误的是
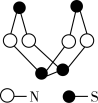

| A.该物质的分子式为S4N4 | B.该物质的熔沸点较低 |
| C.该物质的分子中不含非极性键 | D.N的电负性比S的电负性强 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列有关物质结构或性质的比较中,正确的是
A.熔点: |
B.键角: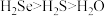 |
C.键的极性: 键 键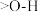 键 键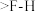 键 键 |
D.热稳定性: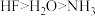 |
您最近半年使用:0次

 K2S+N2↑+3CO2↑。下列有关说法正确的是
K2S+N2↑+3CO2↑。下列有关说法正确的是


