2-甲基-2-丁醇是一种重要的有机化合物,可用于合成香料、农药等。某化学兴趣小组欲利用格氏试剂法制备2-甲基-2-丁醇。实验原理及具体操作步骤如下:
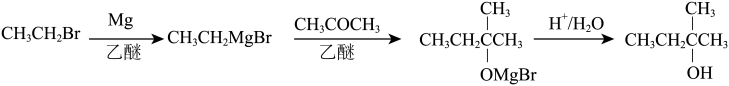
Ⅰ.乙基溴化镁的制备
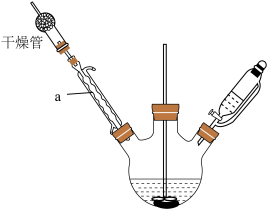
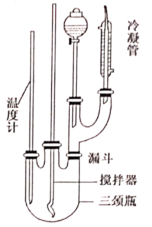
如图安装好装置(夹持仪器未画出),在三颈烧瓶中加入1.7g镁屑及一小粒碘。在恒压滴液漏斗中加入5.0mL溴乙烷和15mL无水乙醚,混匀。开动搅拌,慢慢滴加混合液,维持反应液呈微沸状态。滴加完毕后,用温热回流搅拌30min,使镁屑几乎作用完全。
Ⅱ.与丙酮的加成反应
将三颈烧瓶置于冰水浴中,在搅拌下从恒压漏斗中缓慢滴入5mL丙酮及5mL无水乙醚混合液,滴加完毕后,在室温下搅拌15min,瓶中有灰白色粘稠状固体析出。
Ⅲ.加成物的水解和产物的提取
将三颈烧瓶在冰水冷却和搅拌下,从恒压漏斗中滴入30mL20%硫酸溶液。滴加完毕后,分离出醚层,水层用无水乙醚萃取2次,合并醚层,用5%碳酸钠溶液洗涤,再用无水碳酸钾干燥。搭建蒸馏装置,热水浴蒸去乙醚后,收集95~105℃馏分。称重,计算产率。
已知:①RMgBr化学性质活泼,易与 、R′X等发生反应生成RH、R-R′;
、R′X等发生反应生成RH、R-R′;
②各物质的沸点见下表:
回答下列问题:
(1)仪器a的名称是___________ 。
(2)干燥管中无水氯化钙的作用是___________ 。
(3)微热或加入小颗粒碘单质可引发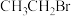 与镁屑的反应,其中碘的作用可能是
与镁屑的反应,其中碘的作用可能是___________ ;不宜使用长时间放置的镁屑进行实验,其原因是___________ 。
(4)滴加丙酮及稀硫酸时采用冰水冷却的目的是___________ 。
(5)蒸去乙醚时采用热水浴的原因是___________ 。
(6)起始加入三颈烧瓶中溴乙烷的体积为5mL,密度为1.28g/mL,最终所得产品的质量为2.69g,则2-甲基-2-丁醇的产率为___________ (结果保留2位有效数字)。

Ⅰ.乙基溴化镁的制备
如图安装好装置(夹持仪器未画出),在三颈烧瓶中加入1.7g镁屑及一小粒碘。在恒压滴液漏斗中加入5.0mL溴乙烷和15mL无水乙醚,混匀。开动搅拌,慢慢滴加混合液,维持反应液呈微沸状态。滴加完毕后,用温热回流搅拌30min,使镁屑几乎作用完全。
Ⅱ.与丙酮的加成反应
将三颈烧瓶置于冰水浴中,在搅拌下从恒压漏斗中缓慢滴入5mL丙酮及5mL无水乙醚混合液,滴加完毕后,在室温下搅拌15min,瓶中有灰白色粘稠状固体析出。
Ⅲ.加成物的水解和产物的提取
将三颈烧瓶在冰水冷却和搅拌下,从恒压漏斗中滴入30mL20%硫酸溶液。滴加完毕后,分离出醚层,水层用无水乙醚萃取2次,合并醚层,用5%碳酸钠溶液洗涤,再用无水碳酸钾干燥。搭建蒸馏装置,热水浴蒸去乙醚后,收集95~105℃馏分。称重,计算产率。
已知:①RMgBr化学性质活泼,易与
 、R′X等发生反应生成RH、R-R′;
、R′X等发生反应生成RH、R-R′;②各物质的沸点见下表:
| 物质 | 无水乙醚 | 溴乙烷 | 丙酮 | 2-甲基-2-丁醇 |
| 沸点(℃) | 34.6 | 38.4 | 56.5 | 102.5 |

回答下列问题:
(1)仪器a的名称是
(2)干燥管中无水氯化钙的作用是
(3)微热或加入小颗粒碘单质可引发
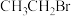 与镁屑的反应,其中碘的作用可能是
与镁屑的反应,其中碘的作用可能是(4)滴加丙酮及稀硫酸时采用冰水冷却的目的是
(5)蒸去乙醚时采用热水浴的原因是
(6)起始加入三颈烧瓶中溴乙烷的体积为5mL,密度为1.28g/mL,最终所得产品的质量为2.69g,则2-甲基-2-丁醇的产率为
更新时间:2023-05-18 10:32:25
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室由安息香制备二苯乙二酮的反应式如下:
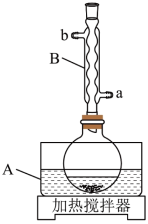
装置示意图如下图所示,实验步骤为: 冰乙酸、
冰乙酸、 水及
水及 ,边搅拌边加热,至固体全部溶解
,边搅拌边加热,至固体全部溶解
②停止加热,待沸腾平息后加入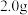 安息香,加热回流
安息香,加热回流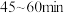
③加入 水,煮沸后冷却,有黄色固体析出
水,煮沸后冷却,有黄色固体析出
④过滤,并用冷水洗涤固体3次,得到粗品
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶
回答下列问题:
(1)仪器A中应加入___________ (填“水”或“油”)作为热传导介质
(2)仪器B的作用是___________ ;冷却水应从___________ (填“a”或“b”)口通入
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是___________ 。
(4)在本实验中, 为氧化剂且过量,其还原产物为
为氧化剂且过量,其还原产物为___________ ;某同学尝试改进本实验:采用催化量的 并通入空气制备二苯乙二酮,该方法的优点是
并通入空气制备二苯乙二酮,该方法的优点是___________ 。
(5)若粗品中混有少量未氧化的安息香,可用少量___________ 洗涤的方法除去(填标号)。若要得到更高纯度的产品,可用重结晶的方法进一步提纯
a.热水 b.乙酸 c.冷水 d.乙醇

| 物质 | 性状 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 安息香 | 白色固体 | 133 | 344 | 难溶于冷水、溶于热水、乙醇、乙酸 |
| 二苯乙二酮 | 淡黄色固体 | 95 | 347 | 不溶于水、溶于乙醇、苯、乙酸 |
| 冰乙酸 | 无色液体 | 17 | 118 | 与水、乙醇互溶 |
 冰乙酸、
冰乙酸、 水及
水及 ,边搅拌边加热,至固体全部溶解
,边搅拌边加热,至固体全部溶解②停止加热,待沸腾平息后加入
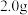 安息香,加热回流
安息香,加热回流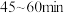
③加入
 水,煮沸后冷却,有黄色固体析出
水,煮沸后冷却,有黄色固体析出④过滤,并用冷水洗涤固体3次,得到粗品
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶

回答下列问题:
(1)仪器A中应加入
(2)仪器B的作用是
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是
(4)在本实验中,
 为氧化剂且过量,其还原产物为
为氧化剂且过量,其还原产物为 并通入空气制备二苯乙二酮,该方法的优点是
并通入空气制备二苯乙二酮,该方法的优点是(5)若粗品中混有少量未氧化的安息香,可用少量
a.热水 b.乙酸 c.冷水 d.乙醇
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】苯乙酮(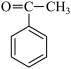 )广泛用于皂用香精中,可由苯和乙酸酐(
)广泛用于皂用香精中,可由苯和乙酸酐(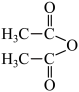 )在氯化铝的催化作用下制备。
)在氯化铝的催化作用下制备。
| 名称 | 熔点/℃ | 沸点/℃ | 密度/(g·mL-1) | 溶解性 |
| 苯 | 5.5 | 80.1 | 0.88 | 不溶于水,易溶于有机溶剂 |
| 苯乙酮 | 19.6 | 203 | 1.03 | 微溶于水,易溶于有机溶剂 |
| 乙酸酐 | -73 | 139 | 1.08 | 遇水反应,易溶于有机溶剂 |
| 乙酸 | 16.6 | 118 | 1.05 | 易溶于水,易溶于有机溶剂 |
步骤Ⅱ冷却后将反应物倒入100g冰水中,有白色胶状沉淀Al(OH)3生成,采用合适的方法处理,水层用苯萃取,合并苯层溶液,再依次用30mL5%NaOH溶液和30mL水洗涤,分离出的苯层。
步骤Ⅲ:苯层用无水硫酸镁干燥,蒸馏回收苯,再收集产品苯乙酮。
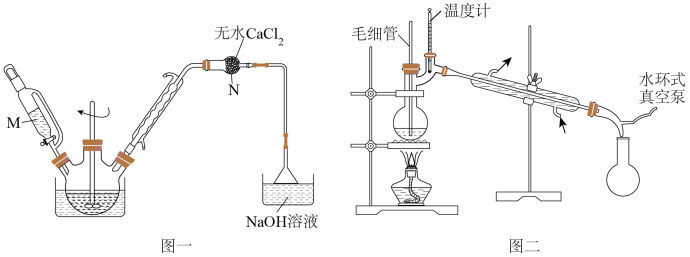
(1)仪器M的名称为
(2)步骤Ⅰ三颈烧瓶中发生反应的化学方程式为
(3)根据上述实验药品的用量,三颈烧瓶的最适宜规格为_____(填标号)。
| A.100mL | B.250mL | C.500mL | D.1000mL |
(5)本实验为收集产品用了减压蒸馏装置,如图二所示,其中毛细管的作用是
A.202℃ B.220℃ C.175℃
(6)实验中收集到24.0mL苯乙酮,则苯乙酮的产率为
(7)已知:
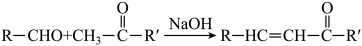 。苯乙酮(
。苯乙酮(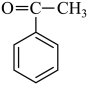 )和苯甲醛(
)和苯甲醛(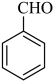 )在NaOH催化下可以合成查尔酮,查尔酮的结构简式为
)在NaOH催化下可以合成查尔酮,查尔酮的结构简式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】查尔酮是一种能制备抗炎药物的化工原料。其中一种合成路线如下:
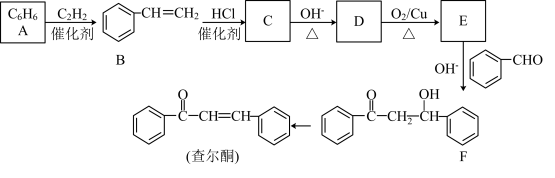
(1)B的名称为_________ ;查尔酮含有的含氧官能团名称是_________ 。
(2)A→B的反应类型是_________ ;C的结构简式为_________ 。
(3)写出E→F的化学方程式_________ 。
(4)F的同分异构体中,含有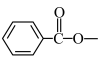 结构且水解产物为芳香醇的酯共有种
结构且水解产物为芳香醇的酯共有种_________ ,其中核磁共振氢谱吸收峰最少的分子结构简式为_________ 。
(5)已知: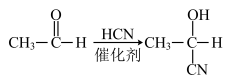 。参照上述流程,以CH2=CH-CH3为原料合成
。参照上述流程,以CH2=CH-CH3为原料合成 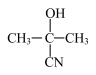 ,设计最简合成路线。
,设计最简合成路线。_______________

(1)B的名称为
(2)A→B的反应类型是
(3)写出E→F的化学方程式
(4)F的同分异构体中,含有
 结构且水解产物为芳香醇的酯共有种
结构且水解产物为芳香醇的酯共有种(5)已知:
 。参照上述流程,以CH2=CH-CH3为原料合成
。参照上述流程,以CH2=CH-CH3为原料合成  ,设计最简合成路线。
,设计最简合成路线。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】邻苯二甲酰亚胺广泛用于染料、农药医药橡胶、香料等行业,是许多重要有机精细化学品的中间体。反应原理为
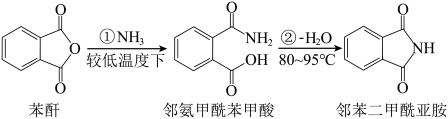
制备邻苯二甲酰亚胺的实验装置如图所示。
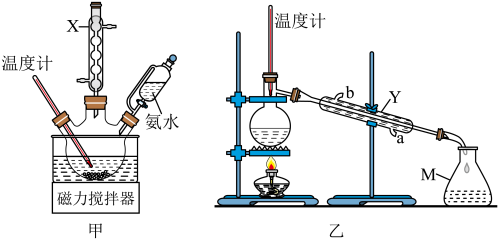
实验步骤:
向装置甲的三颈烧瓶中加入14.8000g苯酐(相对分子质量为148),然后再加入15.0mL氨水(过量),加热至冷凝管中有部分液体回流时开启搅拌,控制温度为80~95C,待苯酐固体完全反应后,改为蒸馏装置乙,继续加热,将装置中的水蒸出,体系温度逐渐升高至固体熔化。保温反应60min后,冷却至室温,洗涤、抽滤、烘干,进一步提纯得固体邻苯二甲酰亚胺(相对分子质量为147)14.1120g。
请回答下列问题:
(1)仪器M的名称是_______ 。
(2)仪器Y中冷水由_______ (填“a”或“b”)口流出。
(3)装置甲中温度控制在80—95℃,若温度过低导致的结果是_______ 。
(4)反应①中除了生成邻氨甲酰苯甲酸,还可能生成的副产物是_______ (写一种物质的结构简式)。
(5)蒸馏时,需要及时将装置中的水蒸出,目的是_______ 。
(6)该固体产品的产率是_______ 。
(7)邻苯二甲酰亚胺还可以用邻二甲苯与氨气、空气在加热条件下催化反应一步制得,写出该反应的化学方程式:_______ 。

物质 | 熔点/°C | 沸点/C | 溶解性 |
| 苯酐 | 131~134 | 284 | 不溶于冷水,微溶于热水 |
| 邻氨甲酰苯甲酸 | 140~143 | 394.2 | 稍溶于热水 |
| 邻苯二甲酰亚胺 | 232~235 | 366 | 微溶于水,易溶于碱溶液 |

实验步骤:
向装置甲的三颈烧瓶中加入14.8000g苯酐(相对分子质量为148),然后再加入15.0mL氨水(过量),加热至冷凝管中有部分液体回流时开启搅拌,控制温度为80~95C,待苯酐固体完全反应后,改为蒸馏装置乙,继续加热,将装置中的水蒸出,体系温度逐渐升高至固体熔化。保温反应60min后,冷却至室温,洗涤、抽滤、烘干,进一步提纯得固体邻苯二甲酰亚胺(相对分子质量为147)14.1120g。
请回答下列问题:
(1)仪器M的名称是
(2)仪器Y中冷水由
(3)装置甲中温度控制在80—95℃,若温度过低导致的结果是
(4)反应①中除了生成邻氨甲酰苯甲酸,还可能生成的副产物是
(5)蒸馏时,需要及时将装置中的水蒸出,目的是
(6)该固体产品的产率是
(7)邻苯二甲酰亚胺还可以用邻二甲苯与氨气、空气在加热条件下催化反应一步制得,写出该反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】溴化钙(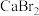 )在医药上用作中枢神经抑制药,实验室用“尿素法”制备溴化钙的主要流程如下:
)在医药上用作中枢神经抑制药,实验室用“尿素法”制备溴化钙的主要流程如下:
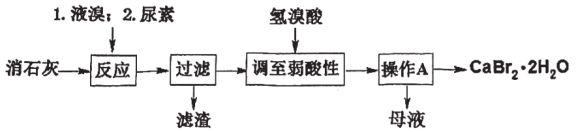
溴化钙的部分溶解度数值如下:
(1)50~70℃时,尿素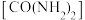 (尿素中碳为+4价)将生成的
(尿素中碳为+4价)将生成的 还原为
还原为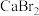 ,尿素的氧化为
,尿素的氧化为 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(2)过滤所需的玻璃仪器有_______ 。
(3)淤积中为什么要加入氢溴酸调至弱酸性?_______ 。
(4)操作 包括:将
包括:将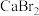 溶液蒸发浓缩至
溶液蒸发浓缩至_______ 为止,冷却结晶,过滤,洗涤,低温干燥得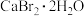 晶体。
晶体。
(5)上述流程中可以循环利用的物质是_______ 。
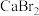 )在医药上用作中枢神经抑制药,实验室用“尿素法”制备溴化钙的主要流程如下:
)在医药上用作中枢神经抑制药,实验室用“尿素法”制备溴化钙的主要流程如下:
溴化钙的部分溶解度数值如下:
| 温度 | 0℃ | 10℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
溶解度( ) ) | 125 | 132 | 143 | 213 | 278 | 295 | 312 |
(1)50~70℃时,尿素
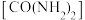 (尿素中碳为+4价)将生成的
(尿素中碳为+4价)将生成的 还原为
还原为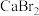 ,尿素的氧化为
,尿素的氧化为 ,该反应的化学方程式为
,该反应的化学方程式为(2)过滤所需的玻璃仪器有
(3)淤积中为什么要加入氢溴酸调至弱酸性?
(4)操作
 包括:将
包括:将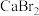 溶液蒸发浓缩至
溶液蒸发浓缩至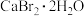 晶体。
晶体。(5)上述流程中可以循环利用的物质是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】Ⅰ.某化学小组同学用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件。
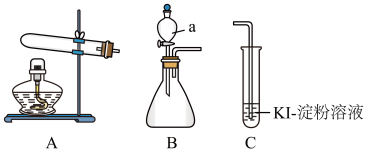
供选试剂:30% H2O2溶液、0.1mol/L H2SO4溶液、MnO2固体、KMnO4固体
该小组同学设计甲、乙、丙三组实验,记录如下:
(1)仪器a的名称是______________ 。
(2)检验A装置气密性的方法是______________ 。
(3)乙实验中O2与KI溶液反应的离子方程式是____________ 。
(4)对比甲、乙实验可知,O2与KI溶液发生反应的适宜条件是___________ 。
(5)由甲、乙、丙三实验推测,丙实验可能是B中的白雾使溶液变蓝。小组同学将B中产生的气体直接通入下列______ 溶液(填编号,下同),证明了白雾中含有H2O2。
A.酸性KMnO4 B. FeCl2 C. Na2S D.品红
Ⅱ.Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取m g KIO3(相对分子质量为214)固体配成溶液,
第二步:加入过量KI固体和H2SO4溶液,滴加指示剂,
第三步:用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为v mL。
已知:IO3-+5I-+6H+=3I2+3H2O 2S2O32-+I2=S4O62-+2I-。
回答下列问题:
(6)滴定终点的现象为________ 。
(7)c(Na2S2O3)=______________ mol·L-1。(只列出算式,不作运算)
(8)若滴定管盛装Na2S2O3溶液之前未润洗,这样测得的Na2S2O3的浓度可能______ (填“无影响”、“偏低”或“偏高”)。

供选试剂:30% H2O2溶液、0.1mol/L H2SO4溶液、MnO2固体、KMnO4固体
该小组同学设计甲、乙、丙三组实验,记录如下:
| 操作 | 现象 | |
| 甲 | 向A中加入KMnO4固体,连接A、C,点燃酒精灯 | C中有气泡冒出,溶液始终不变蓝 |
| 乙 | 向A中加入KMnO4固体,C中加入适量0.1mol/L H2SO4溶液,连接A、C,点燃酒精灯 | C中有气泡冒出,溶液变蓝 |
| 丙 | 向B的锥形瓶中加入MnO2固体,a中加入30% H2O2溶液,连接B、C,打开活塞 | B中产生无色气体并伴随大量白雾;C中有气泡冒出,溶液迅速变蓝 |
(2)检验A装置气密性的方法是
(3)乙实验中O2与KI溶液反应的离子方程式是
(4)对比甲、乙实验可知,O2与KI溶液发生反应的适宜条件是
(5)由甲、乙、丙三实验推测,丙实验可能是B中的白雾使溶液变蓝。小组同学将B中产生的气体直接通入下列
A.酸性KMnO4 B. FeCl2 C. Na2S D.品红
Ⅱ.Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取m g KIO3(相对分子质量为214)固体配成溶液,
第二步:加入过量KI固体和H2SO4溶液,滴加指示剂,
第三步:用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为v mL。
已知:IO3-+5I-+6H+=3I2+3H2O 2S2O32-+I2=S4O62-+2I-。
回答下列问题:
(6)滴定终点的现象为
(7)c(Na2S2O3)=
(8)若滴定管盛装Na2S2O3溶液之前未润洗,这样测得的Na2S2O3的浓度可能
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下。
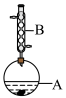
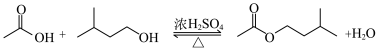
实验步㵵:在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。“…___________…”后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水 固体,静置片刻,过滤除去
固体,静置片刻,过滤除去 固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g。
固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g。
1.下列说法不正确的是:___________。
2.本实验的产率是:___________。

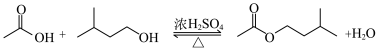
| 相对分子质量 | 密度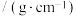 | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
 固体,静置片刻,过滤除去
固体,静置片刻,过滤除去 固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g。
固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g。1.下列说法不正确的是:___________。
| A.仪器B的名称是球形冷凝管,作用是冷凝回流 |
| B.题干部分“…___________…”表达的操作是待反应液恢复至室温 |
| C.在洗涤操作中,第一次水洗的主要目的是洗掉大部分硫酸和醋酸等水溶性物质 |
| D.在进行蒸馏操作时:若从130℃便开始收集馏分,会使实验的产率偏低 |
| A.30% | B.40% | C.60% | D.90% |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】肉桂酸是一种常见的食品香料,巴蜀中学高年级化学社成员按以下的制备原理探究了肉桂酸的制取。
 +(CH3CO)2O
+(CH3CO)2O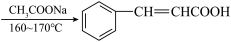 +CH3COOH
+CH3COOH
已知:a.乙酸酐溶于水发生水解反应。
b.主要试剂及物理性质如下表:
实验步骤:
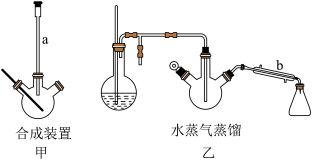
①在250 mL三口烧瓶中(如图甲)放入3 mL(3.18g)苯甲醛,8 mL(8.64g)乙酸酐,以及研细的4.2g无水碳酸钾,由于CO2的产生,反应初期会产生较多泡沫。
②采用空气冷凝管缓缓回流加热45 min。
③在搅拌下向反应液中分批加入20 mL水,再慢慢加入碳酸钠中和反应液至pH等于8。
④进行水蒸气蒸馏(如图乙),然后将三口烧瓶中的剩余液体自然冷却。
⑤加入活性炭煮沸10~15 min。
⑥进行趁热过滤,最终得到产品,干燥,称量得固体4.0g。
请回答下列问题:
(1)仪器b的名称是________________ 。
(2)合成时装置必须是干燥的,理由是____________________________ 。
(3)步骤③加入碳酸钠调pH时宜慢不宜快,否则难以准确调pH,请推测其原因是____________________________________________ 。
(4)步骤④及步骤⑤中,除去的杂质是__________________ 。
(5)步骤⑥需趁热过滤,其目的是__________________________ 。
(6)若需进一步提纯粗产品,可通过在水中__________ 的方法提纯,该实验产品的产率约是____________ 。(保留3位有效数字)
 +(CH3CO)2O
+(CH3CO)2O +CH3COOH
+CH3COOH已知:a.乙酸酐溶于水发生水解反应。
b.主要试剂及物理性质如下表:
| 名称 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(g·mL-1) | 溶解性 |
| 苯甲醛 | 106 | -26 | 179 | 1.06 | 微溶于水,易溶于乙醇 |
| 肉桂酸 | 148 | 133 | 300 | 1.248 | 难溶于冷水,易溶于乙醇、热水 |
①在250 mL三口烧瓶中(如图甲)放入3 mL(3.18g)苯甲醛,8 mL(8.64g)乙酸酐,以及研细的4.2g无水碳酸钾,由于CO2的产生,反应初期会产生较多泡沫。
②采用空气冷凝管缓缓回流加热45 min。
③在搅拌下向反应液中分批加入20 mL水,再慢慢加入碳酸钠中和反应液至pH等于8。
④进行水蒸气蒸馏(如图乙),然后将三口烧瓶中的剩余液体自然冷却。
⑤加入活性炭煮沸10~15 min。
⑥进行趁热过滤,最终得到产品,干燥,称量得固体4.0g。

请回答下列问题:
(1)仪器b的名称是
(2)合成时装置必须是干燥的,理由是
(3)步骤③加入碳酸钠调pH时宜慢不宜快,否则难以准确调pH,请推测其原因是
(4)步骤④及步骤⑤中,除去的杂质是
(5)步骤⑥需趁热过滤,其目的是
(6)若需进一步提纯粗产品,可通过在水中
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硝基苯是一种重要的化工原料,制备过程需控制温度50~60℃,在温度稍高的情况下会生成(间二硝基苯)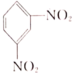 等副产物,请回答下列问题:
等副产物,请回答下列问题:
(1)写出制备硝基苯的化学反应方程式_______ 。
(2)混酸的配制:取100mL烧杯,用浓硫酸20mL、浓硝酸18mL (密度为1.4 )配制混酸,其操作过程为
)配制混酸,其操作过程为_______ 。
(3)安装反应装置:按图所示安装实验装置,冷凝管的作用是_______ 。
(4)反应步骤:
①把18mL的苯(密度为0.88 )加入到三颈瓶中,将混酸加入到分液漏斗中,逐滴滴加混酸,边滴加边搅拌。
)加入到三颈瓶中,将混酸加入到分液漏斗中,逐滴滴加混酸,边滴加边搅拌。
②混酸滴加完毕后,在加热搅拌的条件下反应半小时。加热的方法是_______ ,控制温度50~60℃的原因是_______ 。
③分离和提纯:除去产物中没有反应的酸,可在产物中加入碱溶液,然后用_______ 分液(填仪器名称),_______ 层物质为粗产品。洗涤、干燥、蒸馏得纯硝基苯18g。
(5)硝基苯的产率为_______ (提示: )。
)。
 等副产物,请回答下列问题:
等副产物,请回答下列问题:
(1)写出制备硝基苯的化学反应方程式
(2)混酸的配制:取100mL烧杯,用浓硫酸20mL、浓硝酸18mL (密度为1.4
 )配制混酸,其操作过程为
)配制混酸,其操作过程为(3)安装反应装置:按图所示安装实验装置,冷凝管的作用是
(4)反应步骤:
①把18mL的苯(密度为0.88
 )加入到三颈瓶中,将混酸加入到分液漏斗中,逐滴滴加混酸,边滴加边搅拌。
)加入到三颈瓶中,将混酸加入到分液漏斗中,逐滴滴加混酸,边滴加边搅拌。②混酸滴加完毕后,在加热搅拌的条件下反应半小时。加热的方法是
③分离和提纯:除去产物中没有反应的酸,可在产物中加入碱溶液,然后用
(5)硝基苯的产率为
 )。
)。
您最近一年使用:0次



