工业上利用焦炭在石灰窑中燃烧放热,使石灰石分解生产CO2。主要反应如下:
C+O2→CO2①, CaCO3→CO2↑+CaO ②
(1)含碳酸钙95%的石灰石2.0 t按②完全分解(设杂质不分解),可得标准状况下CO2的体积为_________________ m3。
(2)纯净的CaCO3和焦炭按①②完全反应,当窑内配比率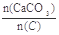 =2.2时,窑气中CO2的最大体积分数为
=2.2时,窑气中CO2的最大体积分数为_______________ ?(设空气只含N2与O2,且体积比为4∶1,下同)
(3)某次窑气成分如下:O20.2%,CO 0.2%,CO241.6%,其余为N2。则此次窑内配比率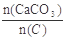 为
为_______________ ?
C+O2→CO2①, CaCO3→CO2↑+CaO ②
(1)含碳酸钙95%的石灰石2.0 t按②完全分解(设杂质不分解),可得标准状况下CO2的体积为
(2)纯净的CaCO3和焦炭按①②完全反应,当窑内配比率
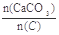 =2.2时,窑气中CO2的最大体积分数为
=2.2时,窑气中CO2的最大体积分数为(3)某次窑气成分如下:O20.2%,CO 0.2%,CO241.6%,其余为N2。则此次窑内配比率
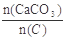 为
为
14-15高二上·吉林·期末 查看更多[4]
(已下线)2013-2014学年吉林省吉林一中高二上学期期末考试化学试卷上海交通大学附属中学2017-2018学年高一上学期期中考试化学试题上海交大附中2017-2018学年高一(上)期中化学试卷(已下线)上海市嘉定区2010届高三上学期期末考试化学试题
更新时间:2014-01-21 17:22:59
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】锌是人体生长发育、维持器官正常功能的微量元素,人体缺锌会引起多种疾病,因此缺锌者可通过服用葡萄糖酸锌等保健品来补锌。已知葡萄糖酸锌的化学式为C12H22O14Zn,请回答:
(1)葡萄糖酸锌中含锌元素的质量分数为多少?(结果保留至0.1%)
(2)现有一支20 mL的葡萄糖酸锌口服液,其中含锌6.5 mg,那么该口服液中葡萄糖酸锌的物质的量浓度为多少?
(1)葡萄糖酸锌中含锌元素的质量分数为多少?(结果保留至0.1%)
(2)现有一支20 mL的葡萄糖酸锌口服液,其中含锌6.5 mg,那么该口服液中葡萄糖酸锌的物质的量浓度为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】请回答下列问题:
(1)5.4gH2O中含有__________ mol H。
(2)硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO 的物质的量是
的物质的量是________ 。
(3)3.01×1024个OH-与__________ mol NH3的质量相同。
(4)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为__________ 。
(5)一定温度和压强下,3L气体A2与9L气体B2完全化合生成6L气体C,则气体C的化学式为__________ (用A、B表示)。
(1)5.4gH2O中含有
(2)硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO
 的物质的量是
的物质的量是(3)3.01×1024个OH-与
(4)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为
(5)一定温度和压强下,3L气体A2与9L气体B2完全化合生成6L气体C,则气体C的化学式为
您最近一年使用:0次
【推荐3】回答下列问题
(1)与16g氧气所含原子总数相同的氨气是___________ g。
(2)已知某硫酸铜溶液的质量百分数为20%,密度为1.2g/cm3,该溶液的物质的量浓度为___________ 。
(3)标准状况下的CH4和CO的混合气体8.96L,其质量为7.6g,则混合气体平均相对分子质量为___________ ,该混合气体对H2的相对密度为___________ ,CO的质量为___________ 。
(4)用1L 1.0mol/L NaOH溶液吸收0.8molCO2,所得溶液中Na2CO3和NaHCO3的物质的量浓度之比是___________ 。
(1)与16g氧气所含原子总数相同的氨气是
(2)已知某硫酸铜溶液的质量百分数为20%,密度为1.2g/cm3,该溶液的物质的量浓度为
(3)标准状况下的CH4和CO的混合气体8.96L,其质量为7.6g,则混合气体平均相对分子质量为
(4)用1L 1.0mol/L NaOH溶液吸收0.8molCO2,所得溶液中Na2CO3和NaHCO3的物质的量浓度之比是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)实验室由Al盐制备Al(OH)3最佳选择NH3·H2O,其离子反应方程式:____________________________
(2)12.4g Na2X含有0.4mol Na+, Na2X的摩尔质量为________ 。
(3)由氨气和氢气组成的混合气体的平均相对分子质量为12,则氨气和氢气的物质的量之比为_________
(4)已知 离子可与R2-离子反应,R2-被氧化为R单质,
离子可与R2-离子反应,R2-被氧化为R单质, 的还原产物中M为+3价;又已知100mL c(
的还原产物中M为+3价;又已知100mL c( )=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为
)=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为__________
A.4 B.5 C.6 D.7
(2)12.4g Na2X含有0.4mol Na+, Na2X的摩尔质量为
(3)由氨气和氢气组成的混合气体的平均相对分子质量为12,则氨气和氢气的物质的量之比为
(4)已知
 离子可与R2-离子反应,R2-被氧化为R单质,
离子可与R2-离子反应,R2-被氧化为R单质, 的还原产物中M为+3价;又已知100mL c(
的还原产物中M为+3价;又已知100mL c( )=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为
)=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为A.4 B.5 C.6 D.7
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol·L-1的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,试回答下列问题:

(1)原NaOH溶液的物质的量浓度为_______________ 。
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是____________ ,其物质的量之比为___ 。
(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况下)的最大值为____ mL。
(4)硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-889.6 kJ·mol-1①
N2(g)+2O2(g)===2NO2(g)ΔH=+67.7 kJ·mol-1②
则CH4还原NO2生成水蒸气和氮气的热化学方程式是_____________ 。

(1)原NaOH溶液的物质的量浓度为
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是
(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况下)的最大值为
(4)硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-889.6 kJ·mol-1①
N2(g)+2O2(g)===2NO2(g)ΔH=+67.7 kJ·mol-1②
则CH4还原NO2生成水蒸气和氮气的热化学方程式是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】为测定某工厂烟道气中SO2的含量,使16.00L烟道气缓慢通过1L水,设SO2完全被吸收,且溶液体积不改变。取出其中20.00mL溶液,加入2—3滴指示剂后,用1.18×10-3mol/L的饱和碘水(密度为1g/cm3)滴定,耗去19.07mL达到终点。
求 (1)实验条件下碘的溶解度_____________ ;
(2)该厂烟道气中SO2的含量____________ (mg/L);
(3)为简便计算,在其余操作都不变的情况下,要使滴定时每5mL碘水相当于烟道气中含SO21mg/L,则所配制的碘水的物质的量浓度为_______________ ?
求 (1)实验条件下碘的溶解度
(2)该厂烟道气中SO2的含量
(3)为简便计算,在其余操作都不变的情况下,要使滴定时每5mL碘水相当于烟道气中含SO21mg/L,则所配制的碘水的物质的量浓度为
您最近一年使用:0次
【推荐2】(1)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为________ 。(计算结果保留两位小数)
(2)为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸的硫铁矿烧渣(铁主要以Fe2O3存在)转变成重要的化工原料FeSO4(反应条件略)。

活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4,不考虑其它反应。假如烧渣中的铁全部视为Fe2O3,其含量为50%。将a kg质量分数为b%的硫酸加入到c kg烧渣中浸取,铁的浸取率为96%,其它杂质浸出消耗的硫酸以及调pH后溶液呈微酸性所残留的硫酸忽略不计。按上述流程,第Ⅲ步应加入FeCO3________ kg。
(3)NaCN超标的电镀废水可用两段氧化法处理:NaCN与NaClO反应,生成NaOCN和NaCl,NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2。已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。处理100m3含NaCN 10.3mg/L的废水,实际至少需NaClO________ g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5mg/L,达到排放标准。
(2)为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸的硫铁矿烧渣(铁主要以Fe2O3存在)转变成重要的化工原料FeSO4(反应条件略)。

活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4,不考虑其它反应。假如烧渣中的铁全部视为Fe2O3,其含量为50%。将a kg质量分数为b%的硫酸加入到c kg烧渣中浸取,铁的浸取率为96%,其它杂质浸出消耗的硫酸以及调pH后溶液呈微酸性所残留的硫酸忽略不计。按上述流程,第Ⅲ步应加入FeCO3
(3)NaCN超标的电镀废水可用两段氧化法处理:NaCN与NaClO反应,生成NaOCN和NaCl,NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2。已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。处理100m3含NaCN 10.3mg/L的废水,实际至少需NaClO
您最近一年使用:0次



