某化学兴趣小组为探究 的性质,按如图所示装置进行实验。
的性质,按如图所示装置进行实验。
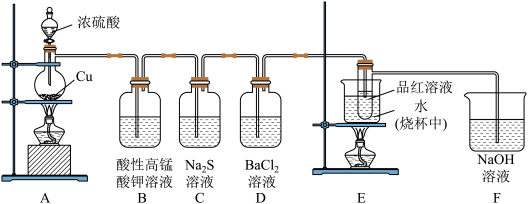
(1)装置A中反应的化学方程式为___________ 。
(2)装置B中酸性 溶液褪色,反应的离子方程式是
溶液褪色,反应的离子方程式是___________ 。装置C中产生淡黄色浑浊,体现了 的
的___________ 性。
(3)通入足量 后D中仍无明显现象,将其分成两份,分别加入列物质后均产生白色沉淀。
后D中仍无明显现象,将其分成两份,分别加入列物质后均产生白色沉淀。
(4)装置E的目的是探究 与品红作用的可逆性,请写出实验操作及现象
与品红作用的可逆性,请写出实验操作及现象___________ 。
(5)F装置中发生反应的离子方程式为___________ 。
 的性质,按如图所示装置进行实验。
的性质,按如图所示装置进行实验。
(1)装置A中反应的化学方程式为
(2)装置B中酸性
 溶液褪色,反应的离子方程式是
溶液褪色,反应的离子方程式是 的
的(3)通入足量
 后D中仍无明显现象,将其分成两份,分别加入列物质后均产生白色沉淀。
后D中仍无明显现象,将其分成两份,分别加入列物质后均产生白色沉淀。| 加入的物质 |  | 氨水 |
| 沉淀的化学式 | ① | ② |
 与品红作用的可逆性,请写出实验操作及现象
与品红作用的可逆性,请写出实验操作及现象(5)F装置中发生反应的离子方程式为
更新时间:2023-05-01 21:32:42
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】物质M是一种日常生活中不可缺少的调味品.已知C可在D中燃烧发出苍白色火焰,M与其他物质的转化关系如图所示(部分产物已略去)
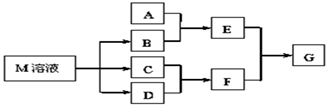
(1)写出用惰性电极电解M溶液的离子方程式_____ 。
(2)比较B中各元素原子半径由大到小_____ (填元素符号)。
(3)若A是一种酸性氧化物,且可用于制造玻璃,则G的化学式是_____ 。
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是_____ 。
(5)若A是一种盐,A溶液与B溶液混合产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,则由A转化成E的离子方程式是_____ 。
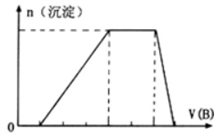
(6)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、CO32﹣、SO42﹣中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子及其浓度之比为_____ 。
(7)若E可用于检验葡萄糖的存在,写出G溶液充分蒸发灼烧后的产物与乙醇反应的化学方程式为_____ 。

(1)写出用惰性电极电解M溶液的离子方程式
(2)比较B中各元素原子半径由大到小
(3)若A是一种酸性氧化物,且可用于制造玻璃,则G的化学式是
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是
(5)若A是一种盐,A溶液与B溶液混合产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,则由A转化成E的离子方程式是
(6)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、CO32﹣、SO42﹣中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子及其浓度之比为

(7)若E可用于检验葡萄糖的存在,写出G溶液充分蒸发灼烧后的产物与乙醇反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表为八种短周期主族元素的部分性质(已知铍的原子半径为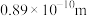 ):
):
(1)元素Z在元素周期表中的位置为_______ 。
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:_______ 。
(3)R与T相比,非金属性较强的是_______ (填元素符号),下列事实能证明这一结论的是_______ (填标号)。
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性: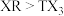
c.最高价氧化物对应水化物的酸性:
(4)J与Q相比,金属性较强的是_______ (填元素符号),能证明这一结论的依据是_______ 。
(5)根据表中数据推测,M的原子半径的最小范围是_______ 。
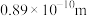 ):
):| 元素代号 | X | Y | Z | M | R | J | Q | T |
原子半径 | 0.74 | 0.75 |  | 0.99 | 1.86 | 1.43 | 1.10 | |
| 主要化合价 |  |  、 、 |  、 、 |  、 、 |  |  |  、 、 | |
| 其他 | 原子核内无中子 | 重要的半导体材料 | 有两种氧化物 |
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:
(3)R与T相比,非金属性较强的是
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性:
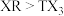
c.最高价氧化物对应水化物的酸性:

(4)J与Q相比,金属性较强的是
(5)根据表中数据推测,M的原子半径的最小范围是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】钛是航空、军工、电力等领域的重要原材料。地壳中的含钛矿石之一是金红石 ,其是冶炼钛的重要原料。生产钛的工艺流程如图:
,其是冶炼钛的重要原料。生产钛的工艺流程如图:
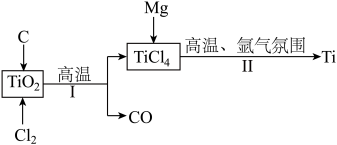
已知:①常温下,钛既不与常见非金属单质反应,也不与强酸反应;
②加热时,钛可以和常见的非金属单质反应。
(1)在反应I中:
①下列有关 的说法正确的是
的说法正确的是_______ (填标号)。
A.属于酸性氧化物 B.摩尔质量为28 C.为可燃性气体 D.具有还原性
②反应I的化学方程式为_______ 。
③每转移 电子,同时生成
电子,同时生成 的体积为
的体积为_______ (标准状况下)。
(2)在反应II中:
①氩气的作用为_______ 。
②该反应的基本反应类型为_______ 。
(3)为了测定反应II制得的金属钛(杂质仅含 )中的钛元素含量。常温下,取
)中的钛元素含量。常温下,取 反应II制得的金属钛置于烧杯中,往烧杯中逐滴滴入物质的量浓度为
反应II制得的金属钛置于烧杯中,往烧杯中逐滴滴入物质的量浓度为 的稀硫酸,当不再出现气泡时,共用去
的稀硫酸,当不再出现气泡时,共用去 稀硫酸:
稀硫酸:
①上述反应的离子方程式为_______ 。
②金属钛的质量分数为_______ (用含m、c、V的代数式表示)。
 ,其是冶炼钛的重要原料。生产钛的工艺流程如图:
,其是冶炼钛的重要原料。生产钛的工艺流程如图:
已知:①常温下,钛既不与常见非金属单质反应,也不与强酸反应;
②加热时,钛可以和常见的非金属单质反应。
(1)在反应I中:
①下列有关
 的说法正确的是
的说法正确的是A.属于酸性氧化物 B.摩尔质量为28 C.为可燃性气体 D.具有还原性
②反应I的化学方程式为
③每转移
 电子,同时生成
电子,同时生成 的体积为
的体积为(2)在反应II中:
①氩气的作用为
②该反应的基本反应类型为
(3)为了测定反应II制得的金属钛(杂质仅含
 )中的钛元素含量。常温下,取
)中的钛元素含量。常温下,取 反应II制得的金属钛置于烧杯中,往烧杯中逐滴滴入物质的量浓度为
反应II制得的金属钛置于烧杯中,往烧杯中逐滴滴入物质的量浓度为 的稀硫酸,当不再出现气泡时,共用去
的稀硫酸,当不再出现气泡时,共用去 稀硫酸:
稀硫酸:①上述反应的离子方程式为
②金属钛的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
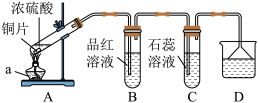
【推荐1】铜丝和浓硫酸反应的装置图如下。
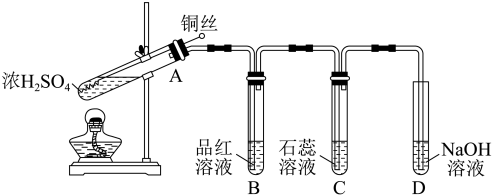
(1)A中反应的化学方程式是_______ 。
(2)A中反应开始后,B中的现象是_______ ,C中的现象是_______ 。
(3)D中NaOH溶液的作用是_______ 。

(1)A中反应的化学方程式是
(2)A中反应开始后,B中的现象是
(3)D中NaOH溶液的作用是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图各方框内字母均表示一步反应中的某些反应物或生成物,其中X与C焰色反应均呈黄色,X分解时以1:1:1的比例得到化合物A、B、C,常温下A为一种常见的无色液体,B、D为无色气体,B是酸雨污染的主要原因,实验室中常用C与F的浓溶液反应来制备少量的B。
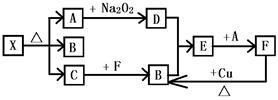
(1)写出下列各物质的化学式:A___ ,B___ ,C___ ,E___ 。
(2)①写出框图中下列转化的化学方程式:F与Cu作用生成B___ ;C与F生成B___ ;
②工业上制备F的工艺方法被称为___ ,生成B的设备名称为___ ,此法产生的含有B的废气常用C的水溶液作为吸收剂,写出吸收生成X的离子方程式___ 。

(1)写出下列各物质的化学式:A
(2)①写出框图中下列转化的化学方程式:F与Cu作用生成B
②工业上制备F的工艺方法被称为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】如图是实验室制取SO2,并验证SO2的某些性质的装置(夹持装置和加热装置已略,气密性已检验)。请回答下列问题:
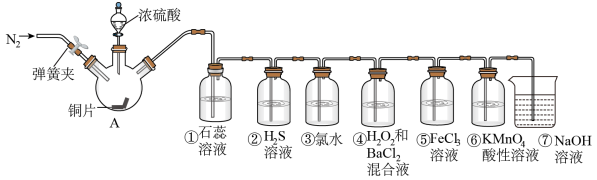
(1)在A中发生反应的化学方程式为:__________ 。
(2)③中化学反应方程式____ ,④中产生白色沉淀,离子方程式为________ ,⑤中的现象见溶液由黄色变为浅绿色,其反应的离子方程式为_________ 。
(3)能体现出SO2还原性的实验序号是____ 。
(4)实验结束后需要通入N2,其目的____ 。

(1)在A中发生反应的化学方程式为:
(2)③中化学反应方程式
(3)能体现出SO2还原性的实验序号是
(4)实验结束后需要通入N2,其目的
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题。
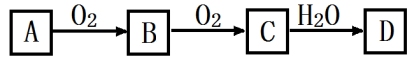
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是_______ ;在工业生产中,B气体的大量排放被雨水吸收后形成了_______ 而污染了环境。
②写出D的浓溶液与金属Cu反应的化学方程式______ ;若2molCu与足量D的浓溶液的浓溶液反应,其中体现酸性作用的D消耗_______ mol,转移电子数_______ NA。
(2)若A在常温下为气体,C是红棕色的气体。
① A的电子式_______ ;C与水反应的化学方程式_______ 。
② 将收集满V mL C的试管倒立在盛有水的水槽中,剩余气体体积为_______ mL,若要使液体完全充满试管,可以采取缓缓通入_______ mLO2 。
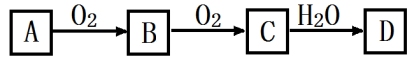
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是
②写出D的浓溶液与金属Cu反应的化学方程式
(2)若A在常温下为气体,C是红棕色的气体。
① A的电子式
② 将收集满V mL C的试管倒立在盛有水的水槽中,剩余气体体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学小组为了研究SO2和Cl2的漂白性,设计了如图所示的实验装置:
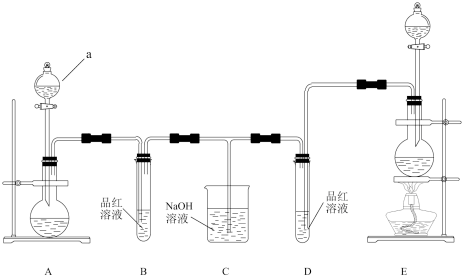
试完成下列空格:
(1)仪器a的名称_______ 。
(2)E装置中发生反应的离子方程式是_______ 。
(3)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是_______ 。
(4)利用下图所示装置探究两种气体按不同比例混合后漂白性的强弱。
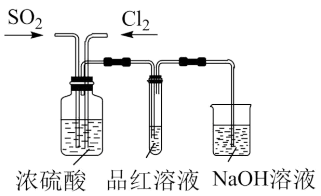
①盛有浓硫酸洗气瓶的作用是_______ ;
②实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其可能原因是_______ (用相应的离子方程式作答);

试完成下列空格:
(1)仪器a的名称
(2)E装置中发生反应的离子方程式是
(3)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是
(4)利用下图所示装置探究两种气体按不同比例混合后漂白性的强弱。

①盛有浓硫酸洗气瓶的作用是
②实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其可能原因是
您最近一年使用:0次