甲基丙烯酸甲酯是合成有机玻璃的单体,有关物质的性质如下:
某小组拟制备甲基丙烯酸甲酯并探究其性质,装置如图所示(夹持及加热仪器略)。

向三颈瓶中依次加入20 mL甲醇、5 mL浓硫酸、30 mL甲基丙烯酸及沸石少许,充分搅拌,加热。
(1)向其中加入沸石的目的是___________ 。
(2)使用油水分离器的作用是___________ 。
(3)实验结束后,提纯产品的流程如下:
混合液 产品
产品
①水洗2的目的是___________ 。
②加入硫酸钠粉末的作用是___________ 。
③蒸馏操作中收集产品的温度约为___________ 。
(4)设计简单实验检验产品中含碳碳双键:___________ 。
(5)甲基丙烯酸甲酯另一种合成方法为 ,已知该反应的原子利用率为100%,则A的结构简式为
,已知该反应的原子利用率为100%,则A的结构简式为___________ 。
| 物质 | 沸点/℃ | 溶解性 |
| 甲醇 | 64.7 | 易溶于水和有机溶剂 |
甲基丙烯酸 | 161 | 溶于水,易溶于有机溶剂 |
| 甲基丙烯酸甲酯 | 100 | 易溶于有机溶剂,微溶于水 |

向三颈瓶中依次加入20 mL甲醇、5 mL浓硫酸、30 mL甲基丙烯酸及沸石少许,充分搅拌,加热。
(1)向其中加入沸石的目的是
(2)使用油水分离器的作用是
(3)实验结束后,提纯产品的流程如下:
混合液
 产品
产品①水洗2的目的是
②加入硫酸钠粉末的作用是
③蒸馏操作中收集产品的温度约为
(4)设计简单实验检验产品中含碳碳双键:
(5)甲基丙烯酸甲酯另一种合成方法为
 ,已知该反应的原子利用率为100%,则A的结构简式为
,已知该反应的原子利用率为100%,则A的结构简式为
更新时间:2023-05-12 14:48:49
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某课外小组设计的制备乙酸乙酯的装置如图所示。

查阅资料知:
Ⅰ. 可与乙醇反应生成不溶于有机溶剂而溶于水的结晶醇化物。
可与乙醇反应生成不溶于有机溶剂而溶于水的结晶醇化物。
Ⅱ.有关数据:
主要实验步骤如下:
①按如图所示连接好装置(装置气密性良好),A中盛有浓硫酸,B中盛有乙醇和乙酸的混合溶液、碎瓷片,D中盛有含酚酞的饱和 溶液。
溶液。
②打开A中活塞,逐滴滴加浓硫酸,用小火均匀地加热装有混合溶液的圆底烧瓶。
③待D中收集到一定量产物后停止加热,撤出C,将D中混合物搅拌,然后静置分层。
④分离出乙酸乙酯层,洗涤、干燥。
回答下列问题:
(1)浓硫酸的作用是___________ ;若用同位素 示踪法来确定产物水分子中氧原子的提供者,写出能表示
示踪法来确定产物水分子中氧原子的提供者,写出能表示 位置的制取乙酸乙酯的化学方程式:
位置的制取乙酸乙酯的化学方程式:_____________ 。
(2)上述实验中饱和 溶液的作用是
溶液的作用是_________ (填标号)。
A.反应乙酸和乙醇
B.反应乙酸并溶解部分乙醇
C.乙酸乙酯在饱和Na2CO3溶液中的溶解度比在水中的小,有利于分层析出
D.加快酯的生成速率,提高其产率
(3)该小组成员将教材中制取乙酸乙酯的实验装置进行了改进,一是将发生装置中的大试管换成了圆底烧瓶,其优点是_____________ ;二是在导管末端连接了球形干燥管,优点是______________ ;步骤②中需要小火均匀加热,其主要理由是____________ 。
(4)写出步骤③中观察到的现象:___________ ;分离出乙酸乙酯层后,一般用饱和食盐水和饱和氯化钙溶液洗涤乙酸乙酯层,可除去__________ (填名称)杂质;为了干燥乙酸乙酯,可选用的干燥剂为__________ (填标号)。
A. B.无水
B.无水 C.NaOH固体 D.碱石灰
C.NaOH固体 D.碱石灰
(5)该小组成员又设计了如图所示的制取乙酸乙酯的装置(夹持装置、加热装置均已略去),与上图所示的装置相比,本装置的主要优点有_____________ 。


查阅资料知:
Ⅰ.
 可与乙醇反应生成不溶于有机溶剂而溶于水的结晶醇化物。
可与乙醇反应生成不溶于有机溶剂而溶于水的结晶醇化物。Ⅱ.有关数据:
| 物质 | 乙醇 | 乙酸 | 乙酸乙酯 | 浓硫酸(98%) |
| 沸点/℃ | 78.5 | 117.9 | 77.0 | 338.0 |
①按如图所示连接好装置(装置气密性良好),A中盛有浓硫酸,B中盛有乙醇和乙酸的混合溶液、碎瓷片,D中盛有含酚酞的饱和
 溶液。
溶液。②打开A中活塞,逐滴滴加浓硫酸,用小火均匀地加热装有混合溶液的圆底烧瓶。
③待D中收集到一定量产物后停止加热,撤出C,将D中混合物搅拌,然后静置分层。
④分离出乙酸乙酯层,洗涤、干燥。
回答下列问题:
(1)浓硫酸的作用是
 示踪法来确定产物水分子中氧原子的提供者,写出能表示
示踪法来确定产物水分子中氧原子的提供者,写出能表示 位置的制取乙酸乙酯的化学方程式:
位置的制取乙酸乙酯的化学方程式:(2)上述实验中饱和
 溶液的作用是
溶液的作用是A.反应乙酸和乙醇
B.反应乙酸并溶解部分乙醇
C.乙酸乙酯在饱和Na2CO3溶液中的溶解度比在水中的小,有利于分层析出
D.加快酯的生成速率,提高其产率
(3)该小组成员将教材中制取乙酸乙酯的实验装置进行了改进,一是将发生装置中的大试管换成了圆底烧瓶,其优点是
(4)写出步骤③中观察到的现象:
A.
 B.无水
B.无水 C.NaOH固体 D.碱石灰
C.NaOH固体 D.碱石灰(5)该小组成员又设计了如图所示的制取乙酸乙酯的装置(夹持装置、加热装置均已略去),与上图所示的装置相比,本装置的主要优点有

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】以粮食为原料制取乙醇并利用其制备乙酸乙酯(C)和高分子材料(G)的流程如下:
ⅰ.D的产量可以用来衡量一个国家石油化工水平。
ⅱ.饱和 水溶液pH为5.6。
水溶液pH为5.6。
(1)某兴趣小组尝试利用该原理酿制米酒。
①《齐民要术》中记载“浸曲三日,如鱼眼汤沸,酘米。其米绝令精细”。此中“曲”为酒曲,含有酶,在反应中起___________ 作用。“精细”即将米研磨为粉状,目的是___________ 。
②为了更好地了解米的发酵过程,小组同学每隔24小时测定米酒的酒精度和pH,连续10天,收集相关数据绘制了实验数据图。 。乙同学认为不合理,其依据一是
。乙同学认为不合理,其依据一是___________ ;依据二是乙醇中含官能团___________ (填名称),在一定条件下会被氧化成B且酸性比碳酸强。
(2)“酒越陈越香”是因为生成酯类物质。
①反应Ⅰ的化学方程式是___________ ,其中n(氧化剂):n(还原剂)=___________ 。
②反应Ⅲ的发生装置如图所示,有关说法正确的是___________ 。 溶液。
溶液。
b.实验时,先加浓硫酸,再加无水乙醇和冰醋酸。
c.一段时间后,观察到X溶液的液面上有一层无色有特殊香味的油状液体。
d.实验结束时,采用蒸发的方法将乙酸乙酯从混合物中分离出来。
(3)①D也可由戊烷裂化裂解制得。写出一氯代物只有一种的戊烷同分异构体的结构简式___________ 。
②F→G为加聚反应,化学方程式是___________ 。
(4)在反应Ⅰ→Ⅵ中,属于加成反应的是___________ 。
(5)研究资料表明,酿酒的过程中会产生乳酸( ),请依据反应Ⅲ推测其生成的六元环酯(
),请依据反应Ⅲ推测其生成的六元环酯(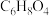 )的结构简式
)的结构简式___________ 。

ⅰ.D的产量可以用来衡量一个国家石油化工水平。
ⅱ.饱和
 水溶液pH为5.6。
水溶液pH为5.6。(1)某兴趣小组尝试利用该原理酿制米酒。
①《齐民要术》中记载“浸曲三日,如鱼眼汤沸,酘米。其米绝令精细”。此中“曲”为酒曲,含有酶,在反应中起
②为了更好地了解米的发酵过程,小组同学每隔24小时测定米酒的酒精度和pH,连续10天,收集相关数据绘制了实验数据图。

 。乙同学认为不合理,其依据一是
。乙同学认为不合理,其依据一是(2)“酒越陈越香”是因为生成酯类物质。
①反应Ⅰ的化学方程式是
②反应Ⅲ的发生装置如图所示,有关说法正确的是

 溶液。
溶液。b.实验时,先加浓硫酸,再加无水乙醇和冰醋酸。
c.一段时间后,观察到X溶液的液面上有一层无色有特殊香味的油状液体。
d.实验结束时,采用蒸发的方法将乙酸乙酯从混合物中分离出来。
(3)①D也可由戊烷裂化裂解制得。写出一氯代物只有一种的戊烷同分异构体的结构简式
②F→G为加聚反应,化学方程式是
(4)在反应Ⅰ→Ⅵ中,属于加成反应的是
(5)研究资料表明,酿酒的过程中会产生乳酸(
 ),请依据反应Ⅲ推测其生成的六元环酯(
),请依据反应Ⅲ推测其生成的六元环酯(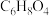 )的结构简式
)的结构简式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】乙醚(CH3CH2OCH2CH3)曾经用作麻醉剂,实验室中可将乙醇、浓硫酸的混合液加热至 140℃制取一定量的乙醚,制备原理、装置、有关物质的部分性质如下(夹持装置、加热仪器和沸石均略去):
2CH3CH2OH CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O

回答下列问题:
(1)温度计 X 的水银球应位于_____________________ 。
(2)使用仪器 B 与不使用仪器 B 相比,其优点是_____________________ 。
(3)所得到的乙醚中含有一定量的乙醇及酸性物质。为得到高纯度的乙醚,可依次用NaOH 溶液、水洗涤;然后用无水 CaCl2干燥,最后进行蒸馏精制。
① 洗涤操作应在_____________ (填仪器名称)中进行。
② 蒸馏精制时,最好的加热方式是________________________ 。
③ 若实验中使用了57.5mL 无水乙醇, 最后得到乙醚 18.0mL,则乙醚的产率为_____ 。
(4)实验中,发现 A 中的液体会变黑; E 中的溶液会逐渐褪色,加热后又会变红。
① A 中溶液颜色变黑的原因是________________________
②乙醇、浓硫酸的混合液在加热条件下会有副反应发生,生成两种常见的无机气体,该副反应的化学方程式为______________________ 。
(5)要证明该反应中有 CO2生成,在 F 后面连接一个盛有澄清石灰水的洗气瓶,并将F中的液体改为______ 溶液。
2CH3CH2OH
 CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
| 沸点/℃ | 水溶性 | 密度(g/mL) | |
| 乙醇 | 78 | 混溶 | 0.8 |
| 乙醚 | 34.6 | 难溶 | 0.7 |
(1)温度计 X 的水银球应位于
(2)使用仪器 B 与不使用仪器 B 相比,其优点是
(3)所得到的乙醚中含有一定量的乙醇及酸性物质。为得到高纯度的乙醚,可依次用NaOH 溶液、水洗涤;然后用无水 CaCl2干燥,最后进行蒸馏精制。
① 洗涤操作应在
② 蒸馏精制时,最好的加热方式是
③ 若实验中使用了57.5mL 无水乙醇, 最后得到乙醚 18.0mL,则乙醚的产率为
(4)实验中,发现 A 中的液体会变黑; E 中的溶液会逐渐褪色,加热后又会变红。
① A 中溶液颜色变黑的原因是
②乙醇、浓硫酸的混合液在加热条件下会有副反应发生,生成两种常见的无机气体,该副反应的化学方程式为
(5)要证明该反应中有 CO2生成,在 F 后面连接一个盛有澄清石灰水的洗气瓶,并将F中的液体改为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】乙基香草醛(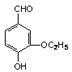 )是食品添加剂的增香原料,其香味比香草醛更加浓郁。
)是食品添加剂的增香原料,其香味比香草醛更加浓郁。
(1)写出乙基香草醛分子中含氧官能团的名称___________ 。
(2)乙基香草醛的同分异构体A是一种有机酸,A可发生以下变化:
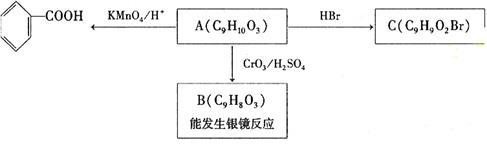
提示:RCH2OH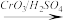 RCHO
RCHO
(a)由A→C的反应属于________ (填反应类型)。
(b)写出A的结构简式_______________ 。
(c)写出能发生银镜反应的苯甲酸的同分异构体______________________ 。
(3)乙基香草醛的一种同分异构体D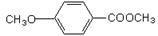 是一种医药中间体。请设计合理方案用茴香醛
是一种医药中间体。请设计合理方案用茴香醛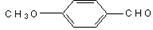 合成D(其他原料自选,用反应流程图表示,并注明必要的反应条件)。
合成D(其他原料自选,用反应流程图表示,并注明必要的反应条件)。
例如: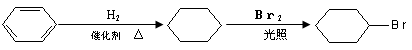
______________________________________________________________
 )是食品添加剂的增香原料,其香味比香草醛更加浓郁。
)是食品添加剂的增香原料,其香味比香草醛更加浓郁。(1)写出乙基香草醛分子中含氧官能团的名称
(2)乙基香草醛的同分异构体A是一种有机酸,A可发生以下变化:

提示:RCH2OH
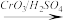 RCHO
RCHO(a)由A→C的反应属于
(b)写出A的结构简式
(c)写出能发生银镜反应的苯甲酸的同分异构体
(3)乙基香草醛的一种同分异构体D
 是一种医药中间体。请设计合理方案用茴香醛
是一种医药中间体。请设计合理方案用茴香醛 合成D(其他原料自选,用反应流程图表示,并注明必要的反应条件)。
合成D(其他原料自选,用反应流程图表示,并注明必要的反应条件)。 例如:

您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】Ⅺ是某药物的中间体,以顺丁烯二酸为原料制备Ⅺ的流程如下:

已知:①Ⅱ和Ⅲ生成Ⅳ的反应中原子利用率为100%。
②图中,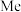 代表甲基,
代表甲基,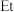 代表乙基。
代表乙基。
请回答下列问题:
(1)Ⅲ的名称是___________ ,Ⅸ中所含官能团的名称为___________ 。
(2)Ⅹ→Ⅺ的反应类型是___________ 。
(3) Ⅷ在碱作用下生成
Ⅷ在碱作用下生成 Ⅸ和
Ⅸ和 Ⅻ,则Ⅻ的核磁共振氢谱图中峰的面积之比为
Ⅻ,则Ⅻ的核磁共振氢谱图中峰的面积之比为___________ 。
(4)已知 在较高温度或浓度过大时会发生分解甚至爆炸,则Ⅹ→Ⅺ过程中必须采取的反应条件和操作是
在较高温度或浓度过大时会发生分解甚至爆炸,则Ⅹ→Ⅺ过程中必须采取的反应条件和操作是___________ 。
(5)已知Ⅷ→Ⅸ、Ⅸ→Ⅹ、Ⅹ→Ⅺ的产率依次为56%、68%、75%,则Ⅷ→Ⅺ的产率为___________ 。
(6)在Ⅳ的同分异构体中,同时具备下列条件的结构有___________ 种。
①遇 溶液发生显色反应;②能发生银镜反应和水解反应。
溶液发生显色反应;②能发生银镜反应和水解反应。
任选其中一种苯环上含3个取代基的同分异构体与足量的热烧碱溶液反应的化学方程式为___________ 。

已知:①Ⅱ和Ⅲ生成Ⅳ的反应中原子利用率为100%。
②图中,
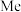 代表甲基,
代表甲基,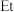 代表乙基。
代表乙基。请回答下列问题:
(1)Ⅲ的名称是
(2)Ⅹ→Ⅺ的反应类型是
(3)
 Ⅷ在碱作用下生成
Ⅷ在碱作用下生成 Ⅸ和
Ⅸ和 Ⅻ,则Ⅻ的核磁共振氢谱图中峰的面积之比为
Ⅻ,则Ⅻ的核磁共振氢谱图中峰的面积之比为(4)已知
 在较高温度或浓度过大时会发生分解甚至爆炸,则Ⅹ→Ⅺ过程中必须采取的反应条件和操作是
在较高温度或浓度过大时会发生分解甚至爆炸,则Ⅹ→Ⅺ过程中必须采取的反应条件和操作是(5)已知Ⅷ→Ⅸ、Ⅸ→Ⅹ、Ⅹ→Ⅺ的产率依次为56%、68%、75%,则Ⅷ→Ⅺ的产率为
(6)在Ⅳ的同分异构体中,同时具备下列条件的结构有
①遇
 溶液发生显色反应;②能发生银镜反应和水解反应。
溶液发生显色反应;②能发生银镜反应和水解反应。任选其中一种苯环上含3个取代基的同分异构体与足量的热烧碱溶液反应的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
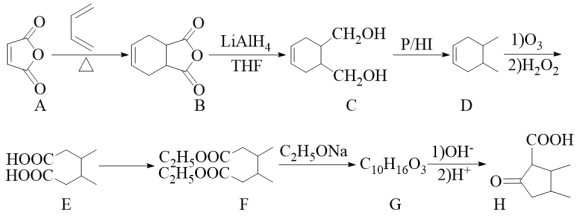
【推荐3】化合物H是有机合成重要的中间体,其合成路线如图:
已知: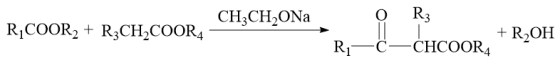
(1)H中官能团的名称为___________ 。
(2)B与H的相对分子质量接近,H的沸点高于B的原因为___________ 。
(3)E→F所需的条件为___________ 。
(4)化合物G的结构简式为___________ 。
(5)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___________ 。
①能与FeCl3溶液发生显色反应:
②碱性水解后酸化,所得两种有机产物分子均只有2种不同化学环境的氢原子。

已知:
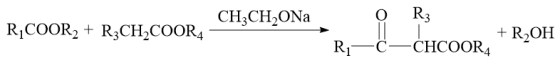
(1)H中官能团的名称为
(2)B与H的相对分子质量接近,H的沸点高于B的原因为
(3)E→F所需的条件为
(4)化合物G的结构简式为
(5)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:
①能与FeCl3溶液发生显色反应:
②碱性水解后酸化,所得两种有机产物分子均只有2种不同化学环境的氢原子。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室制备溴乙烷(C2H5Br)的装置和步骤如下:(已知溴乙烷的沸点38.4℃)①检查装置的气密性,向装置图所示的∪形管和大烧杯中加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小心加热,使其充分反应.回答下列问题:
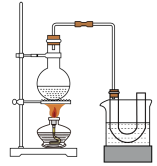
(1)该实验制取溴乙烷的化学方程式为:__ .
(2)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为__ ,同时生成的无色气体分子式为__ .
(3)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是__ .
(4)U形管内可观察到的现象是__ .
(5)反应结束后,∪形管中粗制的C2H5Br呈棕黄色.为了除去粗产品中的杂质,可选择下列试剂中的__ (填序号).
(a)NaOH溶液 (b)H2O (c)Na2SO3溶液(d)CCl4
所需的主要玻璃仪器是__ (填仪器名称).要进一步制得纯净的C2H5Br,可用水洗,然后加入无水CaCl2,再进行__ (填操作名称).
(6)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后__ (填代号).
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却.

(1)该实验制取溴乙烷的化学方程式为:
(2)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为
(3)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是
(4)U形管内可观察到的现象是
(5)反应结束后,∪形管中粗制的C2H5Br呈棕黄色.为了除去粗产品中的杂质,可选择下列试剂中的
(a)NaOH溶液 (b)H2O (c)Na2SO3溶液(d)CCl4
所需的主要玻璃仪器是
(6)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硼氢化钠(NaBH4)通常为白色粉末,容易吸水潮解,可溶于异丙胺(熔点:-101℃,沸点:33℃),在有机合成中被称为“万能还原剂”。制备硼氢化钠的流程如图:

硼酸三甲酯B(OCH3)3的制备:将硼酸(H3BO3)和适量甲醇加入圆底烧瓶中,然后缓慢地加入浓硫酸,振荡,在烧瓶上加装分馏柱a,用电炉经水浴锅加热,回流2小时,收集硼酸三甲酯与甲醇共沸液。装置如图所示(夹持装置略去,下同)。

相关信息见表:
请回答下列问题:
(1)冷却水应从直形冷凝管_____________ (填“b”或“c”)口出。
(2)本实验采用水浴加热,优点是___________ ,仪器d的名称是_________ ,仪器d中应该盛装的试剂是______ (填序号),所盛试剂的作用是_______________ 。
a.浓H2SO4b.无水硫酸铜c.五氧化二磷
(3)圆底烧瓶中发生的主要反应的化学方程式是_________________ 。
(4)在240℃条件下硼酸三甲酯与氢化钠反应制取NaBH4,同时生成CH3ONa。萃取NaBH4时可采用索氏提取法,其装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现连续萃取。当萃取完全后,硼氢化钠在________ (填“圆底烧瓶”或“索氏提取器”)中。

(5)与常规的萃取相比,采用索氏提取法的优点是__________ 。
(6)“有效氢含量”可用来衡量含氢还原剂的还原能力。1mol NaBH4的还原能力相当于______ 克H2的还原能力。

硼酸三甲酯B(OCH3)3的制备:将硼酸(H3BO3)和适量甲醇加入圆底烧瓶中,然后缓慢地加入浓硫酸,振荡,在烧瓶上加装分馏柱a,用电炉经水浴锅加热,回流2小时,收集硼酸三甲酯与甲醇共沸液。装置如图所示(夹持装置略去,下同)。

相关信息见表:
| 硼酸三甲酯B(OCH3)3 | 甲醇 | 甲醇钠 | |
| 溶解性 | 与乙醇、甲醇混溶,能水解 | 与水混溶 | 溶于甲醇,不溶于异丙胺 |
| 沸点/℃ | 68 | 64 | 450 |
| 硼酸三甲酯与甲醇混合物的共沸点为54℃ | |||
(1)冷却水应从直形冷凝管
(2)本实验采用水浴加热,优点是
a.浓H2SO4b.无水硫酸铜c.五氧化二磷
(3)圆底烧瓶中发生的主要反应的化学方程式是
(4)在240℃条件下硼酸三甲酯与氢化钠反应制取NaBH4,同时生成CH3ONa。萃取NaBH4时可采用索氏提取法,其装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现连续萃取。当萃取完全后,硼氢化钠在

(5)与常规的萃取相比,采用索氏提取法的优点是
(6)“有效氢含量”可用来衡量含氢还原剂的还原能力。1mol NaBH4的还原能力相当于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】苯甲醛(微溶于水、易溶于有机溶剂,密度约等于水的密度)在碱性条件下发生歧化反应可以制备苯甲酸和苯甲醇(在水中溶解度不大,易溶于有机溶剂,密度约等于水的密度)。反应原理如下:
2C6H5CHO+NaOH→C6H5CH2OH+C6H5COONa
C6H5COONa+HCl→C6H5COOH+NaCl
相关物质物理性质如表:
实验流程如下:

(1)操作①需连续加热1小时(如图1),其中加热固定装置未画出。

仪器A的名称为___ ,若将仪器B改为图2中的仪器C,效果不如B,请说明原因___ 。
(2)操作②有关分液漏斗的使用不正确的是___ (填字母)。
A.分液漏斗在使用之前必须检查是否漏水
B.分液漏斗内的液体不能过多,否则不利于振荡
C.充分振荡后将分液漏斗置于铁架台上静置,分层后立即打开旋塞进行分液
D.分液时待下层液体放完后立即关闭旋塞,换一个烧杯再打开旋塞使上层液体流下
(3)操作③是用沸水浴加热蒸馏,再进行操作④(如图2),收集___ ℃的馏分。图2中有一处明显错误,正确的应改为___ 。
(4)抽滤时(如图3)烧杯中苯甲酸晶体转入布氏漏斗时,杯壁上还粘有少量晶体;用___ 冲洗杯壁上残留的晶体。抽滤完成后用少量冰水对晶体进行洗涤,洗涤前应先___ 。
(5)用电子天平准确称取0.2440g苯甲酸于锥形瓶中加100mL蒸馏水溶解(必要时可以加热),再用0.1000mol·L-1的标准氢氧化钠溶液滴定,共消耗标准氢氧化钠溶液19.20mL,苯甲酸的纯度为___ %。
2C6H5CHO+NaOH→C6H5CH2OH+C6H5COONa
C6H5COONa+HCl→C6H5COOH+NaCl
相关物质物理性质如表:
| 苯甲醛 | 苯甲醇 | 苯甲酸. | 苯 | |
| 沸点/℃ | 178 | 205 | 249 | 80 |
| 熔点/℃ | 26 | -15 | 122 | 5.5 |
| 苯甲酸在水中的溶解 | ||
| 17℃ | 25℃ | 100℃ |
| 0.21g | 0.34g | 5.9g |

(1)操作①需连续加热1小时(如图1),其中加热固定装置未画出。

仪器A的名称为
(2)操作②有关分液漏斗的使用不正确的是
A.分液漏斗在使用之前必须检查是否漏水
B.分液漏斗内的液体不能过多,否则不利于振荡
C.充分振荡后将分液漏斗置于铁架台上静置,分层后立即打开旋塞进行分液
D.分液时待下层液体放完后立即关闭旋塞,换一个烧杯再打开旋塞使上层液体流下
(3)操作③是用沸水浴加热蒸馏,再进行操作④(如图2),收集
(4)抽滤时(如图3)烧杯中苯甲酸晶体转入布氏漏斗时,杯壁上还粘有少量晶体;用
(5)用电子天平准确称取0.2440g苯甲酸于锥形瓶中加100mL蒸馏水溶解(必要时可以加热),再用0.1000mol·L-1的标准氢氧化钠溶液滴定,共消耗标准氢氧化钠溶液19.20mL,苯甲酸的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
氯化铁:熔点为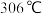 ,沸点为
,沸点为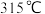 ;易吸收空气中的水分而潮解。工业上采用向
;易吸收空气中的水分而潮解。工业上采用向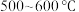 的铁粉中通入氯气来生产无水氯化铁。
的铁粉中通入氯气来生产无水氯化铁。
氯化亚铁:熔点为 ,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用如图所示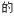 装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:
装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:

(1)在装置A中,用MnO2与浓盐酸反应制取氯气(加热装置略去),写出反应的化学方程式___________ ,当生成35.5g氯气,做还原剂的HCl的物质的量为___________ mol。
(2)C放置在盛冷水的水槽中,水浴的作用是___________ 。
(3)仪器D的名称是___________ ,D中装的药品可以是___________ (填序号)
A. B.碱石灰 C.
B.碱石灰 C. D.
D.
(4)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。若产物中混有 ,可用下列试剂中的___________进行检测。(填序号,试剂不组合使用)
,可用下列试剂中的___________进行检测。(填序号,试剂不组合使用)
氯化铁:熔点为
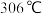 ,沸点为
,沸点为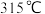 ;易吸收空气中的水分而潮解。工业上采用向
;易吸收空气中的水分而潮解。工业上采用向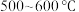 的铁粉中通入氯气来生产无水氯化铁。
的铁粉中通入氯气来生产无水氯化铁。氯化亚铁:熔点为
 ,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。某化学活动小组用如图所示
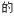 装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:
装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:
(1)在装置A中,用MnO2与浓盐酸反应制取氯气(加热装置略去),写出反应的化学方程式
(2)C放置在盛冷水的水槽中,水浴的作用是
(3)仪器D的名称是
A.
 B.碱石灰 C.
B.碱石灰 C. D.
D.
(4)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。若产物中混有
 ,可用下列试剂中的___________进行检测。(填序号,试剂不组合使用)
,可用下列试剂中的___________进行检测。(填序号,试剂不组合使用)A. 溶液 溶液 | B.酸性 溶液 溶液 | C. 溶液 溶液 | D.KI-淀粉溶液 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】二氧化氯(ClO2)可用于自来水消毒。以粗盐为原料生产C1O2的工艺主要包括:①粗盐精制;②电解微酸性NaCl溶液;③C1O2的制取。工艺流程如图:

提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液
(1)粗食盐水中含有Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的试剂X,选出试剂X所代表的试剂,按滴加顺序依次为是__ (填化学式)。
(2)上述过程中,将食盐水在特定条件下电解得到的氯酸钠与盐酸反应生成C1O2。电解时生成的气体B是___ :电解时阳极反应式为__ 。反应Ⅲ的化学方程式为___ 。
(3)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了以下实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知ClO2+I-+H+ I2+Cl-+H2O未配平)
步骤3:以淀粉溶液作指示剂,用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。(已知:I2+2S2O32-=2I-+S4O62-)
①准确量取10.00mLClO2溶液的玻璃仪器是__ 。
②上述步骤3中滴定终点的现象是___ 。
③若实验中使用的Na2S2O3标准溶液部分因被氧气氧化而变质,则实验结果__ (填“偏高”、“偏低”或“无影响”)
④根据上述步骤可计算出原C1O2溶液的浓度为__ mol·L-1(用含字母的代数式表示)。

提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液
(1)粗食盐水中含有Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的试剂X,选出试剂X所代表的试剂,按滴加顺序依次为是
(2)上述过程中,将食盐水在特定条件下电解得到的氯酸钠与盐酸反应生成C1O2。电解时生成的气体B是
(3)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了以下实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知ClO2+I-+H+ I2+Cl-+H2O未配平)
步骤3:以淀粉溶液作指示剂,用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。(已知:I2+2S2O32-=2I-+S4O62-)
①准确量取10.00mLClO2溶液的玻璃仪器是
②上述步骤3中滴定终点的现象是
③若实验中使用的Na2S2O3标准溶液部分因被氧气氧化而变质,则实验结果
④根据上述步骤可计算出原C1O2溶液的浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硫脲 是一种溶于水的白色晶体,是一种重要的化工原料。实验室模拟化工生产,在45℃、pH大约为10的条件下,利用氰胺(
是一种溶于水的白色晶体,是一种重要的化工原料。实验室模拟化工生产,在45℃、pH大约为10的条件下,利用氰胺( )与
)与 溶液反应制备硫脲,实验装置如图所示:
溶液反应制备硫脲,实验装置如图所示:
(1)写出装置A中离子反应方程式_______ 。
(2)装置B中长玻璃管的作用是_______ ,X试剂为_______ 。
(3)写出装置C中生成 的化学反应方程式
的化学反应方程式_______ 。
(4)实验过程中要以一定的气流速率通入 ,其目的是
,其目的是_______ 。
(5)常采用碘氧化法测定硫脲的纯度。实验操作如下:
Ⅰ.称取mg硫脲晶体样品,配制成溶液,加入 足量的
足量的 溶液。
溶液。
Ⅱ.用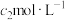 的
的 标准溶液滴定未反应的
标准溶液滴定未反应的 。
。
Ⅲ.当溶液显淡黄色时滴加淀粉指示剂,滴定至终点时共消耗 标准溶液,已知杂质不参与反应。(已知:
标准溶液,已知杂质不参与反应。(已知: ,
, ,
, )
)
①滴定至终点的现象是_______ 。
② 的纯度为
的纯度为_______ (写出计算式即可),若盛放 标准溶液的滴定管没有润洗,则最终结果会
标准溶液的滴定管没有润洗,则最终结果会_______ (填“偏大”“偏小”或“无影响”)。
 是一种溶于水的白色晶体,是一种重要的化工原料。实验室模拟化工生产,在45℃、pH大约为10的条件下,利用氰胺(
是一种溶于水的白色晶体,是一种重要的化工原料。实验室模拟化工生产,在45℃、pH大约为10的条件下,利用氰胺( )与
)与 溶液反应制备硫脲,实验装置如图所示:
溶液反应制备硫脲,实验装置如图所示:
(1)写出装置A中离子反应方程式
(2)装置B中长玻璃管的作用是
(3)写出装置C中生成
 的化学反应方程式
的化学反应方程式(4)实验过程中要以一定的气流速率通入
 ,其目的是
,其目的是(5)常采用碘氧化法测定硫脲的纯度。实验操作如下:
Ⅰ.称取mg硫脲晶体样品,配制成溶液,加入
 足量的
足量的 溶液。
溶液。Ⅱ.用
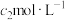 的
的 标准溶液滴定未反应的
标准溶液滴定未反应的 。
。Ⅲ.当溶液显淡黄色时滴加淀粉指示剂,滴定至终点时共消耗
 标准溶液,已知杂质不参与反应。(已知:
标准溶液,已知杂质不参与反应。(已知: ,
, ,
, )
)①滴定至终点的现象是
②
 的纯度为
的纯度为 标准溶液的滴定管没有润洗,则最终结果会
标准溶液的滴定管没有润洗,则最终结果会
您最近一年使用:0次



