二氧化硫对环境有一定的负面影响,对SO2的处理和利用是科学研究的重要课题之一。
I.用石灰石、氨水等脱硫。以硫酸工业的二氧化硫尾气、氨水、石灰石、碳酸氢铵和氯化钾等为原料,可以制备有重要应用价值的硫酸钾、亚硫酸铵等物质,制备流程如下:
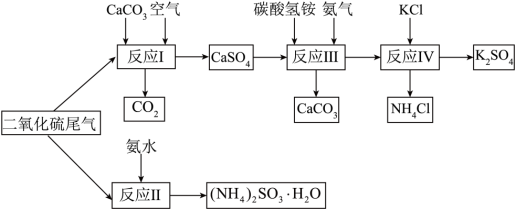
(1)①反应I是脱去SO2的一种常用方法,其总反应的化学方程式为_______ 。
②研究发现,pH和温度对石灰石浆液的脱硫效率有一定影响。当烟气通入速度一定时,石灰石浆液的脱硫率与浆液pH的关系如图所示(pH=-lgc(H+))。
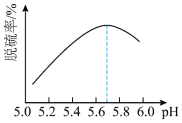
下列有关说法正确的是_______ 。
a.烟气通入石灰石浆液时的温度越高,吸收越快,吸收率越高
b.反应时需鼓入足量的空气以保证SO2被充分氧化生成CaSO4
c.将脱硫后的气体通入KMnO4溶液,可粗略判断烟气脱硫效率
d.石灰石浆液pH>5.7烟气脱硫效果降低,是因为石灰石的溶解程度增大
(2)生产中,需要向反应Ⅱ的溶液中加入适量强还原剂,其目的是_______ 。
(3)反应Ⅲ所得的滤液中所含阳离子的电子式为_______ ,检验该滤液中所含阴离子的方法是_______ 。
(4)(NH4)2SO3可用于电厂等烟道气中脱氮。将氮氧化物转化为氮气,同时生成一种氨肥。写出用(NH4)2SO3溶液吸收NO的离子方程式_______ 。
Ⅱ.H2还原法也是处理硫酸厂废气的方法之一。400℃时,将H2和含SO2的尾气按一定比例混合,以一定流速通过装有Fe2O3/Al2O3的负载型催化剂(Fe2O3为催化剂,Al2O3为载体),发生反应。
(5)该反应生成S单质和水,其中氧化剂和还原剂的物质的量之比为_______ 。
(6)研究表明,该反应过程中实际起催化作用的是反应初期生成的FeS2,催化硫化过程中还检测到H2S气体。整个FeS2催化硫化的过程可分为三步,写出第三步的化学方程式:
①H2+FeS2=FeS+H2S;
②2H2S+SO2=3S↓+2H2O;
③_______ 。
I.用石灰石、氨水等脱硫。以硫酸工业的二氧化硫尾气、氨水、石灰石、碳酸氢铵和氯化钾等为原料,可以制备有重要应用价值的硫酸钾、亚硫酸铵等物质,制备流程如下:

(1)①反应I是脱去SO2的一种常用方法,其总反应的化学方程式为
②研究发现,pH和温度对石灰石浆液的脱硫效率有一定影响。当烟气通入速度一定时,石灰石浆液的脱硫率与浆液pH的关系如图所示(pH=-lgc(H+))。

下列有关说法正确的是
a.烟气通入石灰石浆液时的温度越高,吸收越快,吸收率越高
b.反应时需鼓入足量的空气以保证SO2被充分氧化生成CaSO4
c.将脱硫后的气体通入KMnO4溶液,可粗略判断烟气脱硫效率
d.石灰石浆液pH>5.7烟气脱硫效果降低,是因为石灰石的溶解程度增大
(2)生产中,需要向反应Ⅱ的溶液中加入适量强还原剂,其目的是
(3)反应Ⅲ所得的滤液中所含阳离子的电子式为
(4)(NH4)2SO3可用于电厂等烟道气中脱氮。将氮氧化物转化为氮气,同时生成一种氨肥。写出用(NH4)2SO3溶液吸收NO的离子方程式
Ⅱ.H2还原法也是处理硫酸厂废气的方法之一。400℃时,将H2和含SO2的尾气按一定比例混合,以一定流速通过装有Fe2O3/Al2O3的负载型催化剂(Fe2O3为催化剂,Al2O3为载体),发生反应。
(5)该反应生成S单质和水,其中氧化剂和还原剂的物质的量之比为
(6)研究表明,该反应过程中实际起催化作用的是反应初期生成的FeS2,催化硫化过程中还检测到H2S气体。整个FeS2催化硫化的过程可分为三步,写出第三步的化学方程式:
①H2+FeS2=FeS+H2S;
②2H2S+SO2=3S↓+2H2O;
③
更新时间:2023-06-15 14:38:53
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】Ⅰ.地球上的金属矿物资源是有限的,应合理开发利用。
(1)金属冶炼的实质是金属离子被______ (填“氧化”或“还原”)生成金属单质。
(2)铜在自然界存在于多种矿石中,如:
请回答下列问题:
①上表所列铜化合物中,推断铜的质量百分含量最高的是______ 。
② 其中Cu为+2价、Fe为+2价,高温焙烧时发生的反应是
其中Cu为+2价、Fe为+2价,高温焙烧时发生的反应是 ,焙烧过程中被还原的元素有
,焙烧过程中被还原的元素有______ 。
③工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:,该反
应中氧化剂是______ 。
④ 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为__________________ 。
Ⅱ.某校化学兴趣小组通过查阅资料得知用海水获取氯化钠和金属镁的实验流程如图所示,请你根据题意回答下列问题。
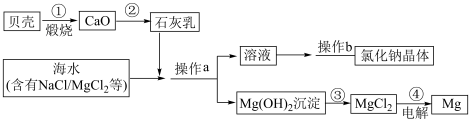
(3)①②③④四个反应中属于复分解反应的是____________ 。
(1)金属冶炼的实质是金属离子被
(2)铜在自然界存在于多种矿石中,如:
| 矿石名称 | 黄铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 |  |  |  |
①上表所列铜化合物中,推断铜的质量百分含量最高的是
②
 其中Cu为+2价、Fe为+2价,高温焙烧时发生的反应是
其中Cu为+2价、Fe为+2价,高温焙烧时发生的反应是 ,焙烧过程中被还原的元素有
,焙烧过程中被还原的元素有③工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:,该反

应中氧化剂是
④
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为Ⅱ.某校化学兴趣小组通过查阅资料得知用海水获取氯化钠和金属镁的实验流程如图所示,请你根据题意回答下列问题。

(3)①②③④四个反应中属于复分解反应的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】工业上以浓缩海水(含较高浓度的 )为原料提取溴的部分流程如图所示:
)为原料提取溴的部分流程如图所示:

已知: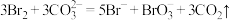 。
。
(1)反应用的 可由下图所示装置制取,制取
可由下图所示装置制取,制取 的化学方程式为
的化学方程式为___________ ,为除去 中挥发出的HCl,装置E中所盛溶液是
中挥发出的HCl,装置E中所盛溶液是___________ 。

(2)实验室用下图所示装置模拟流程中的部分过程。
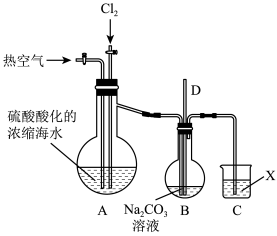
①写出通入 时发生反应的离子方程式
时发生反应的离子方程式________ 。
②通入热空气的作用是________ 。
③烧瓶B中的长导管D起着平衡压强的作用,当烧瓶内气体压强过大时,可以观察到的现象是___________ 。
(3)“反应釜2”中所发生的反应是氧化还原反应,其中的氧化剂是___________ 。
(4)蒸馏后,蒸馏塔溶液中仍溶有少量Br,可以向其中加入少量___________ 萃取其中的 。
。
 )为原料提取溴的部分流程如图所示:
)为原料提取溴的部分流程如图所示:
已知:
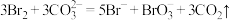 。
。(1)反应用的
 可由下图所示装置制取,制取
可由下图所示装置制取,制取 的化学方程式为
的化学方程式为 中挥发出的HCl,装置E中所盛溶液是
中挥发出的HCl,装置E中所盛溶液是
(2)实验室用下图所示装置模拟流程中的部分过程。

①写出通入
 时发生反应的离子方程式
时发生反应的离子方程式②通入热空气的作用是
③烧瓶B中的长导管D起着平衡压强的作用,当烧瓶内气体压强过大时,可以观察到的现象是
(3)“反应釜2”中所发生的反应是氧化还原反应,其中的氧化剂是
(4)蒸馏后,蒸馏塔溶液中仍溶有少量Br,可以向其中加入少量
 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊 法制备亚氯酸钠的流程如图:
法制备亚氯酸钠的流程如图: ,该反应的还原产物是
,该反应的还原产物是___________ (写化学式)。
(2)在□补充反应②另一种产物,并配平此离子方程式,然后用单线桥法分析此化学反应。___________
________ClO2+ ________H2O2+ ________OH-=________ +________H2O+ _______□
+________H2O+ _______□
(3)NaClO2中Cl的化合价为___________ ,H2O2在反应②中___________ (填字母)。
A.只能作氧化剂 B.只能作还原剂 C.既能作氧化剂也能作还原剂
(4)实验室采用马蒂逊 法制备NaClO2的实验装置如图甲所示:
法制备NaClO2的实验装置如图甲所示:
②当温度低于38℃时,NaClO2饱和溶液中析出的晶体是NaClO2∙3H2O;当温度在 38~60℃时,析出NaClO2;温度高于 60℃时,NaClO2分解。
C中将装置浸入冰水浴中的目的是___________ 。
 法制备亚氯酸钠的流程如图:
法制备亚氯酸钠的流程如图: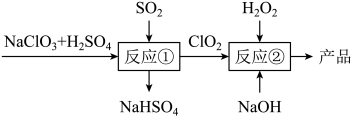
 ,该反应的还原产物是
,该反应的还原产物是(2)在□补充反应②另一种产物,并配平此离子方程式,然后用单线桥法分析此化学反应。
________ClO2+ ________H2O2+ ________OH-=________
 +________H2O+ _______□
+________H2O+ _______□(3)NaClO2中Cl的化合价为
A.只能作氧化剂 B.只能作还原剂 C.既能作氧化剂也能作还原剂
(4)实验室采用马蒂逊
 法制备NaClO2的实验装置如图甲所示:
法制备NaClO2的实验装置如图甲所示:
②当温度低于38℃时,NaClO2饱和溶液中析出的晶体是NaClO2∙3H2O;当温度在 38~60℃时,析出NaClO2;温度高于 60℃时,NaClO2分解。
C中将装置浸入冰水浴中的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学小组为了证明二氧化硫和氯水的漂白性,设计了如图所示的实验装置:
(1)用来制取氯气的装置是_____ (填字母序号),反应中浓盐酸所表现出的化学性质是_____ 和_____ 。
(2)反应开始一段时间后,B、D试管中的品红溶液均褪色,停止通气后,再将B、D两个试管分别加热,_____ (填“B”或“D”)试管中无明显现象。
(3)装置C的主要作用是_____ 。
(4)该小组同学将两种气体混合后通入品红溶液中,发现漂白效果并不像预期的一样增强。查阅资料得知:两种气体混合,再与水反应可生成两种常见的酸,因而漂白作用减弱,该反应的离子方程式是_____ 。

(1)用来制取氯气的装置是
(2)反应开始一段时间后,B、D试管中的品红溶液均褪色,停止通气后,再将B、D两个试管分别加热,
(3)装置C的主要作用是
(4)该小组同学将两种气体混合后通入品红溶液中,发现漂白效果并不像预期的一样增强。查阅资料得知:两种气体混合,再与水反应可生成两种常见的酸,因而漂白作用减弱,该反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外活动小组的同学在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证哪位同学的判断正确,丙同学设计了图中的实验装置(锌与浓硫酸共热时产生的气体为X,且该反应装置略去)。
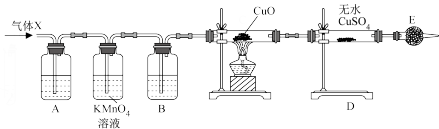
试回答下列问题:
(1)上述反应中生成二氧化硫的化学方程式为_____ 。
(2)乙同学认为还可能产生氢气的理由是____ 。
(3)丙同学在安装好装置后,必须首先进行的一步操作是_____ 。
(4)A中加入的试剂可能是____ ,作用是____ 。
(5)可以证明气体X中含有氢气的实验现象是C中:____ ;D中:____ 。如果去掉装置B,则“不能”根据D中的现象判断气体X中有氢气,原因是_____ 。

试回答下列问题:
(1)上述反应中生成二氧化硫的化学方程式为
(2)乙同学认为还可能产生氢气的理由是
(3)丙同学在安装好装置后,必须首先进行的一步操作是
(4)A中加入的试剂可能是
(5)可以证明气体X中含有氢气的实验现象是C中:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某研究性学习小组在研究二氧化硫漂白作用时,从“氯气的漂白作用实际上是氯气与水反应生成的次氯酸的漂白作用”得到启发。为了探究二氧化硫的漂白作用到底是二氧化硫本身还是二氧化硫与水作用的产物,该小组设计了如下实验。请回答相关问题。
(1)实验室用亚硫酸钠粉末跟硫酸制取二氧化硫,现有下列三种硫酸溶液,应选用________ (填字母)
A.98%浓硫酸 B.70%硫酸 C.10%稀硫酸

(2)为了探究SO2能否使品红褪色,该同学选择了正确的药品后设计了如下图所示实验装置,请指出实验装置设计中的不合理之处。
①________________________________________________________________________ ;
②________________________________________________________________________ 。
(3)该同学选择了正确装置后,实验中控制二氧化硫以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色。为此,你认为使品红的水溶液褪色的微粒可能是________ 。
(4)该同学进一步实验如下:取等量相同浓度的品红水溶液于两支试管中,再分别加入少量亚硫酸钠固体和亚硫酸氢钠固体,两支试管中的品红都褪色,他得出的结论:使品红褪色的微粒肯定是HSO3-或SO32-。你认为他的结论是否正确________ ,其理由是______________ 。
(1)实验室用亚硫酸钠粉末跟硫酸制取二氧化硫,现有下列三种硫酸溶液,应选用
A.98%浓硫酸 B.70%硫酸 C.10%稀硫酸

(2)为了探究SO2能否使品红褪色,该同学选择了正确的药品后设计了如下图所示实验装置,请指出实验装置设计中的不合理之处。
①
②
(3)该同学选择了正确装置后,实验中控制二氧化硫以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色。为此,你认为使品红的水溶液褪色的微粒可能是
(4)该同学进一步实验如下:取等量相同浓度的品红水溶液于两支试管中,再分别加入少量亚硫酸钠固体和亚硫酸氢钠固体,两支试管中的品红都褪色,他得出的结论:使品红褪色的微粒肯定是HSO3-或SO32-。你认为他的结论是否正确
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】海洋是资源的宝库,以海水为原料可以制取粗盐、Br2、镁等多种物质。
I.粗盐中主要含NaCl,还含有少量泥沙、CaCl2、MgCl2和Na2SO4。
(1)将粗盐提纯的方法是:将粗盐溶于水,向里面依次加入稍过量的_______ (填字母),过滤,将滤液用盐酸酸化后,蒸发结晶。
A.Na2CO3 B.NaOH C.BaCl2
(2)实验中,判断所加BaCl2溶液已经过量的方法是_______ 。
II.浓缩海水中含有NaCl、NaBr等物质。从浓缩海水中提取溴的流程如下:_______ 。
(4)“吸收”时是用SO2水溶液吸收空气吹出的溴蒸汽。写出“吸收”时发生反应的化学方程式,并用双线桥标出电子转移的方向和数目:_______ 。
III.从海水中提取镁流程如下:
②MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
(5)操作②是_______ 、过滤。
(6)工业上是将氢氧化镁转变为氯化镁,再电解氯化镁来制取镁单质,而不采用加热Mg(OH)2得到MgO,再电解熔融MgO的方法制取金属镁,其原因是_______ 。
I.粗盐中主要含NaCl,还含有少量泥沙、CaCl2、MgCl2和Na2SO4。
(1)将粗盐提纯的方法是:将粗盐溶于水,向里面依次加入稍过量的
A.Na2CO3 B.NaOH C.BaCl2
(2)实验中,判断所加BaCl2溶液已经过量的方法是
II.浓缩海水中含有NaCl、NaBr等物质。从浓缩海水中提取溴的流程如下:

(4)“吸收”时是用SO2水溶液吸收空气吹出的溴蒸汽。写出“吸收”时发生反应的化学方程式,并用双线桥标出电子转移的方向和数目:
III.从海水中提取镁流程如下:
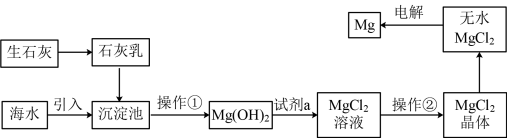
②MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
(5)操作②是
(6)工业上是将氢氧化镁转变为氯化镁,再电解氯化镁来制取镁单质,而不采用加热Mg(OH)2得到MgO,再电解熔融MgO的方法制取金属镁,其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】草木灰中含有可溶性钾盐(主要成分是 ,含有少量的
,含有少量的 、
、 )。某同学设计实验拟提取草木灰中的钾盐。
)。某同学设计实验拟提取草木灰中的钾盐。
(1)实验步骤:Ⅰ.取适量的草木灰,加水搅拌、溶解,过滤,_______ (填写操作名称),得到白色固体。
(2)为检验草木灰中的离子,某实验小组设计了四组实验,其装置如图所示:

①实验一:往试管中加入少量草木灰,加水溶解,再加入足量稀硝酸,烧杯中加入澄清石灰水。说明草木灰中含有 的实验现象是
的实验现象是_______ 。
②实验二:取少量实验一中的溶液,再加入足量 溶液,有白色沉淀生成。说明草木灰中含有的离子是
溶液,有白色沉淀生成。说明草木灰中含有的离子是_______ 。
③实验三:取少量实验二的溶液,滴加硝酸银溶液,有白色沉淀生成。
根据实验现象,该小组甲同学得出结论:草木灰中含有 ,但小组中乙同学认为不能得出结论,你认为乙同学的理由是
,但小组中乙同学认为不能得出结论,你认为乙同学的理由是_______ 。
④实验四:用洁净的铂丝蘸取草木灰固体,进行如图所示实验,预计观察到的实验现象为_______ ,证明含有的离子是_______ 。
(3)通过如图所示流程,由草木灰制取硝酸钾:
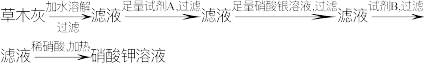
试剂A是_______ ,试剂B是_______ ,加入硝酸反应的离子方程式是_______ 。
 ,含有少量的
,含有少量的 、
、 )。某同学设计实验拟提取草木灰中的钾盐。
)。某同学设计实验拟提取草木灰中的钾盐。(1)实验步骤:Ⅰ.取适量的草木灰,加水搅拌、溶解,过滤,
(2)为检验草木灰中的离子,某实验小组设计了四组实验,其装置如图所示:

①实验一:往试管中加入少量草木灰,加水溶解,再加入足量稀硝酸,烧杯中加入澄清石灰水。说明草木灰中含有
 的实验现象是
的实验现象是②实验二:取少量实验一中的溶液,再加入足量
 溶液,有白色沉淀生成。说明草木灰中含有的离子是
溶液,有白色沉淀生成。说明草木灰中含有的离子是③实验三:取少量实验二的溶液,滴加硝酸银溶液,有白色沉淀生成。
根据实验现象,该小组甲同学得出结论:草木灰中含有
 ,但小组中乙同学认为不能得出结论,你认为乙同学的理由是
,但小组中乙同学认为不能得出结论,你认为乙同学的理由是④实验四:用洁净的铂丝蘸取草木灰固体,进行如图所示实验,预计观察到的实验现象为
(3)通过如图所示流程,由草木灰制取硝酸钾:
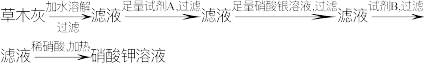
试剂A是
您最近一年使用:0次
【推荐3】资源高效利用是化学生产中一直追求的目标,下图是电解精炼铜的阳极泥综合利用提取金和制备AgCl、PbSO4的工艺,其中阳极泥含铜、银、金、铅等单质。
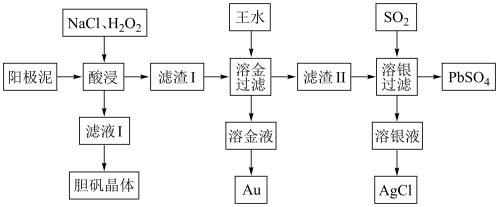
(1)“酸浸”过程中应加入的酸为___________ ,此环节对温度的控制有很高的要求,应采用___________ (填写加热方式),写出酸浸时铜元素参与反应的离子方程式___________ 。
(2)“滤渣Ⅰ”的成分除了Au、Ag、AgCl外,还有___________ 。在这些滤渣中加入王水可将Au转化成H[AuCl4],实验室将王水换成盐酸和氯酸钠的混合溶液也可将金单质转化成相同的物质,请写出混合溶液溶金的化学方程式___________ 。
(3)向“溶银液”中加入硫酸,经过滤、洗涤干燥即可得到AgCl,检验是否洗涤干净的操作方法为___________ 。
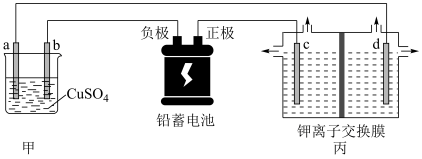
(4)硫酸铅可用于制造蓄电池,下图是研究小组应用铅蓄电池模拟工业生产的电化学装置,a、b、c、d四电极均为惰性电极,甲装置电解质溶液为CuSO4溶液,丙装置电解质溶液为KCl溶液,忽略气体溶解,当电路中转移0.4mol电子时,丙装置阳极室溶液质量减少___________ g,向甲所得溶液中加入Cu2(OH)2CO3后能后能使溶液复原,则b电极的电极反应式为___________ 。

(1)“酸浸”过程中应加入的酸为
(2)“滤渣Ⅰ”的成分除了Au、Ag、AgCl外,还有
(3)向“溶银液”中加入硫酸,经过滤、洗涤干燥即可得到AgCl,检验是否洗涤干净的操作方法为
(4)硫酸铅可用于制造蓄电池,下图是研究小组应用铅蓄电池模拟工业生产的电化学装置,a、b、c、d四电极均为惰性电极,甲装置电解质溶液为CuSO4溶液,丙装置电解质溶液为KCl溶液,忽略气体溶解,当电路中转移0.4mol电子时,丙装置阳极室溶液质量减少

您最近一年使用:0次



