W、X、Y、Z、N、M六种主族元素,它们在周期表中位置如图所示,请用对应的的化学用语回答下列问题:
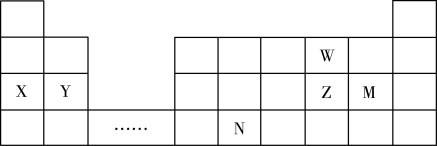
(1)N元素在周期表中的位置___________ ,根据周期表,推测N原子序数为___________
(2)比较Y、Z、W三种元素形成简单离子的半径由大到小的顺序___________ (用元素符号表示)
(3)M最高价氧化物的水化物在水中的电离方程式:___________
(4)以下说法正确的是___________
(5)由X、W元素构成的原子个数比为1:1的化合物所含化学键类型为___________ ,将一定量此化合物投入到足量的水中,产生2.24L气体(标准状况下),转移电子的物质的量为________ 。

(1)N元素在周期表中的位置
(2)比较Y、Z、W三种元素形成简单离子的半径由大到小的顺序
(3)M最高价氧化物的水化物在水中的电离方程式:
(4)以下说法正确的是___________
| A.单质的还原性:X>Y,可以用X与YM2溶液发生反应置换出Y来证明 |
| B.Y与同周期的ⅢA元素的原子序数相差1 |
| C.硅主要用于半导体器件的研制,目前用硅研发出的太阳能光伏电池,如我校的路灯 |
| D.元素N位于金属与非金属的分界线附近,可以推断N元素的单质可与氨水反应放出氢气 |
22-23高一下·安徽亳州·期中 查看更多[2]
安徽省亳州市第二完全中学2022-2023学年高一下学期期中考试化学试题(特培班)(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
更新时间:2023-05-17 07:21:55
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。

根据判断出的元素回答问题:
(1)f在周期表中的位置是____ 。
(2)比较d、e常见离子的半径大小(用化学式表示,下同):____ >____ ;比较g、h的最高价氧化物对应水化物的酸性强弱:____ >____ 。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:_________ 。
(4)已知1 mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:_________________ 。
(5)上述元素可组成盐R:zx4f(gd4)2。向盛有10 mL 1 mol·L-1 R溶液的烧杯中滴加1 mol·L-1 NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如图:
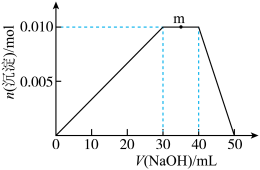
①R化学式为:________ ,其物质的量为________ 。
②写出m点反应的离子方程式:_________ 。
③若在R溶液中改加20 mL 1.1 mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_____ mol。

根据判断出的元素回答问题:
(1)f在周期表中的位置是
(2)比较d、e常见离子的半径大小(用化学式表示,下同):
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:
(4)已知1 mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:
(5)上述元素可组成盐R:zx4f(gd4)2。向盛有10 mL 1 mol·L-1 R溶液的烧杯中滴加1 mol·L-1 NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如图:

①R化学式为:
②写出m点反应的离子方程式:
③若在R溶液中改加20 mL 1.1 mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E是短周期元素,原子序数依次增大,B、C同周期,C的非金属性在元素周期表中最强,A、D同主族、隔周期,E元素原子最外层的p能级电子数是最外层的s能级电子数的一半。A、B能形成常温常压下两种液态化合物甲和乙,原子个数比分别为2:1和1:1.根据以上信息回答下列问题:
(1)甲、乙两种化合物中含有非极性共价键的物质的电子式是___________ ,C元素在元素周期表中的位置是___________ 。
(2)C和D形成的简单离子中,半径较小的是___________ (填离子符号)。
(3)将D的单质投入甲中,待D消失后再向溶液中加入E的单质,此时发生反应的化学方程式是___________ 。
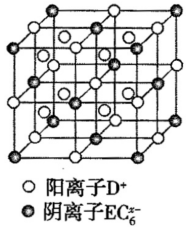
(4)C、D、E可组成离子化合物,其晶胞结构如图所示,阳离子D*(用○表示)位于正方体棱的中点和正方体内部;阴离子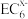 (用
(用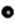 表示)位于该正方体的顶点和面心。该化合物的化学式是
表示)位于该正方体的顶点和面心。该化合物的化学式是___________ 。
(1)甲、乙两种化合物中含有非极性共价键的物质的电子式是
(2)C和D形成的简单离子中,半径较小的是
(3)将D的单质投入甲中,待D消失后再向溶液中加入E的单质,此时发生反应的化学方程式是
(4)C、D、E可组成离子化合物,其晶胞结构如图所示,阳离子D*(用○表示)位于正方体棱的中点和正方体内部;阴离子
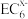 (用
(用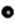 表示)位于该正方体的顶点和面心。该化合物的化学式是
表示)位于该正方体的顶点和面心。该化合物的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的气态氢化物能使湿润的红色石蕊试纸变蓝;C单质在实验室一般保存在煤油中;F的最高价氧化物对应水化物既能和酸反应又能和强碱反应,G单质是日常生活中用量最大的金属,易被腐蚀。请回答下列问题:

(1)A元素在周期表中的位置是____________ 。
(2)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中可能引起的环境问题有:(任写一种)。__________________ ;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH__ 7(填 “>"或“<”或“=”),若使所得溶液pH=7,则a_________ b(填“>"或“<”或“=”)。
(4)写出F的单质与NaOH溶液反应的离子方程式:____________________ 。
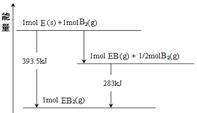
(5)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如下左图所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式__________________ 。
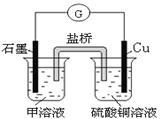
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如上右图所示,其反应中正极反应式为______________ 。某同学假设正极产物是Fe2+,请你设计实验证明该假设___________________ 。

(1)A元素在周期表中的位置是
(2)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中可能引起的环境问题有:(任写一种)。
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH
(4)写出F的单质与NaOH溶液反应的离子方程式:
(5)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如下左图所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式


(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如上右图所示,其反应中正极反应式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】L、M、R、T、W是原子序数依次增大的短周期主族元素,M、T在周期表中的相对位置如表;L与R原子的最外层电子数相同,R的单质是一种常见的半导体材料。请回答:
(1)T离子的结构示意图为_______ ,元素L在周期表中的位置为_______ ,
(2)M单质分子的电子式为_______ 。用电子式表示由W和Na组成的化合物的形成过程_______ 。
(3)R是组成玻璃的元素之一,不能用带磨口玻璃塞的试剂瓶盛放氢氧化钠溶液的原因是_______ (用化学方程式表示)。
(4)下列有关相应元素非金属性强弱比较的说法正确的是_______ (填字母序号)。
a.M的气态氢化物比R的气态氢化物稳定,则非金属性M强于R
b.高温下,L的单质能从R的最高价氧化物中置换出R,则非金属性L强于R
c.W核电荷数比T多,原子半径比T小,得电子能力比T强,则非金属性W强于T
(5)工业上可用二氧化硅、氯气和焦炭在高温条件下制备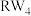 ,且该反应中除
,且该反应中除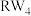 外的另一种产物可以用于工业冶炼铁。制备
外的另一种产物可以用于工业冶炼铁。制备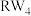 反应的化学方程式为
反应的化学方程式为_______ 。
| M | |
| T |
(2)M单质分子的电子式为
(3)R是组成玻璃的元素之一,不能用带磨口玻璃塞的试剂瓶盛放氢氧化钠溶液的原因是
(4)下列有关相应元素非金属性强弱比较的说法正确的是
a.M的气态氢化物比R的气态氢化物稳定,则非金属性M强于R
b.高温下,L的单质能从R的最高价氧化物中置换出R,则非金属性L强于R
c.W核电荷数比T多,原子半径比T小,得电子能力比T强,则非金属性W强于T
(5)工业上可用二氧化硅、氯气和焦炭在高温条件下制备
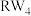 ,且该反应中除
,且该反应中除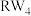 外的另一种产物可以用于工业冶炼铁。制备
外的另一种产物可以用于工业冶炼铁。制备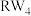 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为八种短周期主族元素的部分性质(已知铍的原子半径为0.89×10-10m):
(1)元素Z在元素周期表中的位置为______ 。
(2)写出 Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式________ 。
(3)R与T相比,非金属性较强的是____ (用元素符号表示),下列事实能证明这一结论的是_____ (填字母)。
a.常温下T的单质呈固态,R的单质呈气态
b.R的氢化物比T的氢化物稳定
c.R的氢化物水溶液酸性比T的氧化物对应水化物酸性强
(4)J与Q相比,金属性较强的是_____ (用元素符号表示),能证明这一结论的依据是__ 。
(5)根据表中数据推测,M的原子半径的最小范围是____________ 。
元素代号 | X | Y | Z | M | R | J | Q | T |
原子半径 /10-10m | 0.74 | 0.75 | 0.99 | 1.86 | 1.43 | 1.10 | ||
主要化合价 | -2 | +5、-3 | +4、-4 | +7、-1 | +1 | +3 | +5、-3 | |
其它 | 原子核内无中子 | 重要的半导体材料 | 有两种氧化物 |
(2)写出 Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式
(3)R与T相比,非金属性较强的是
a.常温下T的单质呈固态,R的单质呈气态
b.R的氢化物比T的氢化物稳定
c.R的氢化物水溶液酸性比T的氧化物对应水化物酸性强
(4)J与Q相比,金属性较强的是
(5)根据表中数据推测,M的原子半径的最小范围是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表列出了9种元素在元素周期表中的位置示意。
请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_______ 。
(2)画出元素⑧形成的简单离子的结构示意图_______ 。
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_______ 。
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是_______ 。
(5)⑤⑧⑨三种元素最高价的氧化物对应的水化物的酸性最弱的是_______ (填化学式)。
(6)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是_______ (填化学式),写出元素⑥的单质与水反应的离子反应方程式_______ ,写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式_______ 。
| 周期 | ⅠA 1 | 0 18 | ||||||
| 1 | ⅡA 2 | ⅢA 13 | ⅣA 14 | ⅤA 15 | ⅥA 16 | ⅦA 17 | ||
| 2 | ① | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | |||||
| 4 | ⑨ | |||||||
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是
(5)⑤⑧⑨三种元素最高价的氧化物对应的水化物的酸性最弱的是
(6)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:

(1)由②③④形成的简单离子半径由小到大顺序是_________ (填化学用语)。
(2)元素④的最高价氧化物对应的水化物和元素⑤的最高价氧化物对应的水化物反应的离子方程式为_______ ,⑦的单质和⑨的单质反应的化学方程式为________ ,冶炼单质⑤的方法是_______ (用化学方程式表示)。
(3)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式____ ,该分子中含有的共价键类型为_____ (填“极性共价键”或“非极性共价键”) 。
(4)下列有关性质的比较正确且能用元素周期律解释的是___ (填标号)
A.电负性:②>③ B.最高价氧化物对应的水化物的碱性:④>⑤
(5)③的简单氢化物的沸点高于⑦的简单氢化物的沸点的原因是_______ 。

(1)由②③④形成的简单离子半径由小到大顺序是
(2)元素④的最高价氧化物对应的水化物和元素⑤的最高价氧化物对应的水化物反应的离子方程式为
(3)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式
(4)下列有关性质的比较正确且能用元素周期律解释的是
A.电负性:②>③ B.最高价氧化物对应的水化物的碱性:④>⑤
(5)③的简单氢化物的沸点高于⑦的简单氢化物的沸点的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】如图是元素周期表的一部分。回答下列问题:

(1)世界上绝大部分卤素都存在于海洋中,海洋是卤素的资源宝库。
① 的离子结构示意图为
的离子结构示意图为________ 。
②表中几种元素的最高价氧化物对应水化物酸性最强的是________ (填化学式);写出该物质在水溶液中的电离方程式:________ 。
③用电子式表示短周期元素中,原子半径最大的元素与氯形成的简单化合物的形成过程:________ 。
④氰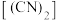 是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:
是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:________ 。
(2)硒是人体必需的微量元素,起到抗氧化的作用。
①写出Se在周期表中的位置:________ 。
② 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成Se和
气体发生反应,生成Se和 。写出
。写出 与
与 反应的化学方程式:
反应的化学方程式:________ 。
(3)下列说法正确的是________ (填字母)。
a.原子半径: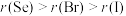
b. 中存在的化学键为非极性共价键
中存在的化学键为非极性共价键
c.非金属性:Cl>Se>Br

(1)世界上绝大部分卤素都存在于海洋中,海洋是卤素的资源宝库。
①
 的离子结构示意图为
的离子结构示意图为②表中几种元素的最高价氧化物对应水化物酸性最强的是
③用电子式表示短周期元素中,原子半径最大的元素与氯形成的简单化合物的形成过程:
④氰
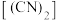 是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:
是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:(2)硒是人体必需的微量元素,起到抗氧化的作用。
①写出Se在周期表中的位置:
②
 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成Se和
气体发生反应,生成Se和 。写出
。写出 与
与 反应的化学方程式:
反应的化学方程式:(3)下列说法正确的是
a.原子半径:
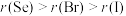
b.
 中存在的化学键为非极性共价键
中存在的化学键为非极性共价键c.非金属性:Cl>Se>Br
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】表为四种短周期元素的相关信息
回答下列问题(注:涉及元素的均要用对应元素的元素符号书写作答)
(1)Y元素的最简单氢化物的空间构型是_______ 。
(2)写出R与Z元素组成最高价氧化物的杂化方式_______ ,其VSEPR模型为_______ 。
(3)Z、Q、R相比,其原子半径由大到小的顺序是_______ 。
(4)Y与R相比,非金属性较强的是_______ ,能证明这一结论的事实是_______ 。(用化学方程式表示)
(5)Q单质在过量Y的最高价氧化物中燃烧,生成黑色颗粒并产生大量白烟,写出该反应的化学方程式_______ 。
| 元素 | 元素的相关信息 |
| Y | 原子最外层电子数是次外层电子数的2倍 |
| Z | 地壳中含量最多的元素 |
| Q | 短周期中金属性最强 |
| R | 常温下,R的单质是淡黄色固体,常在火山喷口附近沉积 |
(1)Y元素的最简单氢化物的空间构型是
(2)写出R与Z元素组成最高价氧化物的杂化方式
(3)Z、Q、R相比,其原子半径由大到小的顺序是
(4)Y与R相比,非金属性较强的是
(5)Q单质在过量Y的最高价氧化物中燃烧,生成黑色颗粒并产生大量白烟,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】有A、B、C、D、E、F六种短周期的主族元素,原子序数依次增大,其中A、D元素的原子最外层均只有一个电子,且A和D可形成离子化合物;C、F同主族,B元素位于元素周期表中的第二周期,且原子最外层电子数占核外电子总数的3/4,F元素原子最外电子层比同周期E元素原子的最外电子层多5个电子。试回答:
(1)D、F两元素最高价氧化物的水化物之间发生的化学方程式是__________ 。
(2)D的氢氧化物和C的氢化物在水溶液中反应的离子方程式为__________ 。
(3)E的氢氧化物的电子式是______________ ;B的氢化物的电子式是______________ 。
(1)D、F两元素最高价氧化物的水化物之间发生的化学方程式是
(2)D的氢氧化物和C的氢化物在水溶液中反应的离子方程式为
(3)E的氢氧化物的电子式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】元素是构成我们生活的世界中一切物质的“原材料”。
Ⅰ.1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
(1)门捷列夫将已有元素按照相对原子质量排序,同一_____ (填“横行”或“纵列”)元素性质相似。
(2)结合表中信息,猜想第5列方框中“Te=128?”的问号表达的含义是___________ 。
Ⅱ.X、Y、Z、W是现在元素周期表中的短周期元素,它们的相对位置如下图所示,其中 Y 元素原子核外最外层电子数是其电子层数的3倍。
请回答下列问题:
(1)W位于周期表中的位置____________________ 。
(2)比较Y、Z气态氢化物的稳定性______________ (用分子式表示)。
(3)科学家们认为存在含氢量最高的化合物XH5,预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式___________ ,XH5是离子化合物,它的电子式为________ 。
(4)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式_______________________________ 。
Ⅰ.1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
| Ni=Co=59 | |||||
| H=1 | Cu=63.4 | Ag=108 | Hg=200 | ||
| Be=9.4 | Mg=24 | Zn=65.2 | Cd=112 | ||
| B=11 | Al=27.4 | ?=68 | Ur=116 | Au=198? | |
| C=12 | Si=28 | ?=70 | Sn=118 | ||
| N=14 | P=31 | As=75 | Sb=122 | Bi=210? | |
| O=16 | S=32 | Se=79.4 | Te=128? | ||
| F=19 | Cl=35.5 | Br=80 | I=127 | ||
| Li=7 | Na=23 | K=39 | Rb=85.4 | Cs=133 | Tl=204 |
| Ca=40 | Pb=207 |
(2)结合表中信息,猜想第5列方框中“Te=128?”的问号表达的含义是
Ⅱ.X、Y、Z、W是现在元素周期表中的短周期元素,它们的相对位置如下图所示,其中 Y 元素原子核外最外层电子数是其电子层数的3倍。
| X | Y | |
| Z | W |
(1)W位于周期表中的位置
(2)比较Y、Z气态氢化物的稳定性
(3)科学家们认为存在含氢量最高的化合物XH5,预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式
(4)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,请参照元素①~⑤在表中的位置,回答下列问题:
(1)①的原子结构示意图是___________ 。
(2)②、③、④三种元素的原子半径最大的是___________ (写元素符号)。
(3)②和⑤的单质可反应生成离子化合物,写出该离子化合物的电子式___________ 。
(4)下列事实不能判断②和③的金属性强弱的是___________ (填字母,下同)。
a.常温下单质与水反应置换出氢气的难易程度
b.相同物质的量的单质与水反应置换出氢气的多少
c.最高价氧化物对应的水化物的碱性强弱
d.相同温度下,最高价氧化物对应的水化物的溶解度大小
(5)写出④的单质与②的最高价氧化物对应的水化物反应的化学方程式___________ 。
 | ⅠA | 0 | ||||||
| 1 | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | ||
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ |
(2)②、③、④三种元素的原子半径最大的是
(3)②和⑤的单质可反应生成离子化合物,写出该离子化合物的电子式
(4)下列事实不能判断②和③的金属性强弱的是
a.常温下单质与水反应置换出氢气的难易程度
b.相同物质的量的单质与水反应置换出氢气的多少
c.最高价氧化物对应的水化物的碱性强弱
d.相同温度下,最高价氧化物对应的水化物的溶解度大小
(5)写出④的单质与②的最高价氧化物对应的水化物反应的化学方程式
您最近一年使用:0次



