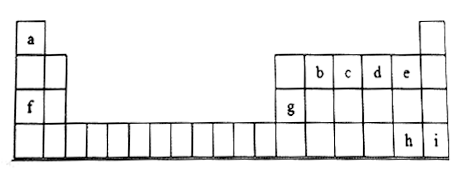
铝镁合金是指以镁为主要添加元素的铝合金,在具有较高的强度、耐腐蚀性基础上拥有更低的密度,在电子、汽车、航天等领域有广阔的应用前景。
(1)Al在元素周期表中的位置是第三周期___________ 族。
(2)Al的最高价氧化物对应的水化物的化学式是___________ 。
(3)Al的金属性弱于Mg的,用原子结构解释原因:Al与Mg位于同一周期,原子核外电子层数相同,___________ ,失电子能力Al弱于Mg。
(4)下列实验或事实能说明Mg的金属性强于Al的是___________ (填字母)。
A.碱性: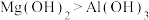
B.密度:Mg<Al
C.Mg能与热水缓慢反应,Al在热水中几乎不反应
(1)Al在元素周期表中的位置是第三周期
(2)Al的最高价氧化物对应的水化物的化学式是
(3)Al的金属性弱于Mg的,用原子结构解释原因:Al与Mg位于同一周期,原子核外电子层数相同,
(4)下列实验或事实能说明Mg的金属性强于Al的是
A.碱性:
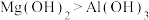
B.密度:Mg<Al
C.Mg能与热水缓慢反应,Al在热水中几乎不反应
更新时间:2023-06-16 14:27:21
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】图为元素周期表的一部分,请参照①~⑧在表中的位置,回答下列问题:

(1)⑥在周期表中的位置是_______ 。
(2)①~⑧中,化学性质最稳定的是_______ (填元素符号),非金属性最强的是_______ (填元素符号),最高价氧化物对应水化物酸性最强的是_______ (填化学式)。
(3)元素③的非金属性比⑥_______ (填“强”或“弱”),元素③④⑤原子半径由大到小的顺序:_______ (填元素符号)。

(1)⑥在周期表中的位置是
(2)①~⑧中,化学性质最稳定的是
(3)元素③的非金属性比⑥
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下表为元素周期表的一部分:
回答下列有关问题:
(1)上表中原子半径最小的元素是_______ (填元素符号)。
(2)表中所列元素中,最活泼的金属元素是_______ (填元素符号,下同),最活泼的非金属元素是_______ ,最不活泼的元素是_______ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式,下同),碱性最强的是_______ ,呈两性的是_______ ,最不稳定的气态氢化物是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
回答下列有关问题:
(1)上表中原子半径最小的元素是
(2)表中所列元素中,最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】分子筛是一类具有规整孔道结构的多孔材料,能够选择性吸附空间结构各异和不同尺寸的分子,在化学工业中有着广泛的应用。近年来,我国科学家在分子筛研究领域不断取得新的突破。这些研究中涉及的部分元素在周期表中位置如下:
(1)近期我国科学家制备了一种无缺陷的分子筛膜,可高效分离CH4与CO2两种气体。下列有关分子空间结构的描述正确的是_______
(2)传统的分子筛主要含有O、Na、Al和Si元素,通过调控这 4种元素的比例,可获得不同性能的分子筛产品。这4种元素描述中正确的是_______ 。
(3)通过将分子筛中的元素Na替换为K或Ca,可改变分子筛的孔径大小。这3种元素中说法正确的是_______
(4)N2常用于分子筛的孔结构测试,H、O和N元素可形成多种物质。下列说法正确的是_______
(5)某些分子筛可以选择性吸附Ar。Ar位于元素周期表的_______
| 周期 | 族 | ||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 1 | H | ||||||
| 2 | C | N | O | ||||
| 3 | Na | Al | Si | ||||
| 4 | K | Ca | |||||
| A.CH4是平面结构 | B.CO2是V形结构 |
| C.CH4是正四面体结构 | D.CO2是直线形结构 |
| A.非金属性最强的是O |
| B.核外电子数最少的是 Na |
| C.金属性最强的是Al |
| D.原子半径最大的是Si |
| A.仅Na可与Cl2反应 |
| B.K的单质与水的反应最剧烈 |
| C.Na的氧化物与水的反应均为化合反应 |
| D.Ca的最高价氧化物的水化物碱性最强 |
| A.N2中含有共价三键 |
| B.NO可由NH3催化氧化得到 |
| C.NH3的水溶液呈碱性 |
| D.稀HNO3与Cu反应产生H2 |
| A.第二周期 | B.Ⅷ族 | C.第三周期 | D.0族 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】针对下表中十种元素,填写空格。
(1)最不活泼的元素是_______________________ 。
(2)N、F、C1中,原子半径最大的是________ 。
(3)最高价氧化物对应水化物酸性最强的是________ (填名称)。
(4)写出实验室制氯气的离子方程式________________________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅦA | ⅧA | O |
2 | N | O | F | |||||
3 | Na | Mg | Al | S | Cl | Ar | ||
4 | K | Ca |
(1)最不活泼的元素是
(2)N、F、C1中,原子半径最大的是
(3)最高价氧化物对应水化物酸性最强的是
(4)写出实验室制氯气的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,请回答:
(1)钠元素在元素周期表中的位置是___________ ;
(2)N、O、F三种元素中,非金属性最强的是___________ (填元素符号);
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为___________ ;
(4)碘与氯是同主族元素。下面关于碘的推断错误的是___________ (选填字母);
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ||||||||
| 2 | N | O | F | |||||
| 3 | Na | Si | Cl |
(1)钠元素在元素周期表中的位置是
(2)N、O、F三种元素中,非金属性最强的是
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为
(4)碘与氯是同主族元素。下面关于碘的推断错误的是
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】请查阅铯在周期表中的位置,预测铯的性质,并回答下列问题。
(1)铯原子的最外层电子数是多少_____ ?
(2)铯和钾比较,谁的熔点高?_____
(3)铯与水反应时,可能观察到什么现象?_____
(4)铯和钾比较,谁的金属性强?试解释你的答案。_____
(5)在实验室中应如何储存铯?_____
(6)硝酸铯是离子化合物还是共价化合物?_____
(1)铯原子的最外层电子数是多少
(2)铯和钾比较,谁的熔点高?
(3)铯与水反应时,可能观察到什么现象?
(4)铯和钾比较,谁的金属性强?试解释你的答案。
(5)在实验室中应如何储存铯?
(6)硝酸铯是离子化合物还是共价化合物?
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】用“ ”或“
”或“ ”回答下列问题
”回答下列问题
①元素的非金属性越强,其对应最高价氧化物水化物的酸性越______ ;
②元素的金属性越强,其对应最高价氧化物水化物的碱性越______ ;
③元素的______ 性越强,其对应气态氢化物的稳定性越______ ;
④酸性: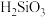
______ 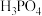 ;气态氢化物稳定性:
;气态氢化物稳定性:
______ HCl。
 ”或“
”或“ ”回答下列问题
”回答下列问题①元素的非金属性越强,其对应最高价氧化物水化物的酸性越
②元素的金属性越强,其对应最高价氧化物水化物的碱性越
③元素的
④酸性:
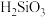
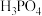 ;气态氢化物稳定性:
;气态氢化物稳定性:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】前面学习碱金属化学性质的比较时,通过金属钠、钾分别与氧气、水的反应,对比金属钠与金属钾的化学性质,再对比金属钠与金属钾的原子结构,认识原子半径对物质性质的影响,最终预测金属锂分别与氧气和水反应的现象。学习卤族元素化学性质的比较时,通过氟、氯、溴、碘与氢气的反应及卤素单质间的置换反应,对比卤族元素的性质。对于第三周期元素,电子层数相同,最外层电子数不同、原子半径不同,因此比较第三周期元素的性质时,需综合考虑最外层电子数与原子半径。
(1)问题一:可从哪些方面设计实验方案比较Na、Mg、Al金属性的强弱___ ?
(2)问题二:可从哪些方面设计实验方案比较Si、P、S、Cl非金属性的强弱___ ?
(1)问题一:可从哪些方面设计实验方案比较Na、Mg、Al金属性的强弱
(2)问题二:可从哪些方面设计实验方案比较Si、P、S、Cl非金属性的强弱
您最近一年使用:0次