铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
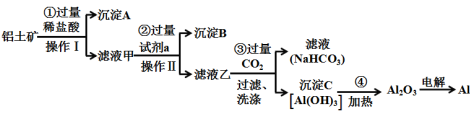
(1)用电解饱和食盐水制备试剂a的化学方程式为___________ ;
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为___________ ;
(3)步骤③中通入过量CO2气体而不加入过量盐酸的理由是___________ ;
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为___________ 。
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________ ;
a.MgO b.V2O5 c.Fe3O4 d.MnO2
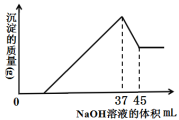
(6)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al2O3的百分含量为___________ 。

(1)用电解饱和食盐水制备试剂a的化学方程式为
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为
(3)步骤③中通入过量CO2气体而不加入过量盐酸的理由是
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是
a.MgO b.V2O5 c.Fe3O4 d.MnO2
(6)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al2O3的百分含量为

更新时间:2023-05-29 22:45:58
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某学习小组用如图所示装置测定铝镁合金中的铝的质量分数和铝的相对原子质量。

(1)A中试剂为_______ 。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是_______ 。
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂;⑤检查气密性。上述操作的顺序是_______ (填序号);记录C的液面位置时,除视线平视外,还应_______ 。
(4)B中发生反应的化学方程式为_______ 。
(5)若实验用铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为_______ 。
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得的质量分数将_______ (填“偏大”“偏小”或“不受影响”)。

(1)A中试剂为
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂;⑤检查气密性。上述操作的顺序是
(4)B中发生反应的化学方程式为
(5)若实验用铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得的质量分数将
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
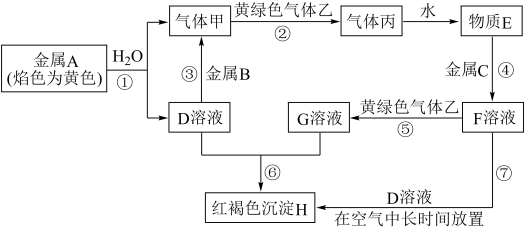
请根据以上信息完成下列各题:
(1)写出下列物质的化学式:B_______ ,丙_______ 。
(2)反应过程⑦可能观察到的实验现象是:_______ ,产生红褐色沉淀的化学方程式是 _______
(3)反应③中的离子方程式是_______
(4)反应⑤的离子方程式是_______
(5)反应⑦中如果可以长时间看到白色沉淀,应如何进行实验操作:_______ 。

请根据以上信息完成下列各题:
(1)写出下列物质的化学式:B
(2)反应过程⑦可能观察到的实验现象是:
(3)反应③中的离子方程式是
(4)反应⑤的离子方程式是
(5)反应⑦中如果可以长时间看到白色沉淀,应如何进行实验操作:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D是四种常见的单质,A、B为金属,C、D常温下是气体,且D为黄绿色气体。甲、乙、丙为常见的化合物,甲是黑色且具有磁性的物质。它们之间的转化关系如图所示:

请回答下列问题:
(1)B与甲反应的化学方程式是___ 。
(2)常温下,将A或B的单质放入浓硫酸或浓硝酸中,是否溶解?___ (填“是”或“否”)。
(3)将丙溶于水配成溶液,检验丙中阳离子的方法所加试剂是:___ 。
(4)写出A与水蒸气反应生成C和甲的化学方程式___ 。
(5)向A、B两种金属的混合物中加入足量的NaOH溶液,发生反应的离子方程式为:___ 。

请回答下列问题:
(1)B与甲反应的化学方程式是
(2)常温下,将A或B的单质放入浓硫酸或浓硝酸中,是否溶解?
(3)将丙溶于水配成溶液,检验丙中阳离子的方法所加试剂是:
(4)写出A与水蒸气反应生成C和甲的化学方程式
(5)向A、B两种金属的混合物中加入足量的NaOH溶液,发生反应的离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】铬铁矿的要紧成分可表示为FeO·Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如图所示。
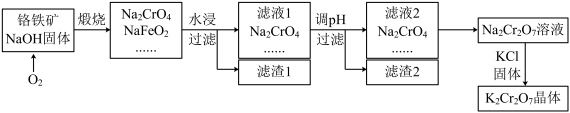
已知:①NaFeO2遇水强烈水解 。
②2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
请回答:
(1)K2Cr2O7中Cr元素的化合价是___ 。
(2)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是___ 。
(3)滤渣1为红褐色的固体,滤渣1的成分是(填名称 )____ ,滤液1的成分除Na2CrO4、NaOH外,还含有___ (填化学式 )。
(4)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是___ 。
(5)写出由滤液2转化为Na2Cr2O7溶液应采取的措施是___ 。
(6)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、____ 、过滤、洗涤、干燥。

已知:①NaFeO2遇水
②2CrO42-+2H+
 Cr2O72-+H2O
Cr2O72-+H2O请回答:
(1)K2Cr2O7中Cr元素的化合价是
(2)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是
(3)滤渣1为红褐色的固体,滤渣1的成分是(填
(4)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是
(5)写出由滤液2转化为Na2Cr2O7溶液应采取的措施是
(6)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某研究小组利用废弃的铁铝混合物(含Fe、Al、Al2O3、Fe2O3)回收金属铝和铁,实验流程设计如下:

(1)写出①中发生反应的离子方程式___________ 、_____________ 。
(2)下列说法正确的是_________ 。
a. ②中发生的是非氧化还原反应
b. ③中所得溶液D中含有Fe2+和Fe3+
c. ④和⑤分别采用电解法和热还原法
(3)由溶液D制取Fe2O3的实验过程是______________ 。
(4)该样品中Al2O3的质量分数是_____________ 。

(1)写出①中发生反应的离子方程式
(2)下列说法正确的是
a. ②中发生的是非氧化还原反应
b. ③中所得溶液D中含有Fe2+和Fe3+
c. ④和⑤分别采用电解法和热还原法
(3)由溶液D制取Fe2O3的实验过程是
(4)该样品中Al2O3的质量分数是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】红帘石矿的主要成分为Fe3O4、Al2O3、MnCO3、MgO少量MnO2 等。工业上将红帘石处理后运用阴离子膜电解法的新技术提取金属锰并制得绿色高效的水处理剂(K2FeO4)。工业流程如下:
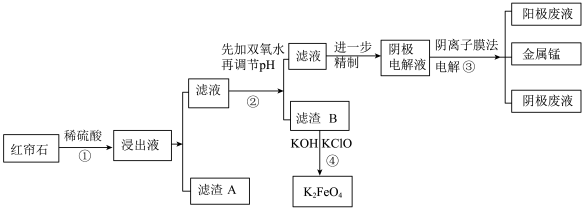
(1)在稀硫酸浸取矿石的过程中,MnO2可将Fe2+氧化为Fe3+,写出该反应的离子方程式:___________________ 。
(2)浸出液中的阳离子除H+、Fe2+、Fe3+外还有_____________ (填离子符号)。
(3)已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
步骤②中调节溶液的pH 等于6,调节pH的试剂最好选用下列哪种试剂__________ (填选项字母,下同)滤渣B除掉杂质后可进一步制取K2FeO4,除掉滤渣B中杂质最好选用下列哪种试剂:________ 。
a. 稀盐酸 b. KOH c. 氨水 d. MnCO3 e. CaCO3
(4)滤渣B经反应④生成高效水处理剂的离子方程式_______________ 。

(1)在稀硫酸浸取矿石的过程中,MnO2可将Fe2+氧化为Fe3+,写出该反应的离子方程式:
(2)浸出液中的阳离子除H+、Fe2+、Fe3+外还有
(3)已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
| 离子 | Fe3+ | Al3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 | 9.6 |
| 完全沉淀的pH | 3.7 | 4.7 | 9.6 | 9.8 | 11.1 |
a. 稀盐酸 b. KOH c. 氨水 d. MnCO3 e. CaCO3
(4)滤渣B经反应④生成高效水处理剂的离子方程式
您最近一年使用:0次



