铬铁矿的要紧成分可表示为FeO·Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如图所示。
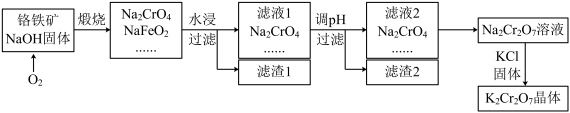
已知:①NaFeO2遇水强烈水解 。
②2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
请回答:
(1)K2Cr2O7中Cr元素的化合价是___ 。
(2)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是___ 。
(3)滤渣1为红褐色的固体,滤渣1的成分是(填名称 )____ ,滤液1的成分除Na2CrO4、NaOH外,还含有___ (填化学式 )。
(4)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是___ 。
(5)写出由滤液2转化为Na2Cr2O7溶液应采取的措施是___ 。
(6)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、____ 、过滤、洗涤、干燥。

已知:①NaFeO2遇水
②2CrO42-+2H+
 Cr2O72-+H2O
Cr2O72-+H2O请回答:
(1)K2Cr2O7中Cr元素的化合价是
(2)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是
(3)滤渣1为红褐色的固体,滤渣1的成分是(填
(4)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是
(5)写出由滤液2转化为Na2Cr2O7溶液应采取的措施是
(6)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、
更新时间:2020-02-16 13:56:42
|
相似题推荐
【推荐1】以高炉渣(主要成分为CaO、Al2O3、MgO和SiO2等)为原料矿化固定CO2并联产氧化铝的实验流程如下:

(1)活化浸出后富钙渣中的主要成分为___________ (填化学式)。
(2)CO2捕集在吸收塔中进行,反应生成(NH4)2CO3。含CO2的烟气应___________ (填“自上而下”或“自下而上”)通过吸收塔被氨水喷淋液充分吸收。
(3)矿化固定步骤是将富钙渣和除铝后的富镁液分别加入到CO2捕集液中,充分搅拌,捕集液中的(NH4)2CO3最终转化为碳酸盐矿物,实现封存CO2的目的。
①矿化反应需在40~50℃条件下进行,适宜的加热方式为___________ 。
②检验矿化固定2中矿化反应是否进行完全的实验操作是___________ 。
③将两步矿化后的母液合并,结晶处理得到___________ (填化学式),可循环利用。
(4)分离净化得到的NH4Al(SO4)2晶体可制备高纯Al2O3。请补充完整相应的实验方案:取一定量NH4Al(SO4)2晶体,经提纯后配成溶液,___________ ,控制反应温度为55℃,___________ ,干燥,置于马弗炉中900℃煅烧,获得高纯Al2O3产品。已知:酸性环境中生成的Al(OH)3黏性大,不易过滤。实验中可选用的试剂:1 mol·L-1的氨水、BaCl2溶液、蒸馏水。

(1)活化浸出后富钙渣中的主要成分为
(2)CO2捕集在吸收塔中进行,反应生成(NH4)2CO3。含CO2的烟气应
(3)矿化固定步骤是将富钙渣和除铝后的富镁液分别加入到CO2捕集液中,充分搅拌,捕集液中的(NH4)2CO3最终转化为碳酸盐矿物,实现封存CO2的目的。
①矿化反应需在40~50℃条件下进行,适宜的加热方式为
②检验矿化固定2中矿化反应是否进行完全的实验操作是
③将两步矿化后的母液合并,结晶处理得到
(4)分离净化得到的NH4Al(SO4)2晶体可制备高纯Al2O3。请补充完整相应的实验方案:取一定量NH4Al(SO4)2晶体,经提纯后配成溶液,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】单质铝应用极为广泛,从铝土矿中提取铝主要分以下三个阶段,根据要求回答相关问题
(1)铝土矿的提纯:铝土矿主要成分是Al2O3(含有Fe2O3、SiO2等杂质),提纯流程如下图所示:
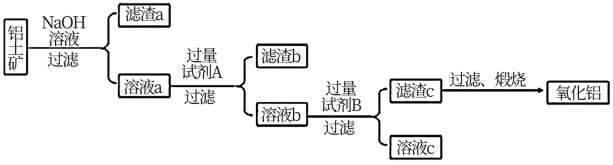
①在用NaOH溶液母液浸提过程中需研碎、湿磨,其目的是______________________________ 。
②向溶液a中通入过量CO2,所得不溶物煅烧后也可得Al2O3,该方法的缺点是___________________________________________________ 。
(2)制备无水氯化铝
其反应为:2Al2O3+6Cl2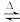 4AlCl3+O2
4AlCl3+O2
③为促进该反应的进行,实际生产中需加入焦炭,其原理是_____________________________ 。
(3)电解制取铝
目前可低温电解AlCl3熔盐得到金属铝纯的无水氯化铝熔点190℃,沸点180℃,其导电性如图:
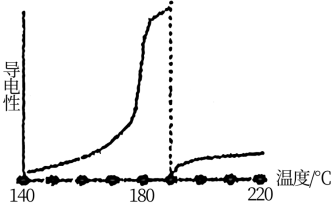
①从图中可知,AlCl3熔融液导电能力___________________________ 。
②但若在AlCl3中加入NaCl,使形成共融物,将AlCl3制成离子型液体,导电能力增强,熔融液中存在的阴离子是Cl-、AlCl4-、Al2Cl7-,请写AlCl3加入NaCl后形成离子型液体的两个离子方程式:AlCl3+ Cl-=AlCl4-、及平衡________________________________ 。
③电解时,阳极主要是AlCl4-放电,其电极反应为__________________________________ 。
④为保证电解进行,熔融液主要离子是AlCl4-、Al2Cl7-,则n(AlCl3)∶n(NaCl)应大于________ 。
(1)铝土矿的提纯:铝土矿主要成分是Al2O3(含有Fe2O3、SiO2等杂质),提纯流程如下图所示:

①在用NaOH溶液母液浸提过程中需研碎、湿磨,其目的是
②向溶液a中通入过量CO2,所得不溶物煅烧后也可得Al2O3,该方法的缺点是
(2)制备无水氯化铝
其反应为:2Al2O3+6Cl2
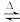 4AlCl3+O2
4AlCl3+O2③为促进该反应的进行,实际生产中需加入焦炭,其原理是
(3)电解制取铝
目前可低温电解AlCl3熔盐得到金属铝纯的无水氯化铝熔点190℃,沸点180℃,其导电性如图:

①从图中可知,AlCl3熔融液导电能力
②但若在AlCl3中加入NaCl,使形成共融物,将AlCl3制成离子型液体,导电能力增强,熔融液中存在的阴离子是Cl-、AlCl4-、Al2Cl7-,请写AlCl3加入NaCl后形成离子型液体的两个离子方程式:AlCl3+ Cl-=AlCl4-、及平衡
③电解时,阳极主要是AlCl4-放电,其电极反应为
④为保证电解进行,熔融液主要离子是AlCl4-、Al2Cl7-,则n(AlCl3)∶n(NaCl)应大于
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备金属铝的主要原料.工业上提取铝的工艺流程如下:
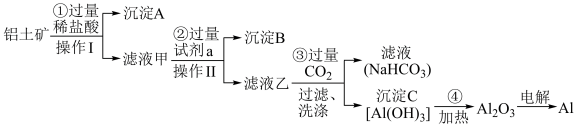
(1)沉淀A的化学式是_________ ,试剂a的化学式为______________ ;
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为______________________________________ ;
(3)Al2O3中所含的化学键的类型为___________________ ;
(4)工业上用电解熔融Al2O3的方法制备金属铝,其阳极反应式为______________________________ ;
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是( )
a MgO b V2O 5 c Fe3O4 d MnO2

(1)沉淀A的化学式是
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为
(3)Al2O3中所含的化学键的类型为
(4)工业上用电解熔融Al2O3的方法制备金属铝,其阳极反应式为
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是
a MgO b V2O 5 c Fe3O4 d MnO2
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
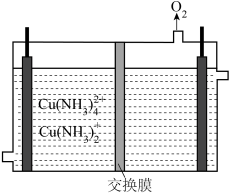
【推荐1】氯化亚铜是一种重要的化工产品,广泛用于颜料、电镀和有机合成等方面。它不溶于H2SO4和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解且被氧化成绿色的碱式氯化铜Cu(OH)Cl]。以海绵铜(主要成分是Cu,还含少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺流程如下:
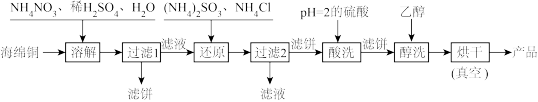
回答下列问题: .
(1)为了提高“溶解”速率,工业生产中宜采用的措施有_______________ (答两条即可)。.
(2)写出“溶解”过程中发生氧化还原反应的离子方程式:___________________ 。
(3)“过滤2”所得滤液经蒸发浓缩、冷却结晶过滤等操作获得一种化学肥料,它的主要成分是_________________ (填化学式)。
(4)工业生产中,用pH=2的硫酸洗涤“产品”,其目的是______________________ 。
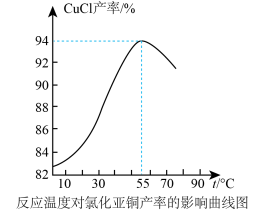
(5)氯化亚铜产率与温度的关系如图1所示。据图分析,流程化生产氯化亚铜的过程中,温度过低会影响CuCl产率的原因是_______________________ 。

回答下列问题: .
(1)为了提高“溶解”速率,工业生产中宜采用的措施有
(2)写出“溶解”过程中发生氧化还原反应的离子方程式:
(3)“过滤2”所得滤液经蒸发浓缩、冷却结晶过滤等操作获得一种化学肥料,它的主要成分是
(4)工业生产中,用pH=2的硫酸洗涤“产品”,其目的是
(5)氯化亚铜产率与温度的关系如图1所示。据图分析,流程化生产氯化亚铜的过程中,温度过低会影响CuCl产率的原因是


您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某小组利用工厂度弃物(主要含MgCO3、MgSiO3、Al2O3和Fe2O3 等)设计回收镁的工艺流程如下:
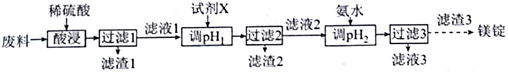
(1)酸浸过程中采用“粉碎废料、加热、搅拌、适当提高稀硫酸的浓度等”措施的目的是____________ 。为了提高产品的纯度,试剂X宜选择_______ (填选项字母)。
A.CuO B.MgO C.MgCO3 D.氨水
(2)滤渣2的主要成分是__________ (填化学式)。
(3)写出生成滤渣3的离子方程式:_______________________ 。
(4)已知:298K时,Ksp[Al(OH)3]=3.0×10-34、Ksp[Fe(OH)3]=4.0×10-38。
①加入试剂X,当Al3+ 开始沉淀时,滤液1中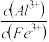 =
=____________ 。
②向浓度均为0.1mol·L-1 的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。在图中面出生成Al(OH)3的物质的量与滴加NaOH溶液体积的关系图(大致图)。______
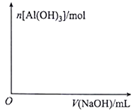
(5)若废料中镁元素的质量分数为a%,取mkg废料按上述流程生产,最终回收到20kg纯度为6%的镁锭,则镁的产率为__________ (用含a、b、m 的代数式表示)。
(6)参照上述流程图,设计经三步,由滤渣3得到镁锭的路线:_________________________ 。

(1)酸浸过程中采用“粉碎废料、加热、搅拌、适当提高稀硫酸的浓度等”措施的目的是
A.CuO B.MgO C.MgCO3 D.氨水
(2)滤渣2的主要成分是
(3)写出生成滤渣3的离子方程式:
(4)已知:298K时,Ksp[Al(OH)3]=3.0×10-34、Ksp[Fe(OH)3]=4.0×10-38。
①加入试剂X,当Al3+ 开始沉淀时,滤液1中
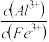 =
=②向浓度均为0.1mol·L-1 的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。在图中面出生成Al(OH)3的物质的量与滴加NaOH溶液体积的关系图(大致图)。

(5)若废料中镁元素的质量分数为a%,取mkg废料按上述流程生产,最终回收到20kg纯度为6%的镁锭,则镁的产率为
(6)参照上述流程图,设计经三步,由滤渣3得到镁锭的路线:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】铝硅合金材料性能优良。铝土矿(含30% SiO2、40.8% Al2O3和少量Fe2O3等)干法制取该铝硅合金的工艺如下:
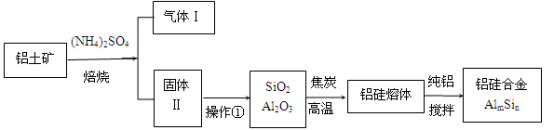
(1)焙烧除铁反应:
4(NH4)2SO4 + Fe2O3 2NH4Fe(SO4)2 + 3H2O + 6NH3↑
2NH4Fe(SO4)2 + 3H2O + 6NH3↑
(Al2O3部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为____________ 。指出气体Ⅰ的用途________________ (任写一种)。
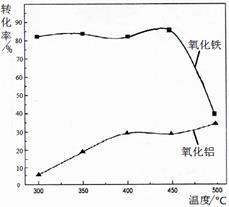
(2)操作①包括:加水溶解、________ 。若所得溶液中加入过量NaOH溶液,含铝微粒发生反应的离子方程式为______________________________________________ 。
(3)用焦炭还原SiO2、Al2O3会产生中间体SiC、Al4C3。任写一个高温下中间体又与Al2O3反应生成铝、硅单质的化学方程式___________________________________________ 。
(4)若湿法处理铝土矿,用强酸浸取时,所得溶液中阳离子有____________________________ ,假设该溶液中Al3+物质的量浓度为1.0 × 10-3mol/L,如果要将溶液在中的金属阳离子分离,则应控制溶液pH的范围为____________________________ (计算结果保留2位有效数字)。
(已知:Ksp[Fe(OH)3] = 8.0 × 10-38,Ksp[Al(OH)3] = 1.0 × 10-33,lg5 = 0.7)

(1)焙烧除铁反应:
4(NH4)2SO4 + Fe2O3
 2NH4Fe(SO4)2 + 3H2O + 6NH3↑
2NH4Fe(SO4)2 + 3H2O + 6NH3↑(Al2O3部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为

(2)操作①包括:加水溶解、
(3)用焦炭还原SiO2、Al2O3会产生中间体SiC、Al4C3。任写一个高温下中间体又与Al2O3反应生成铝、硅单质的化学方程式
(4)若湿法处理铝土矿,用强酸浸取时,所得溶液中阳离子有
(已知:Ksp[Fe(OH)3] = 8.0 × 10-38,Ksp[Al(OH)3] = 1.0 × 10-33,lg5 = 0.7)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】硼、镁及其化合物在工农业生产中应用广泛。
I.已知硼镁矿主要成分为Mg2B2O5•H2O,硼砂的化学式为Na2B4O7•10H2O。一种利用硼镁矿制取金属镁及粗硼的工艺流程如下所示:
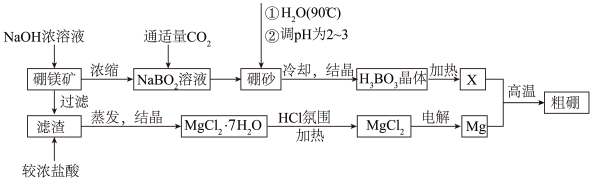
(1)硼砂中B元素的化合价为_______ ,将硼砂溶于热水后,用硫酸调节溶液的pH为2~3以制取H3BO3,该反应的离子方程式为____________________ 。X为H3BO3晶体加热脱水的产物,其与Mg反应制取粗硼的化学方程式为_____________ 。
(2)由MgCl2·7H2O制备MgCl2时,需要在HCl氛围中加热,其目的是________ 。
(3)镁-H2O2酸性燃料电池的反应原理为Mg+H2O2+2H+=Mg2++2H2O,常温下,若起始电解质溶液pH=1,则pH=2时,电解质溶液中所含Mg2+的物质的量浓度为_____________ mol·L-1。已知该温度下,Ksp[Mg(OH)2]=5.6×10-12,当电解质溶液的pH=6时,_______ (填“有”或“无”)Mg(OH)2沉淀析出。(忽略反应过程中溶液的体积变化)
II.工业上可用纳米MgH2和LiBH4组成的体系储放氢,如图所示。
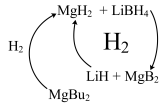
(4)写出放氢过程中发生反应的化学方程式:____________ 。
III. MgO浆液是一种高活性的脱硫剂,常用于脱除烟气中的SO2,发生的主要反应如下:
①Mg(OH)2+SO2=MgSO3+H2O
②MgSO3+SO2+H2O=Mg(HSO3)2
③Mg(HSO3)2+Mg(OH)2=2MgSO3+2H2O
④2MgSO3+O2=2MgSO4
已知25℃时,Ksp(MgSO3)=3.86×10-3,Ksp(CaSO3)=3.1×10-7。
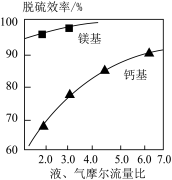
(5)其他条件相同时,镁基和钙基的脱硫效率与液、气摩尔流量比的变化情况如图所示。镁基的脱硫效率总比钙基的大,除生成的MgSO4具有良好的水溶性外,还因为_____________ 。
I.已知硼镁矿主要成分为Mg2B2O5•H2O,硼砂的化学式为Na2B4O7•10H2O。一种利用硼镁矿制取金属镁及粗硼的工艺流程如下所示:

(1)硼砂中B元素的化合价为
(2)由MgCl2·7H2O制备MgCl2时,需要在HCl氛围中加热,其目的是
(3)镁-H2O2酸性燃料电池的反应原理为Mg+H2O2+2H+=Mg2++2H2O,常温下,若起始电解质溶液pH=1,则pH=2时,电解质溶液中所含Mg2+的物质的量浓度为
II.工业上可用纳米MgH2和LiBH4组成的体系储放氢,如图所示。
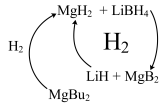
(4)写出放氢过程中发生反应的化学方程式:
III. MgO浆液是一种高活性的脱硫剂,常用于脱除烟气中的SO2,发生的主要反应如下:
①Mg(OH)2+SO2=MgSO3+H2O
②MgSO3+SO2+H2O=Mg(HSO3)2
③Mg(HSO3)2+Mg(OH)2=2MgSO3+2H2O
④2MgSO3+O2=2MgSO4
已知25℃时,Ksp(MgSO3)=3.86×10-3,Ksp(CaSO3)=3.1×10-7。
(5)其他条件相同时,镁基和钙基的脱硫效率与液、气摩尔流量比的变化情况如图所示。镁基的脱硫效率总比钙基的大,除生成的MgSO4具有良好的水溶性外,还因为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】摩尔盐[ ]是一种复盐,它易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,不易被氧化。制备摩尔盐的流程如下。
]是一种复盐,它易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,不易被氧化。制备摩尔盐的流程如下。

回答相关问题:
(1)步骤1中碱煮10分钟的目的是_______ 。
(2)步骤2中的“加热”,最佳加热方式为_______ (填“明火”或“水浴”)加热,理由是_______ 。
(3)步骤2中的“过滤”,需要趁热过滤,并用热水洗涤,其目的是_______ 。
(4)步骤3中“洗涤”,需用乙醇洗涤的目的是_______ 。
(5)步骤3中“加热浓缩”,所用到的主要仪器中属于硅酸盐材质的有酒精灯、玻璃棒和_______ 。
(6)样品中 含量测定:取30.00g所制得的固体于小烧杯中,加入适量稀硫酸,溶解后在250mL容量瓶中定容。取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000
含量测定:取30.00g所制得的固体于小烧杯中,加入适量稀硫酸,溶解后在250mL容量瓶中定容。取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000 酸性
酸性 溶液16.00mL,两者恰好完全反应。则此样品中
溶液16.00mL,两者恰好完全反应。则此样品中 含量为
含量为_______ %(保留小数点后1位)。导致该测定结果与理论值有偏差的可能原因是_______ 。
A.配溶液定容时俯视刻度线B.取摩尔盐溶液的滴定管没有润洗
C.取待测液的锥形瓶洗净后未干燥D.摩尔盐的结晶水数量不足
 ]是一种复盐,它易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,不易被氧化。制备摩尔盐的流程如下。
]是一种复盐,它易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,不易被氧化。制备摩尔盐的流程如下。
回答相关问题:
(1)步骤1中碱煮10分钟的目的是
(2)步骤2中的“加热”,最佳加热方式为
(3)步骤2中的“过滤”,需要趁热过滤,并用热水洗涤,其目的是
(4)步骤3中“洗涤”,需用乙醇洗涤的目的是
(5)步骤3中“加热浓缩”,所用到的主要仪器中属于硅酸盐材质的有酒精灯、玻璃棒和
(6)样品中
 含量测定:取30.00g所制得的固体于小烧杯中,加入适量稀硫酸,溶解后在250mL容量瓶中定容。取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000
含量测定:取30.00g所制得的固体于小烧杯中,加入适量稀硫酸,溶解后在250mL容量瓶中定容。取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000 酸性
酸性 溶液16.00mL,两者恰好完全反应。则此样品中
溶液16.00mL,两者恰好完全反应。则此样品中 含量为
含量为A.配溶液定容时俯视刻度线B.取摩尔盐溶液的滴定管没有润洗
C.取待测液的锥形瓶洗净后未干燥D.摩尔盐的结晶水数量不足
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】亚硝酰氯( ,熔点为
,熔点为 ℃,沸点为
℃,沸点为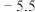 ℃)是一种红褐色液体或黄色气体,遇水反现生成一种氢化物和两种氧化物,可用于合成清洁剂、触媒剂及中间体等。某学习小组在实验室中用
℃)是一种红褐色液体或黄色气体,遇水反现生成一种氢化物和两种氧化物,可用于合成清洁剂、触媒剂及中间体等。某学习小组在实验室中用 和NO制备
和NO制备 。请回答下列问题:
。请回答下列问题:
(1)原料气NO和 的制备。
的制备。___________ 。实验室制备NO的反应的离子方程式为___________ 。
②实验室制备 可选择图中的装置
可选择图中的装置___________ (填标号);制备并收集干燥的 的装置连接顺序:a→
的装置连接顺序:a→___________ (按气流方向,用小写字母表示)。
(2)利用制得的NO和 制备亚硝酰氯
制备亚硝酰氯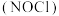 ,装置如图所示。
,装置如图所示。 外,另一个作用是
外,另一个作用是___________ 。
②装置Ⅳ的作用是___________ ;若无装置V,则装置Ⅳ中 可能发生反应的化学方相式为
可能发生反应的化学方相式为___________ 。
③查阅资料知,王水是浓硝酸与浓盐酸的混合酸,一定条件下该混合酸可自身反应生成亚硝酰氯、氯气和水,该反应的化学方程式为___________ 。
 ,熔点为
,熔点为 ℃,沸点为
℃,沸点为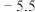 ℃)是一种红褐色液体或黄色气体,遇水反现生成一种氢化物和两种氧化物,可用于合成清洁剂、触媒剂及中间体等。某学习小组在实验室中用
℃)是一种红褐色液体或黄色气体,遇水反现生成一种氢化物和两种氧化物,可用于合成清洁剂、触媒剂及中间体等。某学习小组在实验室中用 和NO制备
和NO制备 。请回答下列问题:
。请回答下列问题:(1)原料气NO和
 的制备。
的制备。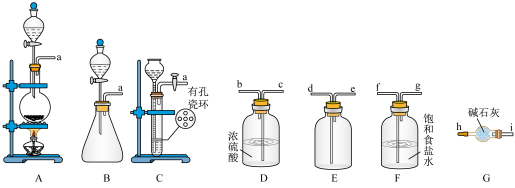
②实验室制备
 可选择图中的装置
可选择图中的装置 的装置连接顺序:a→
的装置连接顺序:a→(2)利用制得的NO和
 制备亚硝酰氯
制备亚硝酰氯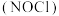 ,装置如图所示。
,装置如图所示。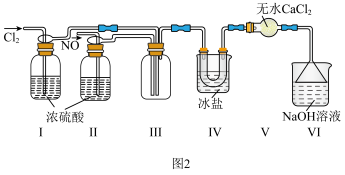
 外,另一个作用是
外,另一个作用是②装置Ⅳ的作用是
 可能发生反应的化学方相式为
可能发生反应的化学方相式为③查阅资料知,王水是浓硝酸与浓盐酸的混合酸,一定条件下该混合酸可自身反应生成亚硝酰氯、氯气和水,该反应的化学方程式为
您最近一年使用:0次



