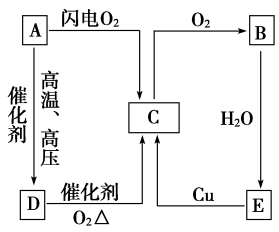
化合物X是新型电子材料的主要成分,由两种元素 组成,为了研究其组成,设计并完成如下实验:
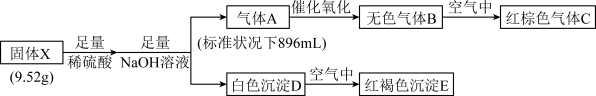
固体E受热分解可得红棕色固体F,请回答:
(1)气体A的空间构型___________ ,化合物X的化学式___________ 。
(2)白色沉淀D在空气中变成红褐色沉淀E的原因是___________ (用化学方程式表示)。
(3)高温条件下,气体A与固体F反应生成水和两种单质,该反应的化学方程式为___________ 。
(4)请设计实验判断D已完全转化为E___________ 。

固体E受热分解可得红棕色固体F,请回答:
(1)气体A的空间构型
(2)白色沉淀D在空气中变成红褐色沉淀E的原因是
(3)高温条件下,气体A与固体F反应生成水和两种单质,该反应的化学方程式为
(4)请设计实验判断D已完全转化为E
更新时间:2023-07-05 20:52:02
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】如图表示A、B、C、D、E五种含氮物质相互转化的关系图。其中A、B、C、D常温下都是气体,B为红棕色。
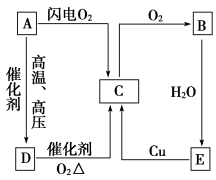
回答下列问题:
(1)A→D反应常用于人工固氮,写出该反应的化学方程式:_______ 。
(2)D→C是工业制硝酸的重要反应,化学方程式为_______ 。
(3)B与一定量的氧气混合通入水中能被完全吸收,则B与 的物质的量之比为
的物质的量之比为_______ ,若该反应转移 个电子,则参加反应的B的物质的量为
个电子,则参加反应的B的物质的量为_______ mol。

回答下列问题:
(1)A→D反应常用于人工固氮,写出该反应的化学方程式:
(2)D→C是工业制硝酸的重要反应,化学方程式为
(3)B与一定量的氧气混合通入水中能被完全吸收,则B与
 的物质的量之比为
的物质的量之比为 个电子,则参加反应的B的物质的量为
个电子,则参加反应的B的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】硅单质化学性质不活泼,但常温下能与强碱溶液反应,下面几种含硅元素的物质之间的相互转化关系如图所示:

(1)写出图示反应的几种物质的化学式:
B____________ ,C____________ ,D________________ 。
(2)写出下列反应的化学方程式:
①B→A:_________________________________________________ ;
②B→E:______________________________________________________ 。
(3)写出下列溶液中反应的离子方程式:
D→C:___________________________________________________ 。

(1)写出图示反应的几种物质的化学式:
B
(2)写出下列反应的化学方程式:
①B→A:
②B→E:
(3)写出下列溶液中反应的离子方程式:
D→C:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】如图,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请据图回答下列问题:

(1)A、G的化学式分别为___________ 、___________ 。
(2)写出反应①的化学方程式:___________ 。
(3)写出反应②的化学方程式:___________ 。
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊溶液中,观察到的现象是___________ 。请写出A与水反应的化学方程式:___________ 。
②A可以制漂白粉,漂白粉可用于游泳池中水的消毒,原理是(用化学方程式表示):___________ 。

(1)A、G的化学式分别为
(2)写出反应①的化学方程式:
(3)写出反应②的化学方程式:
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊溶液中,观察到的现象是
②A可以制漂白粉,漂白粉可用于游泳池中水的消毒,原理是(用化学方程式表示):
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】NH3是重要的化工原料。
Ⅰ.氨气的制备
(1)实验室用下列装置制备NH3,装置依次为_____ 。_____ 。
(3)下列物质能用于干燥氨气的有_____  填字母序号
填字母序号 。
。
 固体
固体  碱石灰
碱石灰  浓
浓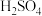
Ⅱ.氨气的性质
(4)按下图装置进行NH3性质实验。_____ ,稳定后,关闭旋塞1.
②再打开旋塞2,B瓶中的现象是_____ 。
(5)探究氨气的还原性
通入干燥 将装置空气排尽后加热,装置Ⅰ中生成黑色粉末,经验证为FeO;装置Ⅱ中无水
将装置空气排尽后加热,装置Ⅰ中生成黑色粉末,经验证为FeO;装置Ⅱ中无水 粉末变为蓝色;装置Ⅲ无水
粉末变为蓝色;装置Ⅲ无水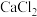 的质量增加,还排出一种无色无味、无污染的气体。
的质量增加,还排出一种无色无味、无污染的气体。 还原
还原 的化学方程式
的化学方程式_____ 。
②设计实验验证 完全转化为FeO:
完全转化为FeO:_____ 。
Ⅰ.氨气的制备
(1)实验室用下列装置制备NH3,装置依次为
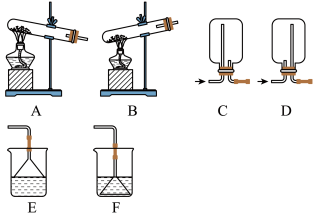
(3)下列物质能用于干燥氨气的有
 填字母序号
填字母序号 。
。 固体
固体  碱石灰
碱石灰  浓
浓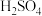
Ⅱ.氨气的性质
(4)按下图装置进行NH3性质实验。
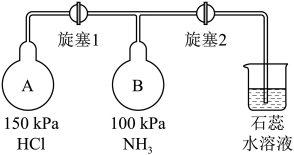
②再打开旋塞2,B瓶中的现象是
(5)探究氨气的还原性
通入干燥
 将装置空气排尽后加热,装置Ⅰ中生成黑色粉末,经验证为FeO;装置Ⅱ中无水
将装置空气排尽后加热,装置Ⅰ中生成黑色粉末,经验证为FeO;装置Ⅱ中无水 粉末变为蓝色;装置Ⅲ无水
粉末变为蓝色;装置Ⅲ无水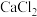 的质量增加,还排出一种无色无味、无污染的气体。
的质量增加,还排出一种无色无味、无污染的气体。
 还原
还原 的化学方程式
的化学方程式②设计实验验证
 完全转化为FeO:
完全转化为FeO:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】正盐A能发生下图所示的反应,图中①~⑧分别代表有关反应中的一种物质(某些物质已略去),其中①、②、④、⑤为无色气体。

请完成下列各题:
(1)写出化学式A_______ ⑥_______ ⑦_______
(2)写出下列反应方程式:
⑧+⑦ ②+③+⑥:
②+③+⑥:_______
①+④ ⑤:
⑤:_______
(3)⑧ ⑤的离子方程式为:
⑤的离子方程式为:_______

请完成下列各题:
(1)写出化学式A
(2)写出下列反应方程式:
⑧+⑦
 ②+③+⑥:
②+③+⑥:①+④
 ⑤:
⑤:(3)⑧
 ⑤的离子方程式为:
⑤的离子方程式为:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】某校课外活动小组为探究铜与稀硝酸反应产生的气体主要是NO,设计了下列实验。图中K为止水夹,F是装有一半空气的注射器,其中十加热装置和固定装置均已略去。请回答:
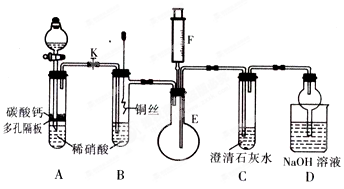
(1)设置装置A的目的是___________ ;实验开始后,如何判断A的实验目的已完成________________________________ 。
(2)当完成装置A的实验目的后,关闭K,再将装置B中的铜丝插入稀硝酸.B中反应的离子方程式为____________________ 。
(3)将F中的空气推入E中,证明NO存在的实验现象是____________________________ ,此过程发生反应的化学方程式是______________________________________________ 。
(4)装置D中NaOH溶液的作用是________________________________________ 。写出可能发生的一个化学方程式___________________________________________________ 。

(1)设置装置A的目的是
(2)当完成装置A的实验目的后,关闭K,再将装置B中的铜丝插入稀硝酸.B中反应的离子方程式为
(3)将F中的空气推入E中,证明NO存在的实验现象是
(4)装置D中NaOH溶液的作用是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】非金属单质A在常温下为气体,经如图所示的过程转化为含氧酸D,已知D为强酸,且C是红棕色气体。请回答下列问题。
A B
B C
C D
D
(1)A的化学式是___________ 。
(2)写出C与水反应的化学方程式___________ 。
(3)写出D的稀溶液在常温下与铜反应的离子方程式___________ 。
A
 B
B C
C D
D(1)A的化学式是
(2)写出C与水反应的化学方程式
(3)写出D的稀溶液在常温下与铜反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】利用钛白工业的副产物硫酸亚铁[含Ti(SO4)2及少量Fe2(SO4)3]制取铁红的工艺流程如图所示。

(1)加热近沸条件下“精制”硫酸亚铁的过程中,Ti4+会与水作用生成偏钛酸(H2TiO3)沉淀,此反应的离子方程式为__________ ,加入铁屑的作用是__________ (用离子方程式表示)。
(2)“氧化”工序中发生反应的化学方程式有________ 。
(3)滤渣2能溶于酸和浓强碱,不溶于水。洗涤滤渣2最好选用的试剂是______ (填写序号)。
a 稀硫酸 b 稀盐酸 c 浓NaOH溶液 d 蒸馏水
(4)副产品M的化学式为_________ ,由滤液得到M的操作为蒸发浓缩、_____ 、_____ 、洗涤、干燥。

(1)加热近沸条件下“精制”硫酸亚铁的过程中,Ti4+会与水作用生成偏钛酸(H2TiO3)沉淀,此反应的离子方程式为
(2)“氧化”工序中发生反应的化学方程式有
(3)滤渣2能溶于酸和浓强碱,不溶于水。洗涤滤渣2最好选用的试剂是
a 稀硫酸 b 稀盐酸 c 浓NaOH溶液 d 蒸馏水
(4)副产品M的化学式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上表面皿,观察现象。

(1)浓盐酸液滴附近会出现_____________ 现象。
(2)浓硫酸液滴一开始没有明显现象,一段时间后液滴中有白色固体产生,该固体可能是一种酸式盐,其化学式为________________ 。
(3)FeSO4液滴中先出现灰绿色沉淀,过一段时间变成红褐色,发生的反应包括(用方程式表示):
①______________ (用离子方程式表示)
②____________ (用化学方程式表示)

(1)浓盐酸液滴附近会出现
(2)浓硫酸液滴一开始没有明显现象,一段时间后液滴中有白色固体产生,该固体可能是一种酸式盐,其化学式为
(3)FeSO4液滴中先出现灰绿色沉淀,过一段时间变成红褐色,发生的反应包括(用方程式表示):
①
②
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】用 溶液刻蚀铜电路板,对刻蚀后的液体(含
溶液刻蚀铜电路板,对刻蚀后的液体(含 、
、 和
和 )进行处理以提取
)进行处理以提取 和
和 ,流程如图所示:
,流程如图所示:
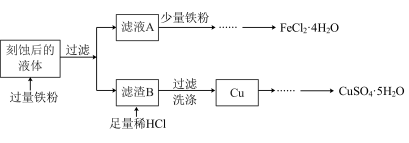
回答下列问题:
(1)氯化铁溶液刻蚀铜电路板的离子方程式为_______ ,过氧化氢和盐酸的混合溶液也可以刻蚀铜电路板,反应的化学方程式为_______ 。
(2)取少量滤液 ,滴入
,滴入 溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成
溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成_______ 沉淀。白色沉淀转化过程对应的化学方程式为_______ 。
(3)检验刻蚀后液体中 通常选用的试剂为
通常选用的试剂为_______ ,滤渣 的主要成分为
的主要成分为_______ 。
(4)检验滤渣 中提取出的
中提取出的 已经洗净的操作为
已经洗净的操作为_______ 。
 溶液刻蚀铜电路板,对刻蚀后的液体(含
溶液刻蚀铜电路板,对刻蚀后的液体(含 、
、 和
和 )进行处理以提取
)进行处理以提取 和
和 ,流程如图所示:
,流程如图所示:
回答下列问题:
(1)氯化铁溶液刻蚀铜电路板的离子方程式为
(2)取少量滤液
 ,滴入
,滴入 溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成
溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成(3)检验刻蚀后液体中
 通常选用的试剂为
通常选用的试剂为 的主要成分为
的主要成分为(4)检验滤渣
 中提取出的
中提取出的 已经洗净的操作为
已经洗净的操作为
您最近一年使用:0次