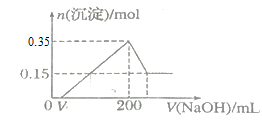
将0.1 mol的镁和铝的混合物溶于50 mL 4 mol·L-1 H2SO4溶液中,然后再滴加2 mol·L-1的NaOH溶液。请回答下列问题:
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V的变化如图所示。当V1=80 mL时,计算金属粉末中镁的物质的量及V2的体积。
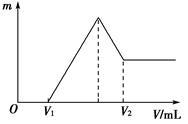
(2)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,计算滴入NaOH溶液的体积。
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V的变化如图所示。当V1=80 mL时,计算金属粉末中镁的物质的量及V2的体积。

(2)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,计算滴入NaOH溶液的体积。
14-15高一上·浙江宁波·期末 查看更多[2]
更新时间:2019-01-30 18:14:09
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】计算填空。
(1)2.3gNa和足量的水反应生成气体在标况下气体的体积是___ 。
(2)5.1g镁和铝混合物与足量的盐酸反应放出气体在标准下5.6L,则镁和铝物质的量之比是___ 。
(3)2.8g铁与足量的氯气反应转移电子数是___ 。
(1)2.3gNa和足量的水反应生成气体在标况下气体的体积是
(2)5.1g镁和铝混合物与足量的盐酸反应放出气体在标准下5.6L,则镁和铝物质的量之比是
(3)2.8g铁与足量的氯气反应转移电子数是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】向500mL氢氧化钠溶液中投入10.8g铝,二者恰好完全反应,计算回答下列问题:
(1)参加反应的铝的物质的量是_______ mol。
(2)分别求氧氧化钠溶液的物质的量浓度和在标准状况下反应生成氢气的体积_____ (请写出计算过程)。
(1)参加反应的铝的物质的量是
(2)分别求氧氧化钠溶液的物质的量浓度和在标准状况下反应生成氢气的体积
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将镁、铝的混合物0.1 mol溶于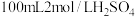 溶液中,然后再滴加1mol/L的NaOH溶液,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示
溶液中,然后再滴加1mol/L的NaOH溶液,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示
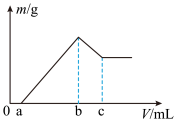
计算:
(1)当a =160mL时,金属混合物中n(Mg)=_____ mol,n(Al)=______ mol,c =______ mL;
(2)若欲使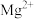 、
、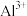 刚好完全沉淀,则加入的NaOH的体积V应为
刚好完全沉淀,则加入的NaOH的体积V应为______ 毫升?
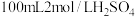 溶液中,然后再滴加1mol/L的NaOH溶液,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示
溶液中,然后再滴加1mol/L的NaOH溶液,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示
计算:
(1)当a =160mL时,金属混合物中n(Mg)=
(2)若欲使
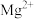 、
、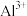 刚好完全沉淀,则加入的NaOH的体积V应为
刚好完全沉淀,则加入的NaOH的体积V应为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
请回答下列问题:
①写出该反应的离子反应方程式_________________________,②反应中被氧化的HCl的物质的量为 ________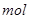 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________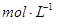 。
。
(2)把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入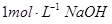 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
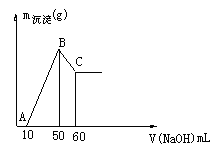
①合金中镁的质量 g。
②盐酸的物质的量浓度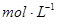 。
。
 MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。请回答下列问题:
①写出该反应的离子反应方程式_________________________,②反应中被氧化的HCl的物质的量为 ________
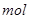 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________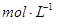 。
。(2)把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入
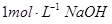 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
①合金中镁的质量 g。
②盐酸的物质的量浓度
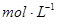 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】将0.1 mol的镁、铝混合物溶于100 mL 2mol/LH2SO4溶液中,然后再滴加1 mol/L NaOH溶液。请回答:
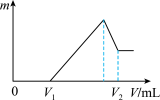
⑴若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。当V1=160mL时,则金属粉末中n(Mg)=______________ mol,V2=______________ mL。
⑵若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)_________ mL。
⑶若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:______________ 。

⑴若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。当V1=160mL时,则金属粉末中n(Mg)=
⑵若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)
⑶若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某混合溶液中氯化镁浓度为2mol/L,含三氯化铝的浓度为3mol/L,则将200mL此溶液中的Mg2+转化为Mg(OH)2沉淀分离析出,至少需要1.6mol/L氢氧化钠溶液的体积是_________ ?
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐2】小苏打、胃舒、平达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.5g NaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是___________ mol。
(2)胃舒平每片含0.245g Al(OH)3。中和胃酸时,6片小苏打片相当于胃舒平_____ 片。
(3)达喜的化学成分是铝和镁的碱式盐。
①取该碱式盐3.01g,加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比。________
②在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后重1.74g,若该碱式盐中氢元素的质量分数为0.040,试推测该碱式盐的化学式。
________
(1)小苏打片每片含0.5g NaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是
(2)胃舒平每片含0.245g Al(OH)3。中和胃酸时,6片小苏打片相当于胃舒平
(3)达喜的化学成分是铝和镁的碱式盐。
①取该碱式盐3.01g,加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比。
②在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后重1.74g,若该碱式盐中氢元素的质量分数为0.040,试推测该碱式盐的化学式。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】0.1 mol的镁、铝混合物溶于100 mL 2mol·L-1H2SO4溶液中,然后再滴加1 mol·L-1NaOH溶液。请回答:

(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。当V1=120mL时,则金属粉末中n(Mg)=________ ,V2=________ mL。
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=________ mL。
(3)若向300mL 1 mol/LAL2(SO4)3的溶液中逐渐加入浓度为1mol/L的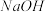 溶液,若产生2.34克白色沉淀,则加入的NaOH溶液的体积可能为
溶液,若产生2.34克白色沉淀,则加入的NaOH溶液的体积可能为__________ 毫升。
(4)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol·L-1硫酸溶解此混合物后,再加入460 mL 1 mol·L-1NaOH溶液,所得沉淀中无Al(OH)3。满足条件的a的取值范围是________ 。

(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。当V1=120mL时,则金属粉末中n(Mg)=
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=
(3)若向300mL 1 mol/LAL2(SO4)3的溶液中逐渐加入浓度为1mol/L的
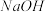 溶液,若产生2.34克白色沉淀,则加入的NaOH溶液的体积可能为
溶液,若产生2.34克白色沉淀,则加入的NaOH溶液的体积可能为(4)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol·L-1硫酸溶解此混合物后,再加入460 mL 1 mol·L-1NaOH溶液,所得沉淀中无Al(OH)3。满足条件的a的取值范围是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】向MgCl2和AlCl3的混合溶液中逐滴加入NaOH溶液直至过量。经测定,加入NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示。

(1)写出各段所发生反应的离子方程式:
OD段___________________________________________ ;
DC段___________________________________________ 。
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为__________ 。
(3)图中C点表示当加入__________ molNaOH时,Al3+已经__________ ,Mg2+已经__________ 。
(4)图中OA=_____ mol;AB=_______ mol。

(1)写出各段所发生反应的离子方程式:
OD段
DC段
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为
(3)图中C点表示当加入
(4)图中OA=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】向20mL某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如下图所示:

(1)写出AB段发生反应的离子方程式___________ 。
(2)A点表示的意义是__________ 。
(3)所用AlCl3溶液的物质的量浓度是________ 。
(4)当所得沉淀量为0.39g时,用去NaOH溶液的体积是_______ mL或______ mL。
(5)向B点处的溶液中通入少量CO2会有什么现象__________ ,写出离子方程式__________ 。

(1)写出AB段发生反应的离子方程式
(2)A点表示的意义是
(3)所用AlCl3溶液的物质的量浓度是
(4)当所得沉淀量为0.39g时,用去NaOH溶液的体积是
(5)向B点处的溶液中通入少量CO2会有什么现象
您最近一年使用:0次

 溶液反应可以生成多硫化钠(
溶液反应可以生成多硫化钠(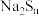 ),离子反应为:
),离子反应为: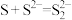 、
、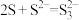 …
…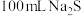 溶液中加入
溶液中加入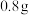 硫粉,只发生
硫粉,只发生 和
和 无剩余,则原
无剩余,则原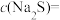
 。
。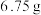 硫粉,控制一定条件使硫粉完全反应,反应后溶液中的阴离子有
硫粉,控制一定条件使硫粉完全反应,反应后溶液中的阴离子有 、
、 、
、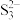 (忽略其他阴离子),且物质的量之比为
(忽略其他阴离子),且物质的量之比为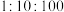 。则反应后溶液中的
。则反应后溶液中的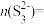
 。(写出计算过程)
。(写出计算过程)