(1)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
请回答下列问题:
①写出该反应的离子反应方程式_________________________,②反应中被氧化的HCl的物质的量为 ________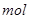 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________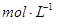 。
。
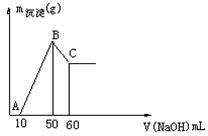
(2)把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入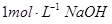 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
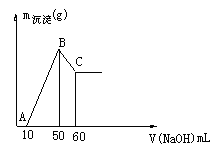
①合金中镁的质量 g。
②盐酸的物质的量浓度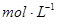 。
。
 MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。请回答下列问题:
①写出该反应的离子反应方程式_________________________,②反应中被氧化的HCl的物质的量为 ________
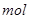 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________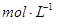 。
。(2)把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入
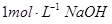 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
①合金中镁的质量 g。
②盐酸的物质的量浓度
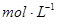 。
。
更新时间:2015/06/03 17:16:14
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】KClO3和浓盐酸在一定温度下反应会生成红黄色的易爆物二氧化氯。
2KClO3+4HCl(浓) 2KCl+2ClO2↑+Cl2↑+2H2O
2KCl+2ClO2↑+Cl2↑+2H2O
(1)该反应中氧化剂为______ ,氧化产物为______ 。
(2)若反应生成0.1 mol Cl2,则转移的电子数为______ 。
(3)ClO2具有很强的氧化性,因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)1 kg的ClO2相当于______ kg的Cl2。(提示:Cl2和ClO2在消毒过程中均变为-1价的Cl)。
2KClO3+4HCl(浓)
 2KCl+2ClO2↑+Cl2↑+2H2O
2KCl+2ClO2↑+Cl2↑+2H2O(1)该反应中氧化剂为
(2)若反应生成0.1 mol Cl2,则转移的电子数为
(3)ClO2具有很强的氧化性,因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)1 kg的ClO2相当于
您最近一年使用:0次
【推荐2】关于离子反应:M2O7x-+3S2﹣+14H+=2M3++3S↓+7H2O其中x值和M2O7x-离子中M化合价分别是______ 和______ .
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
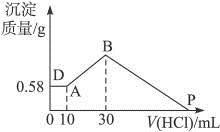
【推荐1】把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58 g白色难溶物析出,向所得溶液中逐滴加入0.5 mol • L-1的盐酸,加入盐酸的体积和生成沉淀的质量如下图所示:
请计算:
(1)混合物中A1C13和MgCl2的质量____________________ ;
(2)P点表示盐酸加入的体积____________________ 。
请计算:
(1)混合物中A1C13和MgCl2的质量
(2)P点表示盐酸加入的体积
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】将共0.4molMg、Al的混合物用盐酸完全溶解,放出标准状况下11.2L气体,然后再滴2mol/LNaOH溶液,请回答:
(1)求该混合物中Mg、Al的物质的量之比______________
(2)若该Mg、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V=________________ mL。
(3)若该Mg、Al混合物溶于400mL 3mol/L盐酸后,滴入NaOH溶液,使所得沉淀中无Al(OH)3,则滴入NaOH溶液的体积最少为_____________________ mL。
(1)求该混合物中Mg、Al的物质的量之比
(2)若该Mg、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V=
(3)若该Mg、Al混合物溶于400mL 3mol/L盐酸后,滴入NaOH溶液,使所得沉淀中无Al(OH)3,则滴入NaOH溶液的体积最少为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】回答下列问题
(1)标准状况下112mL气体A的质量为0.32g,则A气体的摩尔质量为____ 。
(2)标准状况下有四种气体:①6.72LC2H6;②3.01×1024个HCl分子;③0.2molH2S;④10.2gNH3。各气体中氢原子数的大小顺序为(用①②③④表示):______________ 。
(3)在300mL由NaCl、MgCl2、AlCl3组成的混合液中,部分离子浓度大小如图所示,回答下列问题。____ mol。将该混合液加水稀释至体积为500mL,稀释后溶液中Al3+物质的量浓度为______ mol/L。
②向①中稀释后的溶液中加入过量氢氧化钠溶液,则发生反应的离子方程式为:_________ ;最终可得到沉淀质量为________ 。
(1)标准状况下112mL气体A的质量为0.32g,则A气体的摩尔质量为
(2)标准状况下有四种气体:①6.72LC2H6;②3.01×1024个HCl分子;③0.2molH2S;④10.2gNH3。各气体中氢原子数的大小顺序为(用①②③④表示):
(3)在300mL由NaCl、MgCl2、AlCl3组成的混合液中,部分离子浓度大小如图所示,回答下列问题。

②向①中稀释后的溶液中加入过量氢氧化钠溶液,则发生反应的离子方程式为:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】将NaOH、MgCl2、A1C13三种固体组成的混合物溶于足量水后得1.16g白色沉淀。在所得的浊液中逐滴加入1mol·L-1HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:
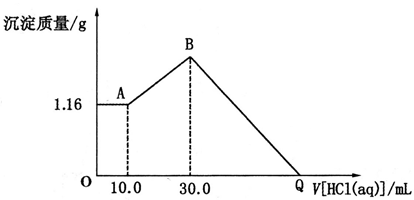
(1)写出混合物溶于水时发生反应的离子方程式:_____________________________ 。
(2)写出AB段反应的离子方程式:_______________________________ 。
(3)原混合物中NaOH的物质的量是多少?(写出计算过程)___________ 。

(1)写出混合物溶于水时发生反应的离子方程式:
(2)写出AB段反应的离子方程式:
(3)原混合物中NaOH的物质的量是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】把一定质量的镁、铝混合物投入到2 mol·L-1的盐酸中,待金属完全溶解后,向溶液中加入2 mol·L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示。则:

(1)金属铝的质量为_________ 。
(2)a的取值范围是_______________ 。
(3)盐酸的体积是____________ ml。
(4)n(Mg)/n(Al)的最大值是________ 。
(5)80~90ml对应反应的离子方程式________________________ 。

(1)金属铝的质量为
(2)a的取值范围是
(3)盐酸的体积是
(4)n(Mg)/n(Al)的最大值是
(5)80~90ml对应反应的离子方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
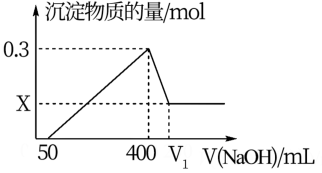
【推荐2】把7.5 g镁铝合金的粉末放入200ml 4mol/L的盐酸中,往充分反应后的混合溶液中逐渐滴入一定物质的量浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积的关系如图所示。
(1)合金中镁的物质的量为_______ 。
(2)氢氧化钠的物质的量浓度为_______ mol/L。
(3)V1=_______ mL。
(4)写出该合金溶于足量NaOH溶液的化学方程式为_________ 。
(1)合金中镁的物质的量为
(2)氢氧化钠的物质的量浓度为
(3)V1=
(4)写出该合金溶于足量NaOH溶液的化学方程式为
您最近一年使用:0次


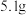 镁铝合金溶于
镁铝合金溶于 溶液中,恰好完全溶解后再加入
溶液中,恰好完全溶解后再加入 的
的 溶液,得到沉淀的最大质量为
溶液,得到沉淀的最大质量为 ,继续滴加
,继续滴加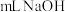 溶液时,可使溶解在硫酸中的
溶液时,可使溶解在硫酸中的 和
和 恰好完全沉淀。
恰好完全沉淀。

