肉桂酸是无公害的环保防腐剂,可直接添加于食品中。某小组设计实验制备肉桂酸并探究其性质:
【原理】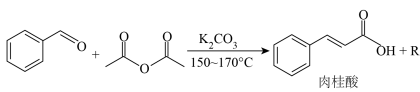
【性质】
【步骤】
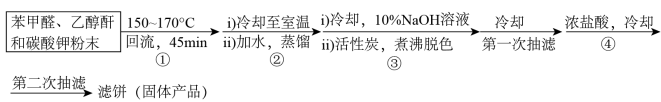
【装置】利用图1装置完成步骤①,利用图2装置完成步骤②,抽滤操作用图3装置。
回答下列问题:
(1)R是_______ (填结构简式)。
(2)图1中,仪器B的名称是_______ ,仪器A的作用是_______ 。实验前,要烘干三颈烧瓶,目的是_______ 。
(3)相比于普通过滤,图3抽滤的主要优点有_______ (答一条即可)。
(4)步骤③加入 溶液的作用是
溶液的作用是_______ ,第二次抽滤得到滤饼的主要成分是_______ (填名称)。
(5)设计简单实验证明肉桂酸中含有碳碳双键:_______ 。
【原理】

【性质】
| 物质 | 苯甲醛 | 肉桂酸 | 乙酸酐 |
| 沸点 | 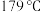 |  |  |
| 水溶性 | 微溶于水、无色油状液体 | 难溶于冷水、易溶于热水 | 与水反应生成乙酸 |

【装置】利用图1装置完成步骤①,利用图2装置完成步骤②,抽滤操作用图3装置。

回答下列问题:
(1)R是
(2)图1中,仪器B的名称是
(3)相比于普通过滤,图3抽滤的主要优点有
(4)步骤③加入
 溶液的作用是
溶液的作用是(5)设计简单实验证明肉桂酸中含有碳碳双键:
更新时间:2023-07-12 07:23:15
|
相似题推荐
解答题-有机推断题
|
较难
(0.4)
名校
【推荐1】以1,3—丁二烯(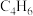 )为原料能合成多种四碳二元酸,其线路如下:
)为原料能合成多种四碳二元酸,其线路如下:
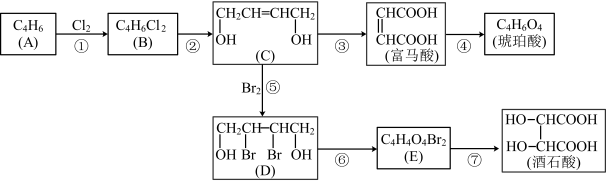
请回答下列问题:
(1)写出反应⑥的类型_______ ,反应⑦的条件_______ ,琥珀酸的结构简式:_______ 。
(2)写出反应②的化学方程式:_______ 。
(3)由C氧化生成富马酸的过程中可能因氧化不充分生成富马醛酸(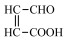 ),再经反应④使产物琥珀酸中含有的副产物是(填写结构简式)
),再经反应④使产物琥珀酸中含有的副产物是(填写结构简式)_______ ;检验富马酸中是否有富马醛酸的试剂是_______ ;
(4)C的同分异构体中,能够发生银镜反应,且遇金属钠产生气体的有_______ 种;请写出其中一种不能被灼热的铜丝催化氧化的异构体的结构简式_______ 。
(5)请设计一条由B制备氯丁橡胶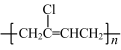 的合成路线,所需无机试剂任选
的合成路线,所需无机试剂任选________ 。(合成路线常用的表示方式为:M N
N 目标产物)
目标产物)
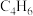 )为原料能合成多种四碳二元酸,其线路如下:
)为原料能合成多种四碳二元酸,其线路如下:
请回答下列问题:
(1)写出反应⑥的类型
(2)写出反应②的化学方程式:
(3)由C氧化生成富马酸的过程中可能因氧化不充分生成富马醛酸(
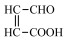 ),再经反应④使产物琥珀酸中含有的副产物是(填写结构简式)
),再经反应④使产物琥珀酸中含有的副产物是(填写结构简式)(4)C的同分异构体中,能够发生银镜反应,且遇金属钠产生气体的有
(5)请设计一条由B制备氯丁橡胶
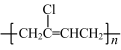 的合成路线,所需无机试剂任选
的合成路线,所需无机试剂任选 N
N 目标产物)
目标产物)
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】某芳香烃A,分子式为C8H10 ;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色;J分子内有两个互为对位的取代基。在一定条件下有如下的转化关系(无机物略去):
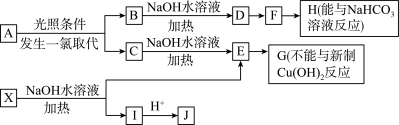
(1)属于芳香烃类的A的一种同分异构体(不包括A)中,在同一平面的原子最多有_____________ 个;
(2)J中所含的含氧官能团的名称为______________ 。
(3)E与H反应的化学方程式是_______________________ ;反应类型是__________ 。
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物M,以M为单体合成的高分子化合物的名称是________________
(5)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式。①与FeCl3溶液作用显紫色;②与新制Cu(OH)2悬浊液作用产生红色沉淀;③苯环上的一卤代物有2种。____________________________

(1)属于芳香烃类的A的一种同分异构体(不包括A)中,在同一平面的原子最多有
(2)J中所含的含氧官能团的名称为
(3)E与H反应的化学方程式是
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物M,以M为单体合成的高分子化合物的名称是
(5)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式。①与FeCl3溶液作用显紫色;②与新制Cu(OH)2悬浊液作用产生红色沉淀;③苯环上的一卤代物有2种。
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】有机物Q是一种抗血栓药物,其合成路线如下。
(1)A和J均属于芳香化合物,J中含有的官能团是_______ 。
(2)A→B的反应类型是_______ 。
(3)D→E的化学方程式为_______ 。
(4)X的分子式为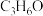 ,G的结构简式为
,G的结构简式为_______ 。
(5)下列说法正确的是_______ (填序号)。
a.可用新制的 检验X中的官能团
检验X中的官能团
b.反应①除了生成L外,还生成
c.反应③的原子利用率为100%
(6)N是L的同分异构体,写出符合下列条件的所有N的结构简式(不考虑立体异构)_______ 。
i.含有苯环,且苯环上只有1个取代基
ii.1molN与足量 溶液反应产生2mol气体
溶液反应产生2mol气体

已知:i. +H2O(
+H2O( 、
、 、
、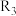 代表烃基或H)
代表烃基或H)
ii.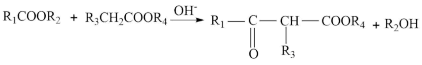
(1)A和J均属于芳香化合物,J中含有的官能团是
(2)A→B的反应类型是
(3)D→E的化学方程式为
(4)X的分子式为
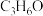 ,G的结构简式为
,G的结构简式为(5)下列说法正确的是
a.可用新制的
 检验X中的官能团
检验X中的官能团b.反应①除了生成L外,还生成

c.反应③的原子利用率为100%
(6)N是L的同分异构体,写出符合下列条件的所有N的结构简式(不考虑立体异构)
i.含有苯环,且苯环上只有1个取代基
ii.1molN与足量
 溶液反应产生2mol气体
溶液反应产生2mol气体
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】铊(Tl)在工业中的用途非常广泛,其中铊锡合金可作超导材料:铊镉合金是原子能工业中的重要材料。铊主要从铅精矿焙烧产生的富铊灰(主要成分PbO、ZnO、 、FeO、
、FeO、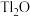 等)中提炼,具体工艺流程如图。
等)中提炼,具体工艺流程如图。

已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂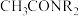 的二乙苯溶液,萃取过程的反应原理为
的二乙苯溶液,萃取过程的反应原理为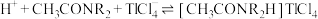 。
。
回答下列问题:
(1)浸取过程中硫酸的作用除了酸化提供 ,另一作用为
,另一作用为_______ 。
(2)在实验室中,“萃取”过程使用的玻璃仪器有_______ ,用平衡移动解释“反萃取”过程的原理和目的_______ 。
(3)“还原、氧化、沉淀”过程中生成TlCl,该反应的离子方程式为_______ ,为提高经济效益充分利用原料,该反应的滤液可加入_______ 步骤循环使用最合适。
(4)Tl对人体毒性很大,难溶盐 可通过离子交换治疗
可通过离子交换治疗 中毒,将其转化为沉淀同时生成
中毒,将其转化为沉淀同时生成 溶液,写出治疗
溶液,写出治疗 中毒的离子方程式:
中毒的离子方程式:_______ 。
 、FeO、
、FeO、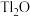 等)中提炼,具体工艺流程如图。
等)中提炼,具体工艺流程如图。
已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂
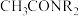 的二乙苯溶液,萃取过程的反应原理为
的二乙苯溶液,萃取过程的反应原理为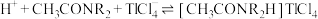 。
。回答下列问题:
(1)浸取过程中硫酸的作用除了酸化提供
 ,另一作用为
,另一作用为(2)在实验室中,“萃取”过程使用的玻璃仪器有
(3)“还原、氧化、沉淀”过程中生成TlCl,该反应的离子方程式为
(4)Tl对人体毒性很大,难溶盐
 可通过离子交换治疗
可通过离子交换治疗 中毒,将其转化为沉淀同时生成
中毒,将其转化为沉淀同时生成 溶液,写出治疗
溶液,写出治疗 中毒的离子方程式:
中毒的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】铈( )的氧化物在半导体材料、高级颜料及汽车尾气的净化器方面有广泛应用。以氟碳铈矿(含
)的氧化物在半导体材料、高级颜料及汽车尾气的净化器方面有广泛应用。以氟碳铈矿(含 、
、 、
、 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图:
(1) 中氟元素对应的氟原子激发态的电子排布式有
中氟元素对应的氟原子激发态的电子排布式有_______ (填序号)。
a. b.
b.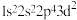 c.
c. d.
d.
(2)“氧化焙烧”后, 元素转化为
元素转化为 和
和 。写出“氧化焙烧”时
。写出“氧化焙烧”时 发生的化学反应方程式:
发生的化学反应方程式:_______ 。
(3)实验室进行操作①所需的玻璃仪器有烧杯、_______ 。
(4)“系列操作”包含下图几个过程: 不能溶于有机物
不能溶于有机物 ;
; 能溶于有机物
能溶于有机物 ,且存在反应
,且存在反应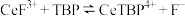 。“滤液
。“滤液 ”中加入有机物
”中加入有机物 后的分离方法是
后的分离方法是_______ ,“有机层B”中发生反应的离子方程式为_______ 。
(5)已知25℃时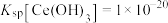 ,“调
,“调 ”时,要使
”时,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制
为沉淀完全),应控制 大于
大于_______ 。
(6) 立方晶胞结构如图所示。
立方晶胞结构如图所示。_______ 。
②阿伏加德罗常数的值为 ,
, 摩尔质量为
摩尔质量为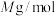 ,晶体密度为
,晶体密度为 ,其晶胞边长的计量表达式为
,其晶胞边长的计量表达式为
_______  。
。
 )的氧化物在半导体材料、高级颜料及汽车尾气的净化器方面有广泛应用。以氟碳铈矿(含
)的氧化物在半导体材料、高级颜料及汽车尾气的净化器方面有广泛应用。以氟碳铈矿(含 、
、 、
、 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图: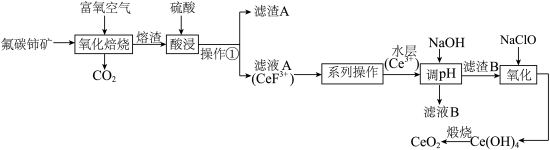
(1)
 中氟元素对应的氟原子激发态的电子排布式有
中氟元素对应的氟原子激发态的电子排布式有a.
 b.
b.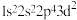 c.
c. d.
d.
(2)“氧化焙烧”后,
 元素转化为
元素转化为 和
和 。写出“氧化焙烧”时
。写出“氧化焙烧”时 发生的化学反应方程式:
发生的化学反应方程式:(3)实验室进行操作①所需的玻璃仪器有烧杯、
(4)“系列操作”包含下图几个过程:

 不能溶于有机物
不能溶于有机物 ;
; 能溶于有机物
能溶于有机物 ,且存在反应
,且存在反应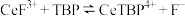 。“滤液
。“滤液 ”中加入有机物
”中加入有机物 后的分离方法是
后的分离方法是(5)已知25℃时
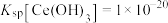 ,“调
,“调 ”时,要使
”时,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制
为沉淀完全),应控制 大于
大于(6)
 立方晶胞结构如图所示。
立方晶胞结构如图所示。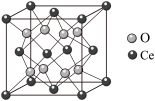
②阿伏加德罗常数的值为
 ,
, 摩尔质量为
摩尔质量为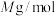 ,晶体密度为
,晶体密度为 ,其晶胞边长的计量表达式为
,其晶胞边长的计量表达式为
 。
。
您最近一年使用:0次
【推荐3】环烷酸镍(易溶于汽油)主要用于顺丁橡胶的合成,也可用于其他产品的有机合成。一种用废镍催化剂(含Ni、Al、Cr、FeS、C及难溶物)制备环烷酸镍(常温下为液体)的工艺流程如下:

该工艺条件下溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”的目的是_______ ,干燥后“灼烧”的主要目的是_______ 。
(2)“酸溶”时,先加入一定量的水,然后分次加入浓硫酸,与直接用稀硫酸溶解相比,其优点是_______ 。
(3)“氧化”时, 被氧化为
被氧化为 的离子方程式为
的离子方程式为_______ 。
(4)“调 ”时,溶液
”时,溶液 的范围为
的范围为_______ ,加入的“试剂 ”适宜是
”适宜是_______ (填标号)。
A. B.
B. C.
C.
(5)若环烷酸用 表示,则“合成”反应的化学方程式为
表示,则“合成”反应的化学方程式为_______ 。
(6)“分离”得到产品包含的操作有_______ 。

该工艺条件下溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |  |
| 开始沉淀的pH | 1.9 | 7.0 | 6.4 | 4.6 |
| 完全沉淀的pH | 3.2 | 9.0 | 8.4 | 5.6 |
回答下列问题:
(1)“碱浸”的目的是
(2)“酸溶”时,先加入一定量的水,然后分次加入浓硫酸,与直接用稀硫酸溶解相比,其优点是
(3)“氧化”时,
 被氧化为
被氧化为 的离子方程式为
的离子方程式为(4)“调
 ”时,溶液
”时,溶液 的范围为
的范围为 ”适宜是
”适宜是A.
 B.
B. C.
C.
(5)若环烷酸用
 表示,则“合成”反应的化学方程式为
表示,则“合成”反应的化学方程式为(6)“分离”得到产品包含的操作有
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】下图是实验室制取乙炔气体及乙炔的性质实验的装置,气密性已检验,部分夹持装置略。___________ ;
(2)圆底烧瓶中生成乙炔的化学方程式是___________ ;
(3)硫酸铜溶液的作用是___________ ;
(4)将通过硫酸铜溶液的气体通入溴的四氯化碳溶液中,反应的方程式是___________ ;若改为通入酸性高锰酸钾溶液中,现象是___________ ;
(5)乙炔与氯化氢加成可以生成氯乙烯聚合生成聚氯乙烯的方程式是___________ 。

(2)圆底烧瓶中生成乙炔的化学方程式是
(3)硫酸铜溶液的作用是
(4)将通过硫酸铜溶液的气体通入溴的四氯化碳溶液中,反应的方程式是
(5)乙炔与氯化氢加成可以生成氯乙烯聚合生成聚氯乙烯的方程式是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】己二酸(M=146)是制备尼龙-66的重要原料。在实验室通常用高锰酸钾氧化环己醇制备:

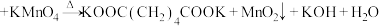 (未配平)。该反应强烈放热,其它相关信息列表如表:
(未配平)。该反应强烈放热,其它相关信息列表如表:
实验步骤:
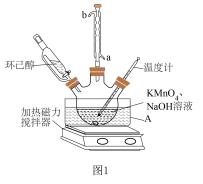
Ⅰ.将50mL 10%NaOH溶液、50mL水、6g 加入如图1的三颈烧瓶中,待
加入如图1的三颈烧瓶中,待 完全溶解后,缓慢滴加环己醇(2.1mL),并维持温度45℃,滴加完毕后,将温度提升到90℃,使得氧化完全。
完全溶解后,缓慢滴加环己醇(2.1mL),并维持温度45℃,滴加完毕后,将温度提升到90℃,使得氧化完全。
Ⅱ.趁热抽滤、 滤渣用热水洗涤3次,合并滤液和洗涤液,用4mL浓盐酸酸化,在石棉网上加热浓缩至溶液体积为10mL左右,降温结晶、抽滤、称重得2.6g产品。
滤渣用热水洗涤3次,合并滤液和洗涤液,用4mL浓盐酸酸化,在石棉网上加热浓缩至溶液体积为10mL左右,降温结晶、抽滤、称重得2.6g产品。
回答下列问题:
(1)仪器A中应加入___________ (填“水”或“油”)作为热传导介质,配平题干中的化学方程式:___________ 。
(2)步骤Ⅰ缓慢滴加环己醇的原因是___________ 。
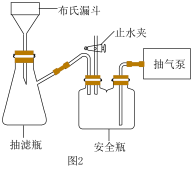
(3)抽滤装置如图2所示,与普通过滤相比,其优点是___________ 。
(4)步骤Ⅱ中用盐酸酸化的目的是___________ 。
(5)根据相关信息可知,己二酸易溶于乙醇,步骤Ⅱ不选择乙醇洗涤 滤渣的原因是
滤渣的原因是___________ (答出一点即可)。
(6)产品纯度测定
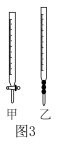
①准确称取1.0g产品加水溶解,配制成100.00mL溶液,取出25.00mL于锥形瓶中,用0.10 的NaOH标准溶液滴定至终点,消耗NaOH溶液20.00mL;己二酸溶液应盛放在如图3仪器
的NaOH标准溶液滴定至终点,消耗NaOH溶液20.00mL;己二酸溶液应盛放在如图3仪器___________ (填“甲”或“乙”)中。
②产品的纯度为___________ 。

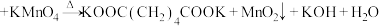 (未配平)。该反应强烈放热,其它相关信息列表如表:
(未配平)。该反应强烈放热,其它相关信息列表如表:| 物质 | 性状 | 密度 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 环己醇 | 液体或晶体 | 0.9624 | 25.2 | 161 | 可溶于乙醇、乙醚 |
| 己二酸 | 固体 | 1.360 | 151.3 | 265 | 易溶于乙醇和热水 |
Ⅰ.将50mL 10%NaOH溶液、50mL水、6g
 加入如图1的三颈烧瓶中,待
加入如图1的三颈烧瓶中,待 完全溶解后,缓慢滴加环己醇(2.1mL),并维持温度45℃,滴加完毕后,将温度提升到90℃,使得氧化完全。
完全溶解后,缓慢滴加环己醇(2.1mL),并维持温度45℃,滴加完毕后,将温度提升到90℃,使得氧化完全。Ⅱ.趁热抽滤、
 滤渣用热水洗涤3次,合并滤液和洗涤液,用4mL浓盐酸酸化,在石棉网上加热浓缩至溶液体积为10mL左右,降温结晶、抽滤、称重得2.6g产品。
滤渣用热水洗涤3次,合并滤液和洗涤液,用4mL浓盐酸酸化,在石棉网上加热浓缩至溶液体积为10mL左右,降温结晶、抽滤、称重得2.6g产品。
回答下列问题:
(1)仪器A中应加入
(2)步骤Ⅰ缓慢滴加环己醇的原因是
(3)抽滤装置如图2所示,与普通过滤相比,其优点是

(4)步骤Ⅱ中用盐酸酸化的目的是
(5)根据相关信息可知,己二酸易溶于乙醇,步骤Ⅱ不选择乙醇洗涤
 滤渣的原因是
滤渣的原因是(6)产品纯度测定
①准确称取1.0g产品加水溶解,配制成100.00mL溶液,取出25.00mL于锥形瓶中,用0.10
 的NaOH标准溶液滴定至终点,消耗NaOH溶液20.00mL;己二酸溶液应盛放在如图3仪器
的NaOH标准溶液滴定至终点,消耗NaOH溶液20.00mL;己二酸溶液应盛放在如图3仪器
②产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】硼氢化钠(NaBH4)通常为白色粉末,容易吸水潮解,在有机合成中被称为“万能还原剂”。制备硼氢化钠的流程如图:
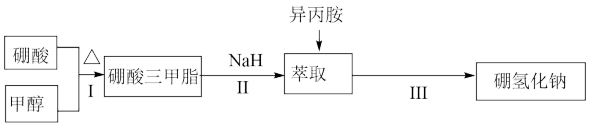
步骤Ⅰ:硼酸三甲酯[B(OCH3)3]的制备(已知硼酸三甲酯能水解)。将硼酸(H3BO3)和适量甲醇加入圆底烧瓶中,然后缓慢地加入浓硫酸,振荡,在烧瓶上加装分馏柱a,用电炉经水浴锅加热,回流2小时,收集硼酸三甲酯与甲醇共沸液。装置如图所示(夹持装置略去,下同)。
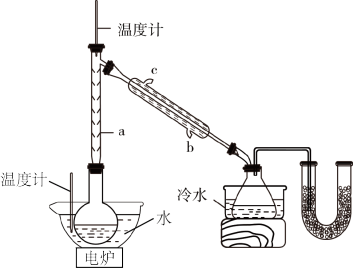
(1)直形冷凝管冷却水应从___________ (填“b”或“c”)接口进入。
(2)浓硫酸的作用是___________ 。
(3)本实验采用水浴加热,优点是___________ ;U形管中试剂为 ___________ ,其作用是___________ 。
(4)步骤Ⅱ:NaBH4的制备。在240℃条件下进行,硼酸三甲酯[B(OCH3)3]与NaH反应制取NaBH4,同时生成CH3ONa,写出该反应的化学方程式___________ 。
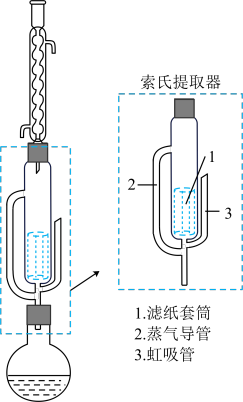
(5)已知:NaBH4可溶于异丙胺(熔点:-101℃,沸点:33℃),甲醇钠不溶于异丙胺。步骤Ⅲ中萃取时可采用索氏提取法,其装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现连续萃取。当萃取完全后,硼氢化钠在___________ (填“圆底烧瓶”或“索氏提取器”)中。
(6)分离NaBH4并回收溶剂,采用的方法是___________ 。

步骤Ⅰ:硼酸三甲酯[B(OCH3)3]的制备(已知硼酸三甲酯能水解)。将硼酸(H3BO3)和适量甲醇加入圆底烧瓶中,然后缓慢地加入浓硫酸,振荡,在烧瓶上加装分馏柱a,用电炉经水浴锅加热,回流2小时,收集硼酸三甲酯与甲醇共沸液。装置如图所示(夹持装置略去,下同)。

(1)直形冷凝管冷却水应从
(2)浓硫酸的作用是
(3)本实验采用水浴加热,优点是
(4)步骤Ⅱ:NaBH4的制备。在240℃条件下进行,硼酸三甲酯[B(OCH3)3]与NaH反应制取NaBH4,同时生成CH3ONa,写出该反应的化学方程式
(5)已知:NaBH4可溶于异丙胺(熔点:-101℃,沸点:33℃),甲醇钠不溶于异丙胺。步骤Ⅲ中萃取时可采用索氏提取法,其装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现连续萃取。当萃取完全后,硼氢化钠在

(6)分离NaBH4并回收溶剂,采用的方法是
您最近一年使用:0次



