某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
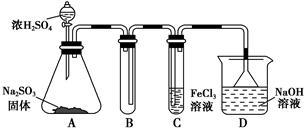
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在________ 中,再加水稀释,这样操作的目的是________ ,操作中不需要的仪器有________ (填入正确选项前的字母)。
a.药匙 b.烧杯 c.石棉网 d.玻璃棒 e.坩埚
(2)通入足量SO2时,C中观察到的现象为______________________________ 。
(3)根据以上现象,该小组同学认为SO2与FeCl3溶液发生了氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:___________________________ ;
②请设计实验方案检验有Fe2+生成:__________________________________ ;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法________ (填“合理”或“不合理”),理由是_______________________________________________________________ 。
(4)D装置中倒置漏斗的作用是______________________________________ 。
(5)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有________ (填入正确选项前的字母)。
a.浓H2SO4b.酸性KMnO4溶液
c.碘水 d.NaCl溶液

(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在
a.药匙 b.烧杯 c.石棉网 d.玻璃棒 e.坩埚
(2)通入足量SO2时,C中观察到的现象为
(3)根据以上现象,该小组同学认为SO2与FeCl3溶液发生了氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:
②请设计实验方案检验有Fe2+生成:
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法
(4)D装置中倒置漏斗的作用是
(5)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有
a.浓H2SO4b.酸性KMnO4溶液
c.碘水 d.NaCl溶液
2014高三·全国·专题练习 查看更多[5]
内蒙古自治区呼和浩特市和林格尔县第一中学2018-2019学年高二上学期第一次月考化学试题陕西省渭南韩城市2019-2020学年高二上学期竞赛考试化学试题2020届高三化学总复习考点强化练习:非金属及其化合物甘肃省天水市甘谷第一中学2020届高三上学期第四次检测考试化学试题(已下线)2014年高中化学二轮创新训练上 专题13化学实验综合应用练习卷
更新时间:2016-12-09 05:26:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
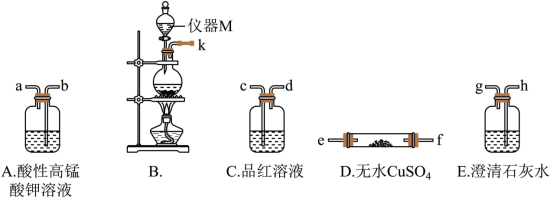
【推荐1】浓硫酸与木炭在加热条件下可发生化学反应,为了检验反应产物,某同学选用了如下图所示的实验装置进行实验,回答下列问题:___________ 。
(2)为验证反应产物,将混合气体依次通过上述仪器(可重复使用),装置接口的连接顺序是:k→________ →c→d→h。
(3)装置D中观察到的现象是___________ ,证明产物中有___________ 。
(4)当出现___________ 现象时,证明产物中有二氧化碳。
(5)装置A的作用是___________ ,反应的离子方程式为___________ 。
(6)在不影响实验检验结果的情况下,理论上可以用___________ 试剂代替A中的酸性KMnO4溶液。
(2)为验证反应产物,将混合气体依次通过上述仪器(可重复使用),装置接口的连接顺序是:k→
(3)装置D中观察到的现象是
(4)当出现
(5)装置A的作用是
(6)在不影响实验检验结果的情况下,理论上可以用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】二氯亚砜 (SOCl2) 是一种无色易挥发液体,剧烈水解生成两种气体,常用作脱水剂,其熔点-105℃,沸点79℃,140℃以上时易分解。
(1)用硫黄(S)、液氯和三氧化硫为原料在一定条件合成二氯亚砜,原子利用率达 100%,则三者的物质的量比为______________ .
(2)甲同学设计如图装置用 ZnCl2 • xH2O 晶体制取无水ZnCl2,回收剩余的SOCl2 并利用装置F验证生成物中的某种气体(夹持及加热装置略)。
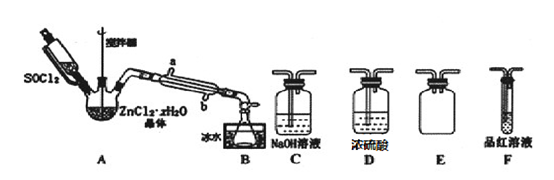
①用原理解释SOCl2在该实验中的作用______________________________________ ;加热条件下,A装置中总的化学方程式为____________________ .
②装置的连接顺序为A→B→_____________________ ;
③实验结束后,为检测 ZnCl2 • xH2O晶体是否完全脱水,甲同学设计实验方案如下,正确的实验顺序为_____________ (填序号)
a.加入足量硝酸酸化的硝酸银溶液,充分反应; b.称得固体为n克; c.干燥;d.称取蒸干后的固体m克溶于水;e.过滤;f.洗涤
若m/n=______________ (保留小数点后一位),即可证明晶体已完全脱水.
(3)乙同学认为SOCl2还可用作由FeCl3 • 6H2O制取无水FeCl3 的脱水剂,但丙同学认为该实验可能发生副反应使最后的产品不纯。
①可能发生的副反应的离子方程式______________________ .
②丙同学设计了如下实验方案判断副反应的可能性:
i.取少量FeCl3 • 6H2O于试管中,加入足量SOCl2,振荡使两种物质充分反应;
ii.往上述试管中加水溶解,取溶解后的溶液少许于两支试管,进行实验验证,完成表格内容。
(供选试剂:AgNO3溶液、稀盐酸、稀HNO3、酸性KMnO4溶液、BaCl2溶液、K3[Fe(CN)6]溶液、溴水)
(1)用硫黄(S)、液氯和三氧化硫为原料在一定条件合成二氯亚砜,原子利用率达 100%,则三者的物质的量比为
(2)甲同学设计如图装置用 ZnCl2 • xH2O 晶体制取无水ZnCl2,回收剩余的SOCl2 并利用装置F验证生成物中的某种气体(夹持及加热装置略)。

①用原理解释SOCl2在该实验中的作用
②装置的连接顺序为A→B→
③实验结束后,为检测 ZnCl2 • xH2O晶体是否完全脱水,甲同学设计实验方案如下,正确的实验顺序为
a.加入足量硝酸酸化的硝酸银溶液,充分反应; b.称得固体为n克; c.干燥;d.称取蒸干后的固体m克溶于水;e.过滤;f.洗涤
若m/n=
(3)乙同学认为SOCl2还可用作由FeCl3 • 6H2O制取无水FeCl3 的脱水剂,但丙同学认为该实验可能发生副反应使最后的产品不纯。
①可能发生的副反应的离子方程式
②丙同学设计了如下实验方案判断副反应的可能性:
i.取少量FeCl3 • 6H2O于试管中,加入足量SOCl2,振荡使两种物质充分反应;
ii.往上述试管中加水溶解,取溶解后的溶液少许于两支试管,进行实验验证,完成表格内容。
(供选试剂:AgNO3溶液、稀盐酸、稀HNO3、酸性KMnO4溶液、BaCl2溶液、K3[Fe(CN)6]溶液、溴水)
| 方案 | 操作 | 现象 | 结论 |
| 方案一 | 往一支试管中滴加 | 若有白色沉淀生成 | 则发生了上述副反应 |
| 方案二 | 往另一支试管中滴加 | 则没有发生上述副反应 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
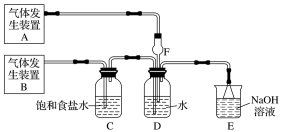
【推荐3】为了探究Cl2、SO2同时通入H2O发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
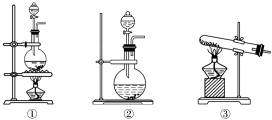
试填空:
(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12 mol·L-1)为原料制取Cl2。在此实验中,F仪器的作用是___ ;气体发生装置B应选择①、②、③三种装置中的_______ (选填序号)。
(2)D装置中主要反应的离子方程式为:_______ 。
(3)为验证通入D装置中气体是Cl2过量还是SO2过量,兴趣小组的同!学准备了以下试剂:氯化铁溶液;氯化亚铁溶液;硫氰化钾溶液;苯酚溶液;品红溶液;酸性高锰酸钾溶液。
若Cl2量:取适量D中溶液滴加至盛有___ (试剂名称,下同)的试管中,再加入产生的现象是_______ ,说明Cl2过量;若SO2过量:取适量D中溶液滴加至盛有______ 的试管内,产生的现象是______ 。


试填空:
(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12 mol·L-1)为原料制取Cl2。在此实验中,F仪器的作用是
(2)D装置中主要反应的离子方程式为:
(3)为验证通入D装置中气体是Cl2过量还是SO2过量,兴趣小组的同!学准备了以下试剂:氯化铁溶液;氯化亚铁溶液;硫氰化钾溶液;苯酚溶液;品红溶液;酸性高锰酸钾溶液。
若Cl2量:取适量D中溶液滴加至盛有
您最近一年使用:0次
【推荐1】某研究小组验证乙醇的还原性,装置如图所示。
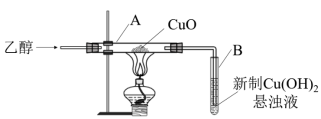
(1)乙醇被氧化的产物为_____ ,1mol乙醇失去_____ mol电子。
(2)通入乙醇反应,试管A的现象是_____ 。
(3)反应结束后,如果对试管B加热至沸腾,将会出现的现象是_____ 。

(1)乙醇被氧化的产物为
(2)通入乙醇反应,试管A的现象是
(3)反应结束后,如果对试管B加热至沸腾,将会出现的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学在实验室进行铁盐与亚铁盐相互转化实验。
实验I:将Fe3+转化为Fe2+

(1)Fe3+与Cu粉发生反应的离子方程式为__ 。
(2)探究白色沉淀产生的原因,请填写实验方案:__ 、__ 。

查阅资料:
已知:①SCN-的化学性质与I-相似。
②2Cu2++4I-=2CuI↓十I2。
则Cu2+与SCN-反应的离子方程式为__ 。
实验II:将Fe2+转化为Fe3+
探究上述现象出现的原因:
查阅资料:Fe2++NO Fe(NO)2+(棕色)
Fe(NO)2+(棕色)
(3)用离子方程式解释NO产生的原因:__ 。
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应I:Fe2+与HNO3反应,
反应II:Fe2+与NO反应。
①依据实验现象,可推知反应I的速率比反应II__ (填“快"或“慢”)。
②反应I是一个不可逆反应,设计实验方案加以证明___ 。
③请用化学平衡移动原理解释溶液由棕色变为黄色的原因:___ 。
实验I:将Fe3+转化为Fe2+

(1)Fe3+与Cu粉发生反应的离子方程式为
(2)探究白色沉淀产生的原因,请填写实验方案:

查阅资料:
已知:①SCN-的化学性质与I-相似。
②2Cu2++4I-=2CuI↓十I2。
则Cu2+与SCN-反应的离子方程式为
实验II:将Fe2+转化为Fe3+
探究上述现象出现的原因:
查阅资料:Fe2++NO
 Fe(NO)2+(棕色)
Fe(NO)2+(棕色)(3)用离子方程式解释NO产生的原因:
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应I:Fe2+与HNO3反应,
反应II:Fe2+与NO反应。
①依据实验现象,可推知反应I的速率比反应II
②反应I是一个不可逆反应,设计实验方案加以证明
③请用化学平衡移动原理解释溶液由棕色变为黄色的原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】利用淀粉可实现下列转化,请回答下列问题:
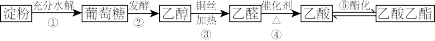
(1)某化学课外活动小组为探究反应③并验证产物,设计甲、乙两套装置图中的夹持仪器均未画出,“△”表示酒精灯热源,每套装置又可划分为Ⅰ、Ⅱ、Ⅲ三部分。仪器中盛放的试剂a为无水乙醇(沸点:78℃);b为铜丝;c为无水硫酸铜;d为新制氢氧化铜悬浊液(已知乙醛与新制氢氧化铜悬浊液加热有明显现象)。
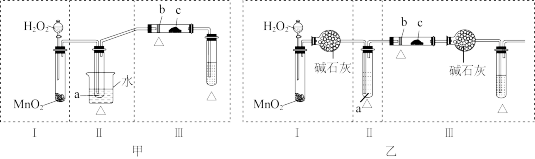
①对比两种方案,简述甲方案的优点:_______ 。
②集中两种方案的优点,组成一套完善合理的方案。按照气流从左至右的顺序为_______ (填写方式如:甲Ⅰ、乙Ⅱ等)。
(2)改进方案后进行该实验。实验过程中通入氧气的速率与反应体系的温度关系曲线如图所示,鼓气速率过快,反应体系温度反而下降的原因是_______ ,为解决该问题可采取的操作是_______ 。

(3)如果用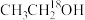 实现反应⑤,写出反应的化学方程式:
实现反应⑤,写出反应的化学方程式:_______ 。
实验室欲从乙酸乙酯、乙酸、乙醇的混合物得到乙酸乙酯,分离流程如下:
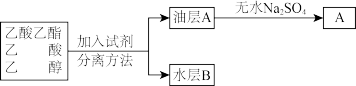
(4)则加入的试剂是_______ ,无水 的作用是
的作用是_______ 。
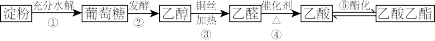
(1)某化学课外活动小组为探究反应③并验证产物,设计甲、乙两套装置图中的夹持仪器均未画出,“△”表示酒精灯热源,每套装置又可划分为Ⅰ、Ⅱ、Ⅲ三部分。仪器中盛放的试剂a为无水乙醇(沸点:78℃);b为铜丝;c为无水硫酸铜;d为新制氢氧化铜悬浊液(已知乙醛与新制氢氧化铜悬浊液加热有明显现象)。

①对比两种方案,简述甲方案的优点:
②集中两种方案的优点,组成一套完善合理的方案。按照气流从左至右的顺序为
(2)改进方案后进行该实验。实验过程中通入氧气的速率与反应体系的温度关系曲线如图所示,鼓气速率过快,反应体系温度反而下降的原因是

(3)如果用
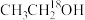 实现反应⑤,写出反应的化学方程式:
实现反应⑤,写出反应的化学方程式:实验室欲从乙酸乙酯、乙酸、乙醇的混合物得到乙酸乙酯,分离流程如下:

(4)则加入的试剂是
 的作用是
的作用是
您最近一年使用:0次



