为防止废弃的硒单质(Se)造成环境污染,通常用浓硫酸将其转化成二氧化硒(SeO2),再用KI溶液处理后回收Se。发生的反应为:① ;②
;②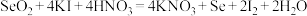 。下列说法错误的是
。下列说法错误的是
 ;②
;②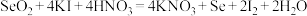 。下列说法错误的是
。下列说法错误的是| A.①中SO2是还原产物,SeO2是氧化产物 |
| B.②中HNO3既不是氧化剂也不是还原剂 |
| C.②中每生成0.2molI2共转移0.4mol电子 |
| D.氧化性由强到弱的顺序是:H2SO4(浓)<SeO2<I2 |
更新时间:2023-06-08 16:35:27
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列化学反应中硫元素仅被氧化的是
| A.3S+6KOH=K2SO3+2K2S+3H2O |
| B.Br2+SO2+2H2O=2HBr+H2SO4 |
| C.2FeS+6H2SO4(浓)=Fe2(SO4)3+3SO2↑+2S↓+6H2O |
| D.H2SO4+Na2SO3=SO2↑+Na2SO4+H2O |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】电子工业常用30%的 溶液腐蚀绝缘板上的铜箔,制作印刷电路板,下列说法正确的是
溶液腐蚀绝缘板上的铜箔,制作印刷电路板,下列说法正确的是
 溶液腐蚀绝缘板上的铜箔,制作印刷电路板,下列说法正确的是
溶液腐蚀绝缘板上的铜箔,制作印刷电路板,下列说法正确的是| A.可用置换法回收废液中的铜 |
B.用 溶液可检验废液中的 溶液可检验废液中的 |
C. 能溶解Cu说明Cu的金属性比Fe强 能溶解Cu说明Cu的金属性比Fe强 |
| D.该反应为复分解反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】设计如下实验验证氧化性: 。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)
。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)
下列说法错误的是
 。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)
。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)| 实验① | 实验② | 实验③ | 实验④ |
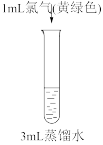 | 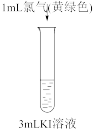 | 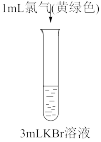 | 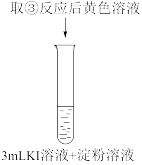 |
| 溶液变为浅黄绿色 | 溶液变为棕黄色 | 溶液变为黄色 | 溶液变为蓝色 |
A.实验①中发生反应: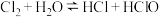 |
B.实验①②的现象可以证明氧化性: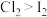 |
C.实验③发生反应: |
D.实验③④能证明氧化性: |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】KSCN 是高中阶段检验 Fe3+的常用试剂,下列实验操作和现象所得到的结论正确的是
| 选项 | 操作 | 现象 | 解释、结论 |
A | 过量的Fe粉与氯气充分反应后,向反应后的混合物中加水,取上层清液滴入KSCN溶液 | 溶液不变红色 | 氯气将Fe氧化为Fe2+ |
B | 向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液 | 溶液变为红色 | X 溶液中一定含有 Fe2+ |
| C | 将硝酸亚铁溶于稀硫酸,滴加KSCN溶液 | 溶液变为红色 | 硝酸亚铁已氧化变质 |
D | 取一定量 FeBr2溶液于试管中,滴加少量新制氯水,再加入少量KSCN溶液 | 溶液变为红色 | Fe2+的还原性强于 Br- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】已知Co2O3可代替MnO2制备Cl2,Co2O3+6HCl=2CoCl2+Cl2↑+3H2O,下列叙述不正确的是( )
| A.该反应中氧化性:Co2O3>Cl2 |
B.参加反应的HCl中,做还原剂的物质的量占总量的 |
| C.每生成1 mol氯气,消耗1 mol Co2O3 |
| D.制备相同量的氯气时,Co2O3得电子数比MnO2少 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】NaBH4(B的化合价为+3)是化工生产中的重要还原剂,其与水发生反应的化学方程式为NaBH4+2H2O=NaBO2+ 4H2↑。下列有关该反应的叙述正确的是
| A.NaBH4被还原 | B.每生成1个H2转移1个电子 |
| C.H2O发生氧化反应 | D.NaBO2是还原产物 |
您最近一年使用:0次



