如图为元素周期表的一部分,图中所列字母分别代表一种化学元素。

(1)元素b、c、e形成的常见稳定单质中最易与H2化合的是___________ (填化学式)。
(2)元素d、c所形成的某化合物的摩尔质量为78g/mol,该化合物的化学式为___________ ,其中所含化学键的类型有___________ 。
(3)推测原子序数为35的元素在元素周期表中的位置是___________ 。
(4)依据元素周期律推测,元素f的单质及其化合物的性质正确的是___________(填字母)。
(5)含有非极性键的c的氢化物,其电子式为___________ 。(ab)2称为拟卤素,性质与卤素单质相似,常温下其与NaOH溶液反应的化学方程式为___________ 。

(1)元素b、c、e形成的常见稳定单质中最易与H2化合的是
(2)元素d、c所形成的某化合物的摩尔质量为78g/mol,该化合物的化学式为
(3)推测原子序数为35的元素在元素周期表中的位置是
(4)依据元素周期律推测,元素f的单质及其化合物的性质正确的是___________(填字母)。
| A.f的单质常温下呈气态 | B.f的单质具有强氧化性 |
| C.fc2属于酸性氧化物 | D.fc2既有氧化性又有还原性 |
更新时间:2023-07-17 21:09:55
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。(用元素符号填空)

(1)写出元素F在周期表中的位置___________ 。
(2)写出工业制取单质C的化学方程式___________ 。
(3)G﹑H﹑B三种元素简单离子的半径由小到大排序___________ 。
(4)元素B和D的最高价氧化物对应的水化物相互反应的离子方程式为:___________ 。
(5)用电子式表示化合物A2G的形成过程的过程:___________ ,该化合物的水溶液呈___________ (填“酸”、“碱”或“中”)性,原因___________ (用离子方程式说明)
(6)元素F、G形成的简单氢化物中,熔沸点更高的是___________ ,原因是___________ 。
(7)E的简单氢化物构成燃料电池,采用铂作电极材料,稀硫酸作电解质溶液,写出负极的电极反应式___________ 。

(1)写出元素F在周期表中的位置
(2)写出工业制取单质C的化学方程式
(3)G﹑H﹑B三种元素简单离子的半径由小到大排序
(4)元素B和D的最高价氧化物对应的水化物相互反应的离子方程式为:
(5)用电子式表示化合物A2G的形成过程的过程:
(6)元素F、G形成的简单氢化物中,熔沸点更高的是
(7)E的简单氢化物构成燃料电池,采用铂作电极材料,稀硫酸作电解质溶液,写出负极的电极反应式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C为短周期元素,在周期表中所处的位置如图所示。
A、C两元素的原子核外电子数之和等于B原子的质子数。
(1)写出A、B元素的名称_________ 、______ 。
(2)B位于元素周期表中第________ 周期第_____ 族。
(3)C的原子结构示意图为____________________ 。
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式____________ 。
| A | C | |
| B |
A、C两元素的原子核外电子数之和等于B原子的质子数。
(1)写出A、B元素的名称
(2)B位于元素周期表中第
(3)C的原子结构示意图为
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】表格是元素周期表的一部分。请按要求回答下列问题:
(1)③对应的元素符号是_____ 。⑥元素在周期表中的位置是_____ 。
(2)上述所列元素最高价氧化物对应水化物酸性最强的是_____ (填化学式)。
(3)下列说法不正确的是_____ 。
(4)写出由上述所列元素形成的10电子分子的化学式_____ 。
(5)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式_____ 。
| IA | 0 | |||||||
| 1 | ④ | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑦ | |||||
| 4 | ② | ⑧ | ||||||
(2)上述所列元素最高价氧化物对应水化物酸性最强的是
(3)下列说法不正确的是
| A.元素最高正价与最低负价绝对值相等的元素一定处于第IVA族 |
| B.第5周期第VA族元素的原子序数为65 |
| C.⑥形成的最简单氢化物比⑤形成的最简单氢化物的稳定性高 |
| D.周期表中当某元素的周期序数大于其族序数时,该一定为金属元素 |
(5)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】五种短周期主族元素M、W、X、Y、Z的原子序数依次增大,M元素原子的最外层电子数是其电子层数的3倍;W是海水中的重要元素,原子结构示意图为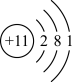 ;X的单质为金属,在空气中燃烧会发出耀眼的白光;Y是地壳中含量最高的金属元素;Z最高正价为+7。回答下列有关问题:
;X的单质为金属,在空气中燃烧会发出耀眼的白光;Y是地壳中含量最高的金属元素;Z最高正价为+7。回答下列有关问题:
(1)元素M在周期表中的位置是______ (指明周期与族),上述五种元素最高价氧化物对应的水化物中,酸性最强的酸是______ (填化学式)。
(2)W的单质着火时不能用水灭火,用化学反应方程式解释其原因____________ 。
(3)工业上可用X的单质与 加热还原出金属Ti,其反应方程式为
加热还原出金属Ti,其反应方程式为____________ 。
(4)门捷列夫曾预言过与Y同主族的“镓(Ga)”元素的存在,Ga与Y相邻。根据元素周期律推测,下列有关说法正确的是______(填字母代号)。
 ;X的单质为金属,在空气中燃烧会发出耀眼的白光;Y是地壳中含量最高的金属元素;Z最高正价为+7。回答下列有关问题:
;X的单质为金属,在空气中燃烧会发出耀眼的白光;Y是地壳中含量最高的金属元素;Z最高正价为+7。回答下列有关问题:(1)元素M在周期表中的位置是
(2)W的单质着火时不能用水灭火,用化学反应方程式解释其原因
(3)工业上可用X的单质与
 加热还原出金属Ti,其反应方程式为
加热还原出金属Ti,其反应方程式为(4)门捷列夫曾预言过与Y同主族的“镓(Ga)”元素的存在,Ga与Y相邻。根据元素周期律推测,下列有关说法正确的是______(填字母代号)。
| A.镓原子的最外层电子数为5 | B.镓的氧化物的化学式为 |
C.碱性强弱: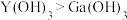 | D.单质Ga能与NaOH溶液反应产生 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了6种元素在周期表中的位置,其中①~③代表3种元素。
(1)①的元素符号是_______ 。
(2)下列能说明 比
比 失电子能力强的事实是
失电子能力强的事实是_______ (填字母)。
 比
比 更容易与水反应置换出氢
更容易与水反应置换出氢
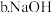 是强碱,
是强碱, 是中强碱
是中强碱
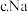 的密度比
的密度比 的小
的小
(3)非金属性②强于③,用原子结构解释原因:②和③位于同一主族,最外层电子数相同,_______ ,原子半径②小于③,得电子能力②强于③。
(4)依据元素周期律,预测气态氢化物的热稳定性: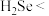
_______ (填写化学式,一种即可)。
| \ | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ||||||||
| 3 |  |  | ① | ② | ||||
| 4 |  | ③ |
(2)下列能说明
 比
比 失电子能力强的事实是
失电子能力强的事实是 比
比 更容易与水反应置换出氢
更容易与水反应置换出氢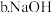 是强碱,
是强碱, 是中强碱
是中强碱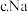 的密度比
的密度比 的小
的小(3)非金属性②强于③,用原子结构解释原因:②和③位于同一主族,最外层电子数相同,
(4)依据元素周期律,预测气态氢化物的热稳定性:
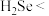
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】元素周期律是指导我们学习元素及其化合物知识的重要工具。氧族元素(不含Po)的部分知识如表所示。
请总结表中规律,并依据元素周期律回答下列问题;
(1)写出硒原子的结构示意图:_______ 。
(2)硒单质的沸点T的范围是_______ ;元素碲的最高化合价为_______ 。
(3)硫、硒、碲的最高价氧化物对应水化物的酸性由弱至强的顺序是_______ (填元素符号)。
(4)氧、硫、硒、碲的单质与氢气反应由易到难的顺序为_______ (填元素符号)。
(5)氢硒酸长期露置在空气中易变质,可能发生反应的化学方程式为_______ 。
| 元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点/°C | -218.4 | 113 | 217 | 450 |
| 单质沸点/°C | -183 | 444.6 | 1390 | |
| 元素主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 |  | |||
(1)写出硒原子的结构示意图:
(2)硒单质的沸点T的范围是
(3)硫、硒、碲的最高价氧化物对应水化物的酸性由弱至强的顺序是
(4)氧、硫、硒、碲的单质与氢气反应由易到难的顺序为
(5)氢硒酸长期露置在空气中易变质,可能发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有部分短周期元素的性质或原子结构如下表:
(1)A的气态氢化物的化学式是___________ ,元素B(含8个中子)的一种同位素可测定文物年代,这种同位素的符号是___________ 。
(2)写出元素F的离子结构示意图___________ 。
(3)写出G元素最高价氧化物对应的水化物的化学式是___________ 。
(4)元素D与元素A相比,非金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ 。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与氢氧化钠溶液反应
(5)F的阴离子和G的阳离子的半径大小比较:___________ (用离子符号表示)
(6)A、D的简单离子的还原性强弱:___________ (用离子符号表示)
| 元素编号 | 元素性质或原子结构 |
| A | 室温下其单质呈粉末状黄色固体,加热易熔化。该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | 最外层电子数比次外层电子数多3个 |
| D | 元素最高正价是+7价 |
| E | 主族元素中得电子能力最强 |
| F | 空气的主要成分之一,其某种同素异形体是保护地球地表环境的重要屏障 |
| G | 第3周期元素的简单离子中半径最小 |
(2)写出元素F的离子结构示意图
(3)写出G元素最高价氧化物对应的水化物的化学式是
(4)元素D与元素A相比,非金属性较强的是
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与氢氧化钠溶液反应
(5)F的阴离子和G的阳离子的半径大小比较:
(6)A、D的简单离子的还原性强弱:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为元素周期表的一部分。
回答下列问题:
(1)X元素在周期表中的位置为__ 。
(2)NH3的电子式为__ 。
(3)下列事实能说明Y 元素的非金属性比S 元素的非金属性强的是__ 。
a.Y 单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y 单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)常温下,碳与镁形成的 1 mol 化合物Q 与水反应,生成2 mol Mg(OH)2和 1 mol 气态烃,该烃中碳氢质量比为 9:1。写出化合物Q 与水反应的化学方程式:__ 。
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)X元素在周期表中的位置为
(2)NH3的电子式为
(3)下列事实能说明Y 元素的非金属性比S 元素的非金属性强的是
a.Y 单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y 单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)常温下,碳与镁形成的 1 mol 化合物Q 与水反应,生成2 mol Mg(OH)2和 1 mol 气态烃,该烃中碳氢质量比为 9:1。写出化合物Q 与水反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】几种主族元素在周期表中的位置如图
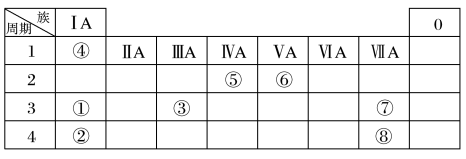
根据上表回答下列问题:
(1)写出⑤和⑧两种元素的名称:___________ 、___________ 。
(2)①和⑦两种元素的形成化合物的电子式是___________ 。
(3)①③⑦三种元素离子半径由大到小的顺序是___________ (用元素符号表示)。
(4)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为___________ ,该元素在周期表中的位置是 ___________ 。
(5)②与③最高价氧化物对应水化物反应的离子方程式为___________ 。
(6)⑦的非金属性强于⑧,下列表述中能证明这一事实的是___________ (填字母)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱

根据上表回答下列问题:
(1)写出⑤和⑧两种元素的名称:
(2)①和⑦两种元素的形成化合物的电子式是
(3)①③⑦三种元素离子半径由大到小的顺序是
(4)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(5)②与③最高价氧化物对应水化物反应的离子方程式为
(6)⑦的非金属性强于⑧,下列表述中能证明这一事实的是
a.⑦的氢化物比⑧的氢化物稳定
b.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知五种短周期元素的原子序数的大小顺序为C>A>B>D>E;其中E元素为原子半径最小的元素,且A、C同周期,B和C同主族;A与B可形成离子化合物A2B,其含有的离子具有相同的电子层结构,且电子总数为30;D和E可形成4核10电子分子,该分子可使湿润的红色石蕊试纸变蓝。试回答下列问题:
(1)C元素的元素符号为________ ;
(2)B、D元素的第一电离能大小关系为:B_____ D(填“<”、“>”或“=”);
(3)写出D元素形成的单质的结构式为______________ ,其中σ键:π键=______ 。
(4)A2B对应的水化物的碱性比LiOH_______ (填“强”或“弱”);化合物A2B2属于_______ (选“离子”或“共价”)化合物,写出A2B2的电子式_________________ ,A2B2溶于水时发生反应的化学方程式为__________________________________________________
(5)化合物E2B、E2C,它们结构与组成相似,热稳定性更强的是__________ (填化学式)
但E2B的沸点比E2C高得多的原因是___________________________________ 。
(1)C元素的元素符号为
(2)B、D元素的第一电离能大小关系为:B
(3)写出D元素形成的单质的结构式为
(4)A2B对应的水化物的碱性比LiOH
(5)化合物E2B、E2C,它们结构与组成相似,热稳定性更强的是
但E2B的沸点比E2C高得多的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)元素⑨单质的电子式_______ 。
(2)第三周期元素除⑩外原子半径最小的是_______ (填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是_______ (填化学式,下同),具有两性的是_______ 。
(3)第三周期元素中最高价氧化物对应水化物酸性最强的是_______ (填化学式)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)第三周期元素除⑩外原子半径最小的是
(3)第三周期元素中最高价氧化物对应水化物酸性最强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D为四种短周期元素,它们的原子序数依次增大,其中A与C、B与D分别是同主族元素;已知B、D两元素间可形成DB2和DB3两种化合物,两者相对分子质量相差16;又知A、C两元素原子序数之和是B、D两元素原子序数之和的 ,请回答下列问题:
,请回答下列问题:
(1)写出由A、B、C三种元素形成的化合物的电子式:__________________________ ,其晶体中所含化学键的类型有________________________________________________________ 。
(2)A2B的沸点比A2D的沸点(填“高”或“低”)________ ;其原因是_________________ 。
(3)由A、B、C、D四种元素形成的物质X,与盐酸反应能够生成具有刺激性气味的气体,写出X与盐酸反应的离子方程式:___________________________________________________ 。
 ,请回答下列问题:
,请回答下列问题:(1)写出由A、B、C三种元素形成的化合物的电子式:
(2)A2B的沸点比A2D的沸点(填“高”或“低”)
(3)由A、B、C、D四种元素形成的物质X,与盐酸反应能够生成具有刺激性气味的气体,写出X与盐酸反应的离子方程式:
您最近一年使用:0次



