甲酸 被认为是一种有前途的储氢化合物。在催化剂作用下,甲酸分解制氢的过程如图所示。
被认为是一种有前途的储氢化合物。在催化剂作用下,甲酸分解制氢的过程如图所示。
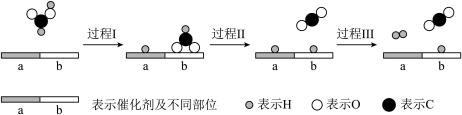
(1) 中官能团的名称是
中官能团的名称是_______ 。
(2)常压下甲酸的沸点是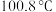 。甲酸沸腾的过程中,外界提供的能量的作用是
。甲酸沸腾的过程中,外界提供的能量的作用是_______ 。
(3)过程Ⅰ中断裂的化学键是_______ ,过程Ⅲ中形成的化学键是_______ 。
(4) 分解制氢的总反应方程式是
分解制氢的总反应方程式是_______ ,两种产物的电子式分别是_______ 、_______ 。
(5) 分解制氢是一个可逆反应。在密闭容器中,通入
分解制氢是一个可逆反应。在密闭容器中,通入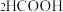 蒸汽,一段时间后,核素
蒸汽,一段时间后,核素 存在于以下分子中:
存在于以下分子中:_______ 。
 被认为是一种有前途的储氢化合物。在催化剂作用下,甲酸分解制氢的过程如图所示。
被认为是一种有前途的储氢化合物。在催化剂作用下,甲酸分解制氢的过程如图所示。
(1)
 中官能团的名称是
中官能团的名称是(2)常压下甲酸的沸点是
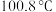 。甲酸沸腾的过程中,外界提供的能量的作用是
。甲酸沸腾的过程中,外界提供的能量的作用是(3)过程Ⅰ中断裂的化学键是
(4)
 分解制氢的总反应方程式是
分解制氢的总反应方程式是(5)
 分解制氢是一个可逆反应。在密闭容器中,通入
分解制氢是一个可逆反应。在密闭容器中,通入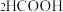 蒸汽,一段时间后,核素
蒸汽,一段时间后,核素 存在于以下分子中:
存在于以下分子中:
更新时间:2023-07-18 07:52:22
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】拟卤离子主要有 、
、 、
、 ,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。已知还原性:
,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。已知还原性: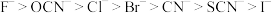 。
。
(1) 与水反应生成的含氧酸的结构式为
与水反应生成的含氧酸的结构式为___________ 。从原子结构角度分析在 中,元素C显正化合价的原因
中,元素C显正化合价的原因___________ 。
(2)调节电镀厂的电镀废液pH在8.5~9.4之间,再加入漂白粉可消除废液中有毒的 。将反应的离子方程式补充完整(漂白粉用
。将反应的离子方程式补充完整(漂白粉用 表示)
表示)___________ 。
________ _______
_______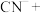 ________
________ ________
________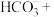 ________
________ ________
________
(3)常温下,将amol·L 的
的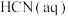 与bmol·L
与bmol·L 的
的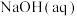 等体积混合,反应后溶液恰好呈中性,用含a、b的代数式表示
等体积混合,反应后溶液恰好呈中性,用含a、b的代数式表示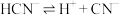 平衡常数
平衡常数
___________ ;向混合溶液中继续加入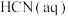 使溶液的
使溶液的 ,此时溶液中
,此时溶液中
___________ mol·L (填准确数值)。
(填准确数值)。
(4)写出酸性条件下, 和
和 反应的离子方程式
反应的离子方程式___________ 。
 、
、 、
、 ,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。已知还原性:
,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。已知还原性: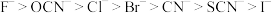 。
。(1)
 与水反应生成的含氧酸的结构式为
与水反应生成的含氧酸的结构式为 中,元素C显正化合价的原因
中,元素C显正化合价的原因(2)调节电镀厂的电镀废液pH在8.5~9.4之间,再加入漂白粉可消除废液中有毒的
 。将反应的离子方程式补充完整(漂白粉用
。将反应的离子方程式补充完整(漂白粉用 表示)
表示)________
 _______
_______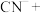 ________
________ ________
________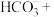 ________
________ ________
________(3)常温下,将amol·L
 的
的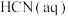 与bmol·L
与bmol·L 的
的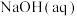 等体积混合,反应后溶液恰好呈中性,用含a、b的代数式表示
等体积混合,反应后溶液恰好呈中性,用含a、b的代数式表示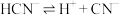 平衡常数
平衡常数
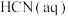 使溶液的
使溶液的 ,此时溶液中
,此时溶液中
 (填准确数值)。
(填准确数值)。(4)写出酸性条件下,
 和
和 反应的离子方程式
反应的离子方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】2015年8月12日晚,天津滨海新区某公司仓库发生爆炸,事发仓库里存放了大量的硝酸铵、氰化钠(NaCN)、金属钠等危险化学品。回答下列问题:
(1)NaCN的电子式为:_______________________ 。
(2)金属钠属于危化品中的易燃固体,其着火时不能用水灭火,请用化学方程式解释其原因:_____________________________ 。
(3)氰化钠是一种重要的化工原料,也是剧毒危险品,皮肤伤口接触、吸入、吞食微量可中毒死亡。氰化钠易溶于水,水溶液呈强碱性。氰化钠泄漏可用双氧水或硫代硫酸钠中和。
①用离子方程式表示氰化钠水溶液呈强碱性的原因:______________________________ 。
②用双氧水处理产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的化学方程式_____________________________ ;
③用硫代硫酸钠中和的离子方程式为CN-+ →A+
→A+ (已配平),A为
(已配平),A为_________ (填化学式)。
(4)CN-中C元素显+2价,N元素显﹣3价,则非金属性N_______ C(填<、=或>),请用简单的实验方法证明(要求说明简单操作、现象和结论):_______________________________________ 。
(5)0.4mol/L的NaCN和0.2mol/L的HCl等体积混合,溶液显碱性,其溶液中离子浓度大小排列顺序是_______________________________________
(1)NaCN的电子式为:
(2)金属钠属于危化品中的易燃固体,其着火时不能用水灭火,请用化学方程式解释其原因:
(3)氰化钠是一种重要的化工原料,也是剧毒危险品,皮肤伤口接触、吸入、吞食微量可中毒死亡。氰化钠易溶于水,水溶液呈强碱性。氰化钠泄漏可用双氧水或硫代硫酸钠中和。
①用离子方程式表示氰化钠水溶液呈强碱性的原因:
②用双氧水处理产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的化学方程式
③用硫代硫酸钠中和的离子方程式为CN-+
 →A+
→A+ (已配平),A为
(已配平),A为(4)CN-中C元素显+2价,N元素显﹣3价,则非金属性N
(5)0.4mol/L的NaCN和0.2mol/L的HCl等体积混合,溶液显碱性,其溶液中离子浓度大小排列顺序是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca,并含有3.5%(质量分数)CaO。
(1)Ca元素在周期表中位置是_________ ,其原子结构示意图_________ 。
(2)Ca与最活跃的非金属元素A形成化合物D,D的电子式为_________ 。
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则金属M为______ ;检测Mn+的方法是_______________________________________ (用离子方程式表达)。
(4)取1.6g钙线试样,与水充分反映,生成224ml.H2(标准状况),在想溶液中通入适量的CO2,最多能得到CaCO3_____________ g。
(1)Ca元素在周期表中位置是
(2)Ca与最活跃的非金属元素A形成化合物D,D的电子式为
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则金属M为
(4)取1.6g钙线试样,与水充分反映,生成224ml.H2(标准状况),在想溶液中通入适量的CO2,最多能得到CaCO3
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】按要求回答下列问题。
(1)某烷烃的蒸气密度是同温同压下氢气密度的64倍,该烷烃核磁共振氢谱有2组峰且峰面积之比为2∶3,写出这种烷烃的结构简式___________ 。若该烷烃为炔烃加氢制得,则此炔烃的结构可能有___________ 种。
(2)有机物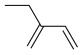 的名称为
的名称为___________ ,其与 按物质的量之比1∶1加成时,所得产物有
按物质的量之比1∶1加成时,所得产物有___________ 种。
(3)分子式为 属于芳香烃的同分异构体共有
属于芳香烃的同分异构体共有___________ 种,其中___________ (填结构简式)的一溴代物只有两种。
(4)有机物A的结构简式为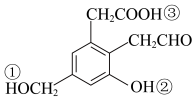 若取等质量的A分别与足量的Na、NaOH、
若取等质量的A分别与足量的Na、NaOH、 充分反应,理论上消耗这三种物质的物质的量之比为
充分反应,理论上消耗这三种物质的物质的量之比为___________ ,有机物A中标有序号①、②、③处羟基上氢原子的活泼性由强到弱顺序为___________ (用序号表示)。
(5)新制氢氧化铜悬浊液能够检测出丙醛中含有醛基,写出丙醛与新制氢氧化铜悬浊液反应的化学方程式___________ 。
(1)某烷烃的蒸气密度是同温同压下氢气密度的64倍,该烷烃核磁共振氢谱有2组峰且峰面积之比为2∶3,写出这种烷烃的结构简式
(2)有机物
 的名称为
的名称为 按物质的量之比1∶1加成时,所得产物有
按物质的量之比1∶1加成时,所得产物有(3)分子式为
 属于芳香烃的同分异构体共有
属于芳香烃的同分异构体共有(4)有机物A的结构简式为
 若取等质量的A分别与足量的Na、NaOH、
若取等质量的A分别与足量的Na、NaOH、 充分反应,理论上消耗这三种物质的物质的量之比为
充分反应,理论上消耗这三种物质的物质的量之比为(5)新制氢氧化铜悬浊液能够检测出丙醛中含有醛基,写出丙醛与新制氢氧化铜悬浊液反应的化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】根据抑制癌细胞增殖药物的恩杂鲁胺 的两条合成路线,回答下列问题。
的两条合成路线,回答下列问题。
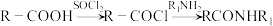 ;
;②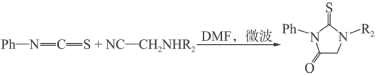 。
。
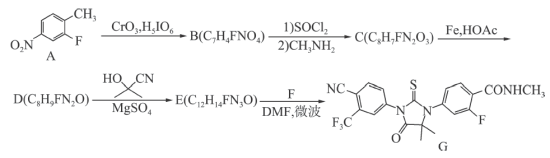
(2)
 反应的化学方程式为
反应的化学方程式为路线二:
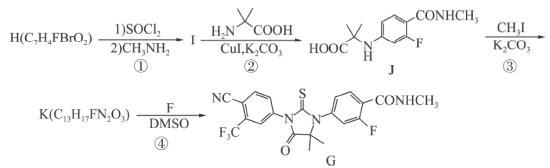
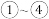 中仅发生取代反应的是
中仅发生取代反应的是
您最近一年使用:0次
【推荐3】根据要求填空:
(1)只用键线来表示碳架,两根单键之间或一根双键和一根单键之间的夹角为120˚,一根单键和一根三键之间的夹角为180˚,而分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略,而其他杂原子及与杂原子相连的氢原子须保留。每个端点和拐角处都代表一个碳。用这种方式表示的结构式为键线式。写出下列有机物的键线式:
①CH3(CH2)2COOH______ ;
②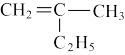 :
:______ 。
(2)写出下列原子团的电子式:
①甲基______ ;
②氢氧根离子______
(3)写出有机物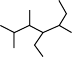 的名称
的名称 ______
(4)在有机物分子中若某一个碳原子连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”。C7H16的同分异构体中具有“手性碳原子”的有______ 种。
(5)某有机高分子化合物的结构片段如下:
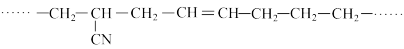
则合成它的单体是______ 。
(1)只用键线来表示碳架,两根单键之间或一根双键和一根单键之间的夹角为120˚,一根单键和一根三键之间的夹角为180˚,而分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略,而其他杂原子及与杂原子相连的氢原子须保留。每个端点和拐角处都代表一个碳。用这种方式表示的结构式为键线式。写出下列有机物的键线式:
①CH3(CH2)2COOH
②
 :
:(2)写出下列原子团的电子式:
①甲基
②氢氧根离子
(3)写出有机物
 的名称
的名称 (4)在有机物分子中若某一个碳原子连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”。C7H16的同分异构体中具有“手性碳原子”的有
(5)某有机高分子化合物的结构片段如下:
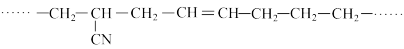
则合成它的单体是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】(1)用电子式表示下列物质的形成过程:
①Na2S_________________ ; ②H2O________________
(2)写出下列物质的电子式:
③ KOH__________ ④CO2_______________ 。
(3)下列物质:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩HBr。回答下列问题:(填序号)
只含极性键的是_______ ;含有极性键和非极性键的是_______ ;含有非极性键的离子化合物是_____ 。
①Na2S
(2)写出下列物质的电子式:
③ KOH
(3)下列物质:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩HBr。回答下列问题:(填序号)
只含极性键的是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】Ⅰ.用化学用语回答下列问题:
(1)写出二氧化碳分子的电子式:___________ ;
(2)写出氮气分子的结构式___________ 。
Ⅱ.下列物质:① N2 ② CO2 ③ NH3 ④ Na2O ⑤Na2O2 ⑥ NaOH ⑦ CaBr2 ⑧ H2O2 ⑨ NH4Cl ⑩ HBr。
(1)含有极性键和非极性键的是_______ ;
(2)含有非极性键的离子化合物是_____ 。(填序号,下同)
Ⅲ.下列变化中:① 干冰气化; ② 硝酸钾熔化; ③ KHSO4熔融; ④ 硫酸溶于水;
⑤ 蔗糖溶于水;⑥ HI分解; ⑦ 碘升华; ⑧ 溴蒸气被木炭吸附。
(1)未破坏化学键的是_____ ;
(2)仅离子键被破坏的是____ ;
(3)仅共价键被破坏的是____ 。
Ⅳ.下列物质:① 1H、2H、3H ; ② H2O、D2O、T2O; ③ O2、O3; ④ 14N、14C
(1)互为同位素的是:______ ;
(2)互为同素异形体的是:______ ;
(3)氢的三种原子1H、2H、3H 与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有________ 种。
(1)写出二氧化碳分子的电子式:
(2)写出氮气分子的结构式
Ⅱ.下列物质:① N2 ② CO2 ③ NH3 ④ Na2O ⑤Na2O2 ⑥ NaOH ⑦ CaBr2 ⑧ H2O2 ⑨ NH4Cl ⑩ HBr。
(1)含有极性键和非极性键的是
(2)含有非极性键的离子化合物是
Ⅲ.下列变化中:① 干冰气化; ② 硝酸钾熔化; ③ KHSO4熔融; ④ 硫酸溶于水;
⑤ 蔗糖溶于水;⑥ HI分解; ⑦ 碘升华; ⑧ 溴蒸气被木炭吸附。
(1)未破坏化学键的是
(2)仅离子键被破坏的是
(3)仅共价键被破坏的是
Ⅳ.下列物质:① 1H、2H、3H ; ② H2O、D2O、T2O; ③ O2、O3; ④ 14N、14C
(1)互为同位素的是:
(2)互为同素异形体的是:
(3)氢的三种原子1H、2H、3H 与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】H、C、N、C、Na、S、Fe是中学化学中常见的元素,请根据题意回答与这些元素有关的问题:
(1)Fe元素在元素周期表中的位置:___________________ ;
(2) 写出(CN)2的电子式:___________________ ;
(3)用电子式表示Na3N 的形成过程:___________________ ;
(4)各种氮氧化物(NO、NO2)是主要的大气污染物之一,治理氨氧化物(NOx)废气的方法之一是用NaOH溶液进行吸收,其反应原理可表示如下:
NO2 +NO+2NaOH=2NaNO2+H2O 2NO2 + 2NaOH =NaNO2+NaNO3+H2O
现有NO 与NO2的混合气体,将其通入50 mL 2 mol/L的NaOH 溶液中,恰好完全吸收,测得溶液中含有NO 0.02 mol,混合气体中v(NO): v(NO2)=
0.02 mol,混合气体中v(NO): v(NO2)=_________ ;
(5) 向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO 、Fe3+、Fe2+等粒子物质的量随n(Cl2)/n(FeI2 )的变化可用下图简单表示
、Fe3+、Fe2+等粒子物质的量随n(Cl2)/n(FeI2 )的变化可用下图简单表示
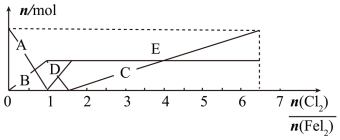
当n(Cl2)/n(FeI2 )=6.5 时,溶液中n(Cl-):n(IO )=
)=_________ ;
(1)Fe元素在元素周期表中的位置:
(2) 写出(CN)2的电子式:
(3)用电子式表示Na3N 的形成过程:
(4)各种氮氧化物(NO、NO2)是主要的大气污染物之一,治理氨氧化物(NOx)废气的方法之一是用NaOH溶液进行吸收,其反应原理可表示如下:
NO2 +NO+2NaOH=2NaNO2+H2O 2NO2 + 2NaOH =NaNO2+NaNO3+H2O
现有NO 与NO2的混合气体,将其通入50 mL 2 mol/L的NaOH 溶液中,恰好完全吸收,测得溶液中含有NO
 0.02 mol,混合气体中v(NO): v(NO2)=
0.02 mol,混合气体中v(NO): v(NO2)=(5) 向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO
 、Fe3+、Fe2+等粒子物质的量随n(Cl2)/n(FeI2 )的变化可用下图简单表示
、Fe3+、Fe2+等粒子物质的量随n(Cl2)/n(FeI2 )的变化可用下图简单表示
当n(Cl2)/n(FeI2 )=6.5 时,溶液中n(Cl-):n(IO
 )=
)=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】(1)X原子有两个电子层,它能与最活泼的金属Y形成 的化合物,X是
的化合物,X是_______ 元素(写元素符号)。
(2)6C元素能够与某非金属元素R形成化合物CRn,已知CRn分子中各原子核外最外层电子总数为32,核外电子数总和为74,则R是_______ 元素(写元素符号),n=_______ 。
(3)下表是元素周期表的一部分,回答有关问题:
①在这些元素中,最不活泼的元素的结构示意图是______________
②在这些元素的最高价氧化物对应的水化物中,酸性最强的与呈两性的发生反应的化学方程式为___________ ;碱性最强的与呈两性的发生反应的离子方程式__________
③元素(8)、(11)和氧元素形成一种广泛使用杀菌消毒剂,该物质中存在的化学键有___________
④用电子式表示由元素(8)和(10)形成化合物的过程:_________________
 的化合物,X是
的化合物,X是(2)6C元素能够与某非金属元素R形成化合物CRn,已知CRn分子中各原子核外最外层电子总数为32,核外电子数总和为74,则R是
(3)下表是元素周期表的一部分,回答有关问题:
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 | |
| 2 | (1) | (2) | ||||||
| 3 | (3) | (4) | (5) | (6) | (7) | (8) | (9) | |
| 4 | (10) | (11) | (12) |
①在这些元素中,最不活泼的元素的结构示意图是
②在这些元素的最高价氧化物对应的水化物中,酸性最强的与呈两性的发生反应的化学方程式为
③元素(8)、(11)和氧元素形成一种广泛使用杀菌消毒剂,该物质中存在的化学键有
④用电子式表示由元素(8)和(10)形成化合物的过程:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】碳的多种同素异形体及一系列化合物广泛应用于科研、医疗、工农业生产等领域。钴单质及其化合物在生产、生活中有广泛应用。回答下列问题:
(1)写出基态C原子核外电子排布的轨道表示式___________ 。
(2)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是___________(填编号)。
(3) 与光气
与光气 反应可用于制取四氯化钛。
反应可用于制取四氯化钛。 中
中 键和
键和 键的数目比为
键的数目比为___________ ,其空间构型为___________ 。
(4)基态Co原子的价层电子排布式为___________ 。
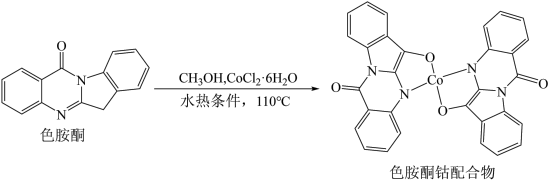
(5)以甲醇为溶剂, 可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示),色胺酮分子中所含元素(H、C、N、O)的电负性由大到小的顺序为
可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示),色胺酮分子中所含元素(H、C、N、O)的电负性由大到小的顺序为___________ (填元素符号),色胺酮分子中N原子的杂化类型有___________ ,X射线衍射分析显示色胺酮钴配合物晶胞中还含有一个 分子,
分子, 通过
通过___________ 作用与色胺酮钴配合物相结合。
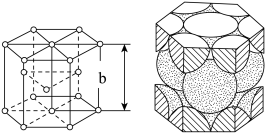
(6)金属钴晶体的晶胞呈六棱柱形,其结构如图所示,每个晶胞中含Co原子数为___________ ;晶胞底面呈正六边形,边长为apm,设 为阿伏加德罗常数的值,晶胞的密度
为阿伏加德罗常数的值,晶胞的密度 ,则该晶胞的高b为
,则该晶胞的高b为___________ pm(列出计算式)。

(1)写出基态C原子核外电子排布的轨道表示式
(2)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是___________(填编号)。
A. | B. | C. | D.苯 |
 与光气
与光气 反应可用于制取四氯化钛。
反应可用于制取四氯化钛。 中
中 键和
键和 键的数目比为
键的数目比为(4)基态Co原子的价层电子排布式为
(5)以甲醇为溶剂,
 可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示),色胺酮分子中所含元素(H、C、N、O)的电负性由大到小的顺序为
可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示),色胺酮分子中所含元素(H、C、N、O)的电负性由大到小的顺序为 分子,
分子, 通过
通过(6)金属钴晶体的晶胞呈六棱柱形,其结构如图所示,每个晶胞中含Co原子数为
 为阿伏加德罗常数的值,晶胞的密度
为阿伏加德罗常数的值,晶胞的密度 ,则该晶胞的高b为
,则该晶胞的高b为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】冰晶石是金属铝冶炼时的助溶剂,工业上制取冰晶石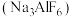 的化学方程式如下:
的化学方程式如下: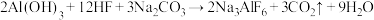 ;根据题意完成下列填空:
;根据题意完成下列填空:
(1)铝原子核外电子占据_______ 个轨道,最外层电子云伸展方向有_______ 种,某元素与铝元素不同周期但在相邻一族,且性质和铝元素十分相似,该元素原子核外电子排布式为_______ 。
(2)冰晶石中存在的化学键_______ ,在上述反应的反应物和生成物中,属于非极性分子的电子式_______ ,属于弱酸的电离方程式_______ 。
(3)金属铝冶炼时,使用助熔剂冰晶石,是因为原料 的高熔点,为什么原料不选用熔点更低的
的高熔点,为什么原料不选用熔点更低的 ?
?_______
(4)在电解法发明前,金属铝是用更活泼的金属通过置换反应来生产的,所以价格非常昂贵,为什么不使用相对廉价的碳或氢气进行置换呢?_______
(5)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是_______(选填编号)。
(6) 俗称纯碱,属于
俗称纯碱,属于_______ 晶体。工业上制取纯碱的原料是_______ 。
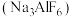 的化学方程式如下:
的化学方程式如下: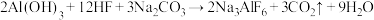 ;根据题意完成下列填空:
;根据题意完成下列填空:(1)铝原子核外电子占据
(2)冰晶石中存在的化学键
(3)金属铝冶炼时,使用助熔剂冰晶石,是因为原料
 的高熔点,为什么原料不选用熔点更低的
的高熔点,为什么原料不选用熔点更低的 ?
?(4)在电解法发明前,金属铝是用更活泼的金属通过置换反应来生产的,所以价格非常昂贵,为什么不使用相对廉价的碳或氢气进行置换呢?
(5)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是_______(选填编号)。
| A.气态氢化物的稳定性 | B.最高价氧化物对应水化物的酸性 |
| C.单质与氢气反应的难易 | D.单质与同浓度酸发生反应的快慢 |
 俗称纯碱,属于
俗称纯碱,属于
您最近一年使用:0次



