冰晶石是金属铝冶炼时的助溶剂,工业上制取冰晶石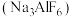 的化学方程式如下:
的化学方程式如下: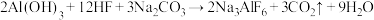 ;根据题意完成下列填空:
;根据题意完成下列填空:
(1)铝原子核外电子占据_______ 个轨道,最外层电子云伸展方向有_______ 种,某元素与铝元素不同周期但在相邻一族,且性质和铝元素十分相似,该元素原子核外电子排布式为_______ 。
(2)冰晶石中存在的化学键_______ ,在上述反应的反应物和生成物中,属于非极性分子的电子式_______ ,属于弱酸的电离方程式_______ 。
(3)金属铝冶炼时,使用助熔剂冰晶石,是因为原料 的高熔点,为什么原料不选用熔点更低的
的高熔点,为什么原料不选用熔点更低的 ?
?_______
(4)在电解法发明前,金属铝是用更活泼的金属通过置换反应来生产的,所以价格非常昂贵,为什么不使用相对廉价的碳或氢气进行置换呢?_______
(5)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是_______(选填编号)。
(6) 俗称纯碱,属于
俗称纯碱,属于_______ 晶体。工业上制取纯碱的原料是_______ 。
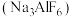 的化学方程式如下:
的化学方程式如下: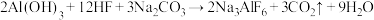 ;根据题意完成下列填空:
;根据题意完成下列填空:(1)铝原子核外电子占据
(2)冰晶石中存在的化学键
(3)金属铝冶炼时,使用助熔剂冰晶石,是因为原料
 的高熔点,为什么原料不选用熔点更低的
的高熔点,为什么原料不选用熔点更低的 ?
?(4)在电解法发明前,金属铝是用更活泼的金属通过置换反应来生产的,所以价格非常昂贵,为什么不使用相对廉价的碳或氢气进行置换呢?
(5)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是_______(选填编号)。
| A.气态氢化物的稳定性 | B.最高价氧化物对应水化物的酸性 |
| C.单质与氢气反应的难易 | D.单质与同浓度酸发生反应的快慢 |
 俗称纯碱,属于
俗称纯碱,属于
更新时间:2022-03-08 16:53:45
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】硫是一种典型的非金属元素,请回答下列问题:
(1)硫元素的非金属性___________ 氯元素(填“大于”或“小于”),请用一个事实来说明_______________________ 。
(2)氧硫化碳(COS)可作储粮杀虫剂,已知COS与CO2的结构相似,试写出COS的电子式______ ,COS属于_______ 分子(填“极性”或“非极性”)。COS的沸点___________ CO2的沸点(填“大于”或“小于”),并说出理由_______________________ 。
(3)冷的浓硫酸可以用铁制容器储存,是因为铁在冷的浓硫酸中发生了_______________ 现象。但是在加热条件下,浓硫酸还是可以和铁反应的。
①写出铁在加热条件下和足量浓硫酸反应的化学方程式,并标出电子转移方向与数目_____________________ 。
②上述反应中________ 元素被还原,还原产物是_________________________ 。
(1)硫元素的非金属性
(2)氧硫化碳(COS)可作储粮杀虫剂,已知COS与CO2的结构相似,试写出COS的电子式
(3)冷的浓硫酸可以用铁制容器储存,是因为铁在冷的浓硫酸中发生了
①写出铁在加热条件下和足量浓硫酸反应的化学方程式,并标出电子转移方向与数目
②上述反应中
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
I.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
_________ 与盐酸反应最剧烈;________ 与盐酸反应的速度最慢;_________ 与盐酸反应产生的气体最多。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由___________ 。
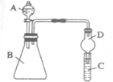
II. 利用如图装置可验证同主族元素非金属性的变化规律。
(3)仪器B的名称为________ ,干燥管D的作用为_______ 。
(4)若要证明非金属性Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液________ (填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用_______ 溶液吸收尾气。
(5)若要证明非金属性C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液_____ (填现象),即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有________ 溶液的洗气瓶除去。
I.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由
II. 利用如图装置可验证同主族元素非金属性的变化规律。
(3)仪器B的名称为
(4)若要证明非金属性Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
(5)若要证明非金属性C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】镍在金属羰基化合物(金属元素和CO中性分子形成的一类配合物)、金属储氢材料(能可逆地多次吸收、储存和释放H2的合金)等领域用途广泛。
(1)基态Ni原子核外电子排布式为__________________________ 。
(2)Ni(CO)4中镍元素的化合价为__________ ,写出与CO互为等电子体的带一个单位正电荷的阳离子为:_______ 。Ni(CO)4的一氯代物有2种,其空间构型为_______________ o
(3)一种储氢合金由镍与镧(La)组成,其晶胞结构如图所示,则该晶体的化学式为_____________

(4)下列反应常用来检验Ni2+,请写出另一产物的化学式:_______________ 。

与Ni2+配位的N原子有__________ 个,该配合物中存在的化学键有_________ (填序号)。
A.共价键 B.离子键 C.配位键 D.金属键 E.氢键
(5)Ni与Fe的构型相同(体心立方堆积),Ni的摩尔质量为M g/mol,阿伏伽德罗常数为NA,密度为a g/cm3Ni原子的半径为_________ pm(金属小球刚性相切)
(1)基态Ni原子核外电子排布式为
(2)Ni(CO)4中镍元素的化合价为
(3)一种储氢合金由镍与镧(La)组成,其晶胞结构如图所示,则该晶体的化学式为

(4)下列反应常用来检验Ni2+,请写出另一产物的化学式:

与Ni2+配位的N原子有
A.共价键 B.离子键 C.配位键 D.金属键 E.氢键
(5)Ni与Fe的构型相同(体心立方堆积),Ni的摩尔质量为M g/mol,阿伏伽德罗常数为NA,密度为a g/cm3Ni原子的半径为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】(1)X原子有两个电子层,它能与最活泼的金属Y形成 的化合物,X是
的化合物,X是_______ 元素(写元素符号)。
(2)6C元素能够与某非金属元素R形成化合物CRn,已知CRn分子中各原子核外最外层电子总数为32,核外电子数总和为74,则R是_______ 元素(写元素符号),n=_______ 。
(3)下表是元素周期表的一部分,回答有关问题:
①在这些元素中,最不活泼的元素的结构示意图是______________
②在这些元素的最高价氧化物对应的水化物中,酸性最强的与呈两性的发生反应的化学方程式为___________ ;碱性最强的与呈两性的发生反应的离子方程式__________
③元素(8)、(11)和氧元素形成一种广泛使用杀菌消毒剂,该物质中存在的化学键有___________
④用电子式表示由元素(8)和(10)形成化合物的过程:_________________
 的化合物,X是
的化合物,X是(2)6C元素能够与某非金属元素R形成化合物CRn,已知CRn分子中各原子核外最外层电子总数为32,核外电子数总和为74,则R是
(3)下表是元素周期表的一部分,回答有关问题:
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 | |
| 2 | (1) | (2) | ||||||
| 3 | (3) | (4) | (5) | (6) | (7) | (8) | (9) | |
| 4 | (10) | (11) | (12) |
①在这些元素中,最不活泼的元素的结构示意图是
②在这些元素的最高价氧化物对应的水化物中,酸性最强的与呈两性的发生反应的化学方程式为
③元素(8)、(11)和氧元素形成一种广泛使用杀菌消毒剂,该物质中存在的化学键有
④用电子式表示由元素(8)和(10)形成化合物的过程:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】(1)已知CuCl2溶液与乙二胺H2N-CH2CH2-NH2[常用(en)表示]作用,可形成配离子(如图所示):
请回答下列问题︰
①乙二胺分子中N原子成键时采取的杂化类型是____________ ,
乙二胺沸点高于Cl-CH2CH2-Cl的主要原因是___________________________ 。
②上述配离子中含有的化学键类型有:__________________ 。(填写代码,多选) ;
a配位键 b极性键 c非极性键 d离子键
③该配合物 [Cu(en)2]Cl2的系统命名为_______ ;其中铜离子的配位数是_______ 。
(2)下表中实线是元素周期表的部分边界,其中上边界未用实线标出。

根据信息回答下列问题:
①周期表中基态Ga原子的最外层电子排布式为__________________
②Fe元素位于周期表的_____ 区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为____ ;
已知:原子数目和电子总数(或价电子总数)相同的粒子互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为______ 和______ (填化学式)。
③根据VSEPR理论预测ED4-离子的空间构型为_________ 。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的化学式为____________ (写2种)。

请回答下列问题︰
①乙二胺分子中N原子成键时采取的杂化类型是
乙二胺沸点高于Cl-CH2CH2-Cl的主要原因是
②上述配离子中含有的化学键类型有:
a配位键 b极性键 c非极性键 d离子键
③该配合物 [Cu(en)2]Cl2的系统命名为
(2)下表中实线是元素周期表的部分边界,其中上边界未用实线标出。

根据信息回答下列问题:
①周期表中基态Ga原子的最外层电子排布式为
②Fe元素位于周期表的
已知:原子数目和电子总数(或价电子总数)相同的粒子互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为
③根据VSEPR理论预测ED4-离子的空间构型为
您最近一年使用:0次
【推荐1】近年来,我国航天事业发展迅猛,这与材料技术的进步密切相关。如新型储氢材料、陶瓷基复合材料氮化硼(BN)、太阳能电池材料砷化镓(GaAs)等,请按要求回答问题:
(1)基态砷原子的核外电子排布式为_______ ,其电子占据的最高能层符号是_______ ,占据最高能级的电子所在的原子轨道为_______ 形。
(2)硼氢化钠(NaBH4,其中氢元素显-1价)是研究最广泛的储氢材料之一,它可以与水反应缓慢产生氢气: NaBH4+ 2H2O=NaBO2+ 4H2↑。上述方程式中所涉及的非金属元素的电负性由大到小的顺序为_______ ;与硼处于同一周期的元素中,第一电离能大于硼的元素有_______ 种。硼原子在成键时,能将一个2s电子激发进入2p能级参与形成化学键,请写出该激发态原子的价电子的轨道表示式_______ ,该过程形成的原子光谱为_______ 光谱(填“吸收”或“发射”)。
(3)简单金属氢化物也是具有良好发展前景的储氢材料。在LiH中,离子半径: Li+_______ H-(填“>”“=”或“<”,原因是_______ 。
(4)铜、锌两种元素位于元素周期表的_______ 区,两元素的第一电离能(I1)、第二电离能(I2)数据如表所示:
铜的I1小于锌,I2却大于锌的主要原因是_______ 。
(1)基态砷原子的核外电子排布式为
(2)硼氢化钠(NaBH4,其中氢元素显-1价)是研究最广泛的储氢材料之一,它可以与水反应缓慢产生氢气: NaBH4+ 2H2O=NaBO2+ 4H2↑。上述方程式中所涉及的非金属元素的电负性由大到小的顺序为
(3)简单金属氢化物也是具有良好发展前景的储氢材料。在LiH中,离子半径: Li+
(4)铜、锌两种元素位于元素周期表的
| 电离能/(kJ·mol-1) | I1 | I2 |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】(1)前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差2。
回答下列问题:
①D2+的价层电子排布图为____ 。
②四种元素中第一电离能最小的是____ (填元素符号,下同),电负性最大的是____ 。
(2)Ge的最高价氯化物分子式是______ 。该元素可能的性质或应用有__________________ 。
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其最高价氯化物的沸点低于其溴化物的沸点
回答下列问题:
①D2+的价层电子排布图为
②四种元素中第一电离能最小的是
(2)Ge的最高价氯化物分子式是
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其最高价氯化物的沸点低于其溴化物的沸点
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】如图是s能级和p能级的原子轨道图,试回答下列问题:
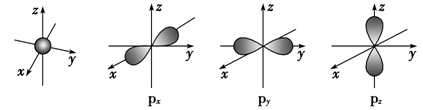
(1)s电子的原子轨道呈______ 形,每个s能级有______ 个原子轨道;p电子的原子轨道呈________ 形,每个p能级有________ 个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是________ 电子,其电子云在空间有________ 方向;元素X的名称是_______ ,它的氢化物的电子式是____________ 。若元素X的原子最外层电子排布式为nsn-1npn+1,那么X的元素符号为________ ,原子的电子排布图为___________ 。

(1)s电子的原子轨道呈
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是
您最近一年使用:0次



