化学与生产、生活有着密切的联系.根据所学知识回答下列问题
(1)铝元素在人体中积累可使人慢性中毒,1989年世界卫生组织正式将铝确定为食品污染源之一而加以控制.铝及其化合物在下列场合使用时必须严格加以控制的是_______ (填字母)
A.用明矾净水 B.制电线电缆 C.制包糖果用的铝箔
(2)_______ (填化学式)可用于呼吸面具或潜艇中的氧气来源
(3)盛装 溶液的试剂瓶不能用玻璃塞的原因是
溶液的试剂瓶不能用玻璃塞的原因是_______ (用化学方程式表示)
(4)当人体缺铁时,往往需要吃补铁保健品,人体能够吸收的是 ,但
,但 很容易被氧化.检验某固体补铁剂中铁元素是否被氧化的方法是
很容易被氧化.检验某固体补铁剂中铁元素是否被氧化的方法是_______ (写出操作过程、现象及结论)
(5)胃舒平[主要成分为 ]是一种治疗胃酸过多的药物,写出胃舒平与胃酸反应的离子方程式
]是一种治疗胃酸过多的药物,写出胃舒平与胃酸反应的离子方程式_______
(6) 是一种有毒气体,如果泄漏会造成严重的环境污染.化工厂检验
是一种有毒气体,如果泄漏会造成严重的环境污染.化工厂检验 是否泄漏的反应方程式为
是否泄漏的反应方程式为 ,若反应中消耗
,若反应中消耗 ,则被氧化的
,则被氧化的 的体积为
的体积为_______ L(标准状况下)
(1)铝元素在人体中积累可使人慢性中毒,1989年世界卫生组织正式将铝确定为食品污染源之一而加以控制.铝及其化合物在下列场合使用时必须严格加以控制的是
A.用明矾净水 B.制电线电缆 C.制包糖果用的铝箔
(2)
(3)盛装
 溶液的试剂瓶不能用玻璃塞的原因是
溶液的试剂瓶不能用玻璃塞的原因是(4)当人体缺铁时,往往需要吃补铁保健品,人体能够吸收的是
 ,但
,但 很容易被氧化.检验某固体补铁剂中铁元素是否被氧化的方法是
很容易被氧化.检验某固体补铁剂中铁元素是否被氧化的方法是(5)胃舒平[主要成分为
 ]是一种治疗胃酸过多的药物,写出胃舒平与胃酸反应的离子方程式
]是一种治疗胃酸过多的药物,写出胃舒平与胃酸反应的离子方程式(6)
 是一种有毒气体,如果泄漏会造成严重的环境污染.化工厂检验
是一种有毒气体,如果泄漏会造成严重的环境污染.化工厂检验 是否泄漏的反应方程式为
是否泄漏的反应方程式为 ,若反应中消耗
,若反应中消耗 ,则被氧化的
,则被氧化的 的体积为
的体积为
更新时间:2023-07-31 14:55:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)已知下列反应:
①HPO3+H2O=H3PO4;②2Na2O2+2H2O=4NaOH+O2↑;
③2F2+2H2O=4HF+O2;④2K+2H2O=2KOH+H2↑;
⑤Cl2+H2O=HCl+HClO。
其中H2O作氧化剂的是________ ,H2O作还原剂的是________ ,H2O既不是氧化剂又不是还原剂的是______ ,其中不属于氧化还原反应的是__________ 。(用序号表示)
(2)除去下列物质中的杂质,写出发生反应的离子方程式:
①氯化钾溶液中混有溴化钾____________________________________ ,
②碳酸氢钾溶液中混有碳酸钾__________________________________ ,
③二氧化碳气体中混有氯化氢气体___________________________________ 。
①HPO3+H2O=H3PO4;②2Na2O2+2H2O=4NaOH+O2↑;
③2F2+2H2O=4HF+O2;④2K+2H2O=2KOH+H2↑;
⑤Cl2+H2O=HCl+HClO。
其中H2O作氧化剂的是
(2)除去下列物质中的杂质,写出发生反应的离子方程式:
①氯化钾溶液中混有溴化钾
②碳酸氢钾溶液中混有碳酸钾
③二氧化碳气体中混有氯化氢气体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮的化合物研究是环境科学的热点课题之一。
金属与不同密度硝酸溶液反应时,还原产物百分比与硝酸密度的关系下图所示:
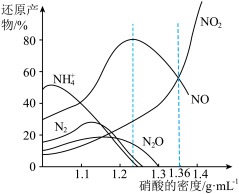
(1)当硝酸溶液的密度为1.36g.cm-3时,下列化学方程式中,能较准确表达Fe与过量硝酸反应的是(填序号)________________ 。
A.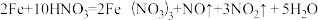
B.
C.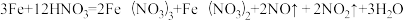
(2)现有一定量铝粉和铜粉的混合物与一定量很稀的硝酸溶液充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入5mo/L的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如下图所示:
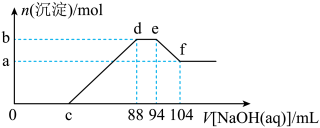
①c点对应NaOH溶液的体积为________________ mL;
②ef段发生反应的离子方程式为________________ 。
(3)研究表明硝酸与金属反应时,最容易生成亚硝酸(HNO2,弱酸),然后才转化成NO2,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的HNO2再氧化成HNO3,如图为金属在不同浓度的HNO3-H2O2混合溶液中的溶解速率和生成NOx的体积V的变化示意图:

①最佳溶解金属的混合溶液中HNO3的质量分数________________ 。
②H2O2与HNO2反应的化学方程式为________________ 。
(4)NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NOx的储存和还原在不同时段交替进行,如图1所示:若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。

①根据图1分析可以得出BaO的作用是________________ 。
②根据图2分析用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,第一步反应的化学方程为________________ 。
③还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有O2条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。请写出该反应的化学方程式________________ 。
金属与不同密度硝酸溶液反应时,还原产物百分比与硝酸密度的关系下图所示:

(1)当硝酸溶液的密度为1.36g.cm-3时,下列化学方程式中,能较准确表达Fe与过量硝酸反应的是(填序号)
A.
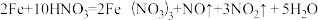
B.

C.
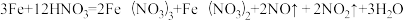
(2)现有一定量铝粉和铜粉的混合物与一定量很稀的硝酸溶液充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入5mo/L的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如下图所示:

①c点对应NaOH溶液的体积为
②ef段发生反应的离子方程式为
(3)研究表明硝酸与金属反应时,最容易生成亚硝酸(HNO2,弱酸),然后才转化成NO2,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的HNO2再氧化成HNO3,如图为金属在不同浓度的HNO3-H2O2混合溶液中的溶解速率和生成NOx的体积V的变化示意图:

①最佳溶解金属的混合溶液中HNO3的质量分数
②H2O2与HNO2反应的化学方程式为
(4)NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NOx的储存和还原在不同时段交替进行,如图1所示:若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。

①根据图1分析可以得出BaO的作用是
②根据图2分析用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,第一步反应的化学方程为
③还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有O2条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】雾霾天气严重影响人们的生活质量,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一、消除氮氧化物有多种方法。
(1)NH3催化还原氮氧化物技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:

①由图1可知NH3催化还原氮氧化物中的氧化剂为___________ 。
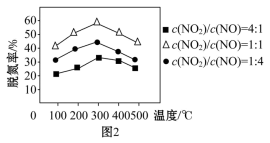
②用Fe作催化剂时,在氨气足量的情况下,不同 对应的脱氮率如图2所示,脱氮效果最佳的
对应的脱氮率如图2所示,脱氮效果最佳的 =
=___________ 。
(2)利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
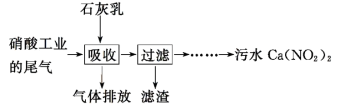
①上述工艺中采用气~液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是___________ ;滤渣可循环使用,滤渣的主要成分是___________ (填化学式)。
②生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为___________ 。
(1)NH3催化还原氮氧化物技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:

①由图1可知NH3催化还原氮氧化物中的氧化剂为
②用Fe作催化剂时,在氨气足量的情况下,不同
 对应的脱氮率如图2所示,脱氮效果最佳的
对应的脱氮率如图2所示,脱氮效果最佳的 =
=
(2)利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:

①上述工艺中采用气~液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是
②生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钛及其合金在航空航天、生物医学等领域具有非常重要的应用价值和广阔的应用前景,可通过下面的转化制取:
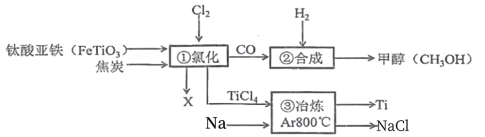
(1)反应①的化学方程式为:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X为____ ,发生氧化反应的物质为____ 。
(2)反应②中,若在标准状况下有5.6LCO参与反应,则转移电子数为____ ,反应②中生成的甲醇属于____ 。
A.氧化物 B.碱 C.有机物 D.电解质 E.非电解质
(3)“反应③”须在无氧和非水性 溶剂中进行,原因是____ 。写出反应③的化学方程式并用双线桥法 表示该反应电子转移的方向和数目____ 。

(1)反应①的化学方程式为:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X为
(2)反应②中,若在标准状况下有5.6LCO参与反应,则转移电子数为
A.氧化物 B.碱 C.有机物 D.电解质 E.非电解质
(3)“反应③”须在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的转化是化学研究的内容之一、回答下列问题:
Ⅰ.一种分解氯化铵( )实现产物分离的物质转化关系如下图所示(a、b、c、d分别代表相应的物质)。
)实现产物分离的物质转化关系如下图所示(a、b、c、d分别代表相应的物质)。

(1)上述转化过程中涉及的物质,除 外,属于盐的是
外,属于盐的是___________ 。(写物质的化学式)
(2)转化过程的总反应方程式为___________ 。
(3)上述转化过程有副产物 生成。请用化学方程式解释其原因
生成。请用化学方程式解释其原因___________ 。
Ⅱ.实验室常用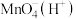 与
与 反应来测定
反应来测定 的浓度,其反应原理(转化过程)如图所示。
的浓度,其反应原理(转化过程)如图所示。
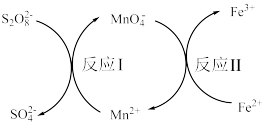
(4)反应Ⅰ中 是
是___________ (填“还原剂”或“氧化剂”)。发生反应Ⅰ时,溶液颜色变化是由无色到___________ 色。
(5)由反应Ⅰ、Ⅱ,判断 、
、 、
、 三者氧化性由强到弱的顺序为:
三者氧化性由强到弱的顺序为:___________ 。
(6)反应Ⅱ的离子方程式为___________ 。每有1mol 参加反应,转移
参加反应,转移___________ mol电子。
Ⅰ.一种分解氯化铵(
 )实现产物分离的物质转化关系如下图所示(a、b、c、d分别代表相应的物质)。
)实现产物分离的物质转化关系如下图所示(a、b、c、d分别代表相应的物质)。
(1)上述转化过程中涉及的物质,除
 外,属于盐的是
外,属于盐的是(2)转化过程的总反应方程式为
(3)上述转化过程有副产物
 生成。请用化学方程式解释其原因
生成。请用化学方程式解释其原因Ⅱ.实验室常用
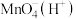 与
与 反应来测定
反应来测定 的浓度,其反应原理(转化过程)如图所示。
的浓度,其反应原理(转化过程)如图所示。
(4)反应Ⅰ中
 是
是(5)由反应Ⅰ、Ⅱ,判断
 、
、 、
、 三者氧化性由强到弱的顺序为:
三者氧化性由强到弱的顺序为:(6)反应Ⅱ的离子方程式为
 参加反应,转移
参加反应,转移
您最近一年使用:0次
【推荐3】氧化还原反应在生产和生活中的很多领域都得到了广泛应用。请运用氧化还原反应的知识完成下列题目:
(1)自然界中的元素大多以化合态存在,而我们在生产和生活中需要许多单质,如金属铁、单质硅等。如果需要把某元素由化合态转变为游离态,则该元素_____
A.被氧化 B.被还原 C.有可能被氧化,也有可能被还原 D.由高价变为0价
(2)铀元素在核工业中有重要作用。物质自然界中存在的铀矿石中含有二氧化铀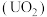 。工业上,可以用钾、钙、镁等金属与二氧化铀反应制得单质铀,若要获得等量的单质铀,钾、钙、镁三种金属中,哪种金属消耗得最多
。工业上,可以用钾、钙、镁等金属与二氧化铀反应制得单质铀,若要获得等量的单质铀,钾、钙、镁三种金属中,哪种金属消耗得最多_____ ,为什么_____ 。
(3)某危险品仓库中存放有化工原料氰化钠(NaCN)。该物质有剧毒,一旦进入城市排水系统,后果不堪设想。当仓库发生火灾爆炸事故时,工作人员一方面封堵氰化钠泄漏渠道,另一方面对已经泄漏的少量氰化钠做无害化处理。下列物质中,可用于处理泄漏的氰化钠的是_____ 。
A.铁粉 B.双氧水 C.臭氧 D.氯化钠
D.氯化钠
(1)自然界中的元素大多以化合态存在,而我们在生产和生活中需要许多单质,如金属铁、单质硅等。如果需要把某元素由化合态转变为游离态,则该元素
A.被氧化 B.被还原 C.有可能被氧化,也有可能被还原 D.由高价变为0价
(2)铀元素在核工业中有重要作用。物质自然界中存在的铀矿石中含有二氧化铀
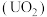 。工业上,可以用钾、钙、镁等金属与二氧化铀反应制得单质铀,若要获得等量的单质铀,钾、钙、镁三种金属中,哪种金属消耗得最多
。工业上,可以用钾、钙、镁等金属与二氧化铀反应制得单质铀,若要获得等量的单质铀,钾、钙、镁三种金属中,哪种金属消耗得最多(3)某危险品仓库中存放有化工原料氰化钠(NaCN)。该物质有剧毒,一旦进入城市排水系统,后果不堪设想。当仓库发生火灾爆炸事故时,工作人员一方面封堵氰化钠泄漏渠道,另一方面对已经泄漏的少量氰化钠做无害化处理。下列物质中,可用于处理泄漏的氰化钠的是
A.铁粉 B.双氧水 C.臭氧
 D.氯化钠
D.氯化钠
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】写出下列离子方程式:
(1)写出 (
( 可表示成
可表示成 形式)与盐酸反应:
形式)与盐酸反应:_______ 。
(2)向 溶液中滴加
溶液中滴加 溶液至溶液呈中性:
溶液至溶液呈中性:_______ 。
(3)氯化铁溶液中滴入硫氰化钾溶液后变为血红色:_______ 。
(1)写出
 (
( 可表示成
可表示成 形式)与盐酸反应:
形式)与盐酸反应:(2)向
 溶液中滴加
溶液中滴加 溶液至溶液呈中性:
溶液至溶液呈中性:(3)氯化铁溶液中滴入硫氰化钾溶液后变为血红色:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】浅绿色的硫酸亚铁铵晶体[又名莫尔盐,(NH4)2SO4·FeSO4·6H2O]比绿矾(FeSO4·7H2O)更稳定,常用于定量分析。莫尔盐的一种实验室制法如下:
废铁屑
 溶液A
溶液A
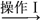
 莫尔盐
莫尔盐
(1)向废铁屑中加入稀硫酸后,并不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是________________________________________________________________ ;
证明溶液A不含Fe3+的最佳试剂是______ (填字母)。
a.酚酞溶液 b.KSCN溶液
c.烧碱溶液 d.KMnO4溶液
操作Ⅰ的步骤是加热蒸发、_____________ 、过滤。
(2)浓度均为0.1 mol·L-1莫尔盐溶液和(NH4)2SO4溶液,c(NH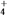 )前者大于后者,原因是
)前者大于后者,原因是____________________________________________________________ 。
(3)用托盘天平称量(NH4)2SO4晶体,晶体要放在天平________ (填“左”或“右”)盘。
(4)从下列装置中选取必要的装置制取(NH4)2SO4溶液,连接的顺序(用接口字母表示)是a接_________ ;________ 接________ 。


(5)将装置C中两种液体分离开的操作名称是_____________ 。
装置D的作用是____________________________________________ 。
废铁屑

 溶液A
溶液A
 莫尔盐
莫尔盐(1)向废铁屑中加入稀硫酸后,并不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是
证明溶液A不含Fe3+的最佳试剂是
a.酚酞溶液 b.KSCN溶液
c.烧碱溶液 d.KMnO4溶液
操作Ⅰ的步骤是加热蒸发、
(2)浓度均为0.1 mol·L-1莫尔盐溶液和(NH4)2SO4溶液,c(NH
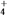 )前者大于后者,原因是
)前者大于后者,原因是(3)用托盘天平称量(NH4)2SO4晶体,晶体要放在天平
(4)从下列装置中选取必要的装置制取(NH4)2SO4溶液,连接的顺序(用接口字母表示)是a接


(5)将装置C中两种液体分离开的操作名称是
装置D的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】关于雾霾的成因,观点颇多。以下是其中的两种观点,请你分析是否可信,并通过进一步查阅资料寻求证据。_______
观点1:某些地区的煤矿含有铀等半衰期达数亿年的核辐射物质,是导致 超标的主要原因。这部分物质通过煤炭燃烧后以粉尘形式排入大气中,并通过核辐射粉尘的方式污染大气。
超标的主要原因。这部分物质通过煤炭燃烧后以粉尘形式排入大气中,并通过核辐射粉尘的方式污染大气。
观点2:我国工业化进程中造成的污染和广大农村的土壤、水源严重污染的叠加效应,是严重雾霾形成的特殊机理。我国水土环境受到富营养化的严重污染,造成环境中微生物种群繁杂和富集;土壤中氨氮浓度高,造成冬春季节水分蒸发带走大量富营养水分,在低空与气溶胶相结合,在凝结核吸水膨胀的同时,也为吸附在凝结核上的微生物快速分裂繁殖提供了养分,长此以往形成了具有地域特征的微生物种群,为雾霾的快速形成、频发和爆发性增长提供了外部条件。
观点1:某些地区的煤矿含有铀等半衰期达数亿年的核辐射物质,是导致
 超标的主要原因。这部分物质通过煤炭燃烧后以粉尘形式排入大气中,并通过核辐射粉尘的方式污染大气。
超标的主要原因。这部分物质通过煤炭燃烧后以粉尘形式排入大气中,并通过核辐射粉尘的方式污染大气。观点2:我国工业化进程中造成的污染和广大农村的土壤、水源严重污染的叠加效应,是严重雾霾形成的特殊机理。我国水土环境受到富营养化的严重污染,造成环境中微生物种群繁杂和富集;土壤中氨氮浓度高,造成冬春季节水分蒸发带走大量富营养水分,在低空与气溶胶相结合,在凝结核吸水膨胀的同时,也为吸附在凝结核上的微生物快速分裂繁殖提供了养分,长此以往形成了具有地域特征的微生物种群,为雾霾的快速形成、频发和爆发性增长提供了外部条件。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】大气污染
①污染物主要来源:除了自然因素外,大气污染物主要来自_______ 和工业生产过程产生的废气及其携带的颗粒物。
②次生污染物的形成

③污水的处理方法
a.常用的污水处理方法有_______ 、_______ 和_______ 等。
b.污水处理的常用化学方法_______ 、_______ 、_______ 等。
c.污水处理的流程
一级处理:通常采用_______ 方法,即用格栅间、沉淀池等除去污水中不溶性的污染物。经一级处理后的水一般达不到排放标准,一级处理作为预处理。
二级处理:采用_______ 方法(又称_______ 法)及某些化学方法,除去水中的可降解有机物等污染物。经二级处理后的水一般可以达到国家规定的排放标准。
三级处理:主要采用_______ 、_______ 、_______ 和_______ 等,对污水进行深度处理和净化。经三级处理后水可用于绿化和景观用水等。
①污染物主要来源:除了自然因素外,大气污染物主要来自
②次生污染物的形成

③污水的处理方法
a.常用的污水处理方法有
b.污水处理的常用化学方法
c.污水处理的流程
一级处理:通常采用
二级处理:采用
三级处理:主要采用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学与生产、生活息息相关。现有下列6种有机物:①乙炔②涤纶③甲醛④油脂⑤苯酚⑥淀粉,请将相应的序号填入空格内。
(1)水溶液(俗称福尔马林)具有杀菌防腐性能的是___________ :
(2)可用于杀菌消毒、制酚醛树脂等,俗称石炭酸的是___________ ;
(3)通常用于制肥皂的是___________ ;
(4)能水解生成葡萄糖供机体利用,还可用于酿制食醋、酒的是___________ ;
(5)属于合成纤维的是___________ ;
(6)常用来焊接或切割金属的是___________ 。
(1)水溶液(俗称福尔马林)具有杀菌防腐性能的是
(2)可用于杀菌消毒、制酚醛树脂等,俗称石炭酸的是
(3)通常用于制肥皂的是
(4)能水解生成葡萄糖供机体利用,还可用于酿制食醋、酒的是
(5)属于合成纤维的是
(6)常用来焊接或切割金属的是
您最近一年使用:0次



