工业上通常采用将氯气通入消石灰或石灰乳的方法制取漂白粉。消石灰要含略少于1%(质量分数)的水,因为极为干燥的消石灰是不跟氯气反应的。生产漂白粉的反应过程比较复杂,可发生如下反应:
①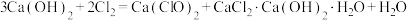 ;
;
②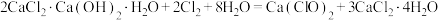 。
。
回答下列问题:
(1) 的摩尔质量为
的摩尔质量为__________ , 中质量分数最大的元素为
中质量分数最大的元素为__________ (填元素符号)。
(2)所含氢原子总数为 的
的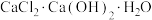 的物质的量为
的物质的量为__________ ,该化合物中Ca元素的物质的量为__________ 。
(3)反应②中,每转移 电子,此时消耗
电子,此时消耗 的体积约为
的体积约为__________ (标准状况下)。
(4)同温同压下,氯化氢与氯气两种气体的密度之比为__________ 。
①
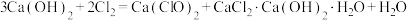 ;
;②
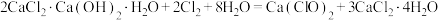 。
。回答下列问题:
(1)
 的摩尔质量为
的摩尔质量为 中质量分数最大的元素为
中质量分数最大的元素为(2)所含氢原子总数为
 的
的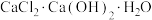 的物质的量为
的物质的量为(3)反应②中,每转移
 电子,此时消耗
电子,此时消耗 的体积约为
的体积约为(4)同温同压下,氯化氢与氯气两种气体的密度之比为
更新时间:2023-08-11 08:51:34
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答下列问题:
(1)5.4gH2O中含有__________ mol H。
(2)硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO 的物质的量是
的物质的量是________ 。
(3)3.01×1024个OH-与__________ mol NH3的质量相同。
(4)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为__________ 。
(5)一定温度和压强下,3L气体A2与9L气体B2完全化合生成6L气体C,则气体C的化学式为__________ (用A、B表示)。
(1)5.4gH2O中含有
(2)硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO
 的物质的量是
的物质的量是(3)3.01×1024个OH-与
(4)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为
(5)一定温度和压强下,3L气体A2与9L气体B2完全化合生成6L气体C,则气体C的化学式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】阿伏伽德罗定律及其推论
(1)在体积相同的两个密闭容器中分别充满以下两种气体:①氧气 ②二氧化硫,并保持两容器内气体的温度和密度均相等,则两气体的物质的量之比___________ ,质量比___________ ,原子个数比___________ ,两装置的压强比___________ 。
(2)同温、同压下,A容器中充满18O2,B容器中充满O3,两装置所含分子总数相等,则A容器和B容器的容积之比是___________ ,密度之比为___________ ;
(3)同温同压时,A容器中的NH3和B容器中的C2H4气所含的氢原子数相等,则A、B两容器的体积比为___________ 。
(1)在体积相同的两个密闭容器中分别充满以下两种气体:①氧气 ②二氧化硫,并保持两容器内气体的温度和密度均相等,则两气体的物质的量之比
(2)同温、同压下,A容器中充满18O2,B容器中充满O3,两装置所含分子总数相等,则A容器和B容器的容积之比是
(3)同温同压时,A容器中的NH3和B容器中的C2H4气所含的氢原子数相等,则A、B两容器的体积比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】填写下列空白:
(1)有6.02×l023个H的H2O,其物质的量是_______ ;1molNa2SO4中所含的离子总数目为______ 。
(2)_____ molH2O中含有的氧原子数与1.5molCO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为_______ 。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为________ 。
(5)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,该混合气体对氢气的相对密度为____________ 。
(6)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为_____________ 。
(1)有6.02×l023个H的H2O,其物质的量是
(2)
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为
(5)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,该混合气体对氢气的相对密度为
(6)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的量是高中化学常用的物理量,请完成以下有关计算:
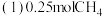 在标准状况下的体积为
在标准状况下的体积为________ L,含有________ 个氢原子。
 同温同压下,等体积的
同温同压下,等体积的 和
和 所含分子个数比为
所含分子个数比为________ ,原子个数比为________ ,密度比为________ 。
 在
在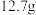 某二价金属的氯化物中含有
某二价金属的氯化物中含有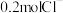 ,此氯化物的摩尔质量为
,此氯化物的摩尔质量为________ ,该金属元素的相对原子质量为________ 。
 若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是
若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是________  设
设 为阿伏加德罗常数的值
为阿伏加德罗常数的值 。
。
 已知
已知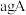 和
和 恰好完全反应生成
恰好完全反应生成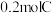 和dgD,则C的摩尔质量为
和dgD,则C的摩尔质量为________ 。
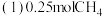 在标准状况下的体积为
在标准状况下的体积为 同温同压下,等体积的
同温同压下,等体积的 和
和 所含分子个数比为
所含分子个数比为 在
在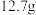 某二价金属的氯化物中含有
某二价金属的氯化物中含有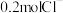 ,此氯化物的摩尔质量为
,此氯化物的摩尔质量为 若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是
若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是 设
设 为阿伏加德罗常数的值
为阿伏加德罗常数的值 。
。 已知
已知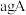 和
和 恰好完全反应生成
恰好完全反应生成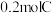 和dgD,则C的摩尔质量为
和dgD,则C的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】根据所学知识,回答下列问题:
(1)标准状况下,1.7 g NH3的体积为___ L;它与标准状况下____ L CH4含有的氢原子数目相同。
(2)等质量的CO和N2所含分子数之比为____ 。
(3)将11.7 g NaCl固体配成10 L溶液,从中取出50 mL,这50 mL溶液中NaCl的物质的量浓度为____ mol·L-1
(4)34 g某二价金属的氯化物中含有0.5 mol Cl-,则该金属氯化物的摩尔质量为_____ g·mol-1,该金属的相对原子质量为_____ 。
(5)已知SO2、O2混合气体的质量共11.2 g,在标准状况下的体积为4.48 L,则混合气体中SO2的物质的量为_____ 。
(1)标准状况下,1.7 g NH3的体积为
(2)等质量的CO和N2所含分子数之比为
(3)将11.7 g NaCl固体配成10 L溶液,从中取出50 mL,这50 mL溶液中NaCl的物质的量浓度为
(4)34 g某二价金属的氯化物中含有0.5 mol Cl-,则该金属氯化物的摩尔质量为
(5)已知SO2、O2混合气体的质量共11.2 g,在标准状况下的体积为4.48 L,则混合气体中SO2的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】Cl2与NaOH溶液反应可生成NaCl、NaClO和NaClO3、c(Cl-)和c(ClO-)的比值与反应温度有关。用48 g NaOH配成的500 mL溶液,与Cl2恰好完全反应(忽略Cl2与水的反应、盐类的水解及溶液体积变化)。
(1)NaOH溶液的物质的量浓度___ mol/L
(2)某温度下,反应后溶液中c(Cl-)=3c(ClO-), 则溶液在c(ClO-)=_____ mol/L。
(1)NaOH溶液的物质的量浓度
(2)某温度下,反应后溶液中c(Cl-)=3c(ClO-), 则溶液在c(ClO-)=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)质量比为16:7:6的三种气体SO2、CO、NO,分子个数之比为_______ ;氧原子个数之比为_______ ;相同条件下体积比为_______ 。
(2)等质量的O2和SO2,物质的量之比为_______ ,在相同条件下的体积之比为_______ ,原子数之比为_______ 。
(3)在反应KIO3+6HI=3I2+KI+3H2O中,氧化剂与还原剂的物质的量之比为_______ 。
(4)Na2CO3溶液与CH3COOH溶液反应的离子方程式为_______
(5)大理石(CaCO3)与稀HNO3反应的离子方程式为:_______
(6)将少量NaHSO4溶液滴加到Ba(OH)2溶液中,当恰好沉淀时,反应的离子方程式为_______ 。
(2)等质量的O2和SO2,物质的量之比为
(3)在反应KIO3+6HI=3I2+KI+3H2O中,氧化剂与还原剂的物质的量之比为
(4)Na2CO3溶液与CH3COOH溶液反应的离子方程式为
(5)大理石(CaCO3)与稀HNO3反应的离子方程式为:
(6)将少量NaHSO4溶液滴加到Ba(OH)2溶液中,当恰好沉淀时,反应的离子方程式为
您最近一年使用:0次
【推荐3】稀有气体在一定条件下能与某些物质反应,如:Xe与F2在一定条件下可以形成XeF4 、XeF6。现有XeF4 和XeF6的混合气体1.12L(标准状况),密度为10.26g/L。
(1)混合气体的平均摩尔质量为:________________ 。(计算结果保留两位小数,下同)
(2)混合气体中XeF4的质量为:___________________ 。
(3)氟化氙都是强氧化剂,在水中能将Cl- 氧化成Cl2,并生成Xe和HF。将标准状况下的上述混合气体1.12L通入含过量Cl- 的溶液中,能生成Cl2_____________ L(标准状况)。
(1)混合气体的平均摩尔质量为:
(2)混合气体中XeF4的质量为:
(3)氟化氙都是强氧化剂,在水中能将Cl- 氧化成Cl2,并生成Xe和HF。将标准状况下的上述混合气体1.12L通入含过量Cl- 的溶液中,能生成Cl2
您最近一年使用:0次



