某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
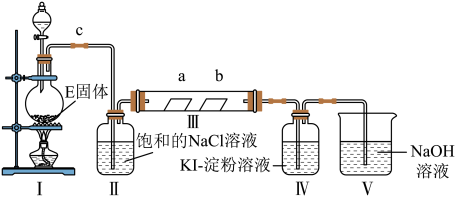
(1)实验室以二氧化锰和浓盐酸制备氯气的离子方程式是___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)实验过程中,装置IV中的实验现象为___________ ;发生反应的化学方程式为___________ 。
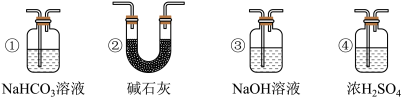
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的___________ 装置(填序号),
(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式___________ 。

(1)实验室以二氧化锰和浓盐酸制备氯气的离子方程式是
(2)装置Ⅱ的作用是
(3)实验过程中,装置IV中的实验现象为
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的

(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式
更新时间:2023-07-10 20:32:44
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学学习小组设计如图实验装置(夹持和加热装置略去)制备Cl2,并探究氯气的相关性质。
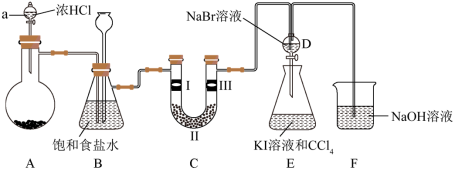
回答下列问题:
⑴ 装置中a玻璃仪器的名称为_____________ ;整套装置装配完毕后,首先进行的操作是______________ ,再添加试剂。
⑵ 若A装置中的固体药品为MnO2,其化学方程式为_______________________ 。若A装置中的固体药品为KClO3,则反应中每生成1 mol Cl2时转移电子的物质的量为_________ mol(结果保留两位小数)。
⑶ 装置C的作用是验证氯气是否具有漂白性,Ⅰ处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是_________ 、_____________ 。
⑷ 设计装置D、E的目的是比较氯、溴、碘的非金属性。但有同学认为该设计不够严密,他的理由可能是_____________ 。
⑸ 甲同学提出,装置F中改用过量的Na2SO3溶液,乙同学认为此法不可行。请用离子方程式解释乙认为不可行的原因:_____________ 。

回答下列问题:
⑴ 装置中a玻璃仪器的名称为
⑵ 若A装置中的固体药品为MnO2,其化学方程式为
⑶ 装置C的作用是验证氯气是否具有漂白性,Ⅰ处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是
⑷ 设计装置D、E的目的是比较氯、溴、碘的非金属性。但有同学认为该设计不够严密,他的理由可能是
⑸ 甲同学提出,装置F中改用过量的Na2SO3溶液,乙同学认为此法不可行。请用离子方程式解释乙认为不可行的原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】无水四氯化锡常用作媒染剂和有机合成中的氯化催化剂。实验室可用熔融的锡(熔点 232 ℃)与 Cl2反应制备 SnCl4,装置如图。
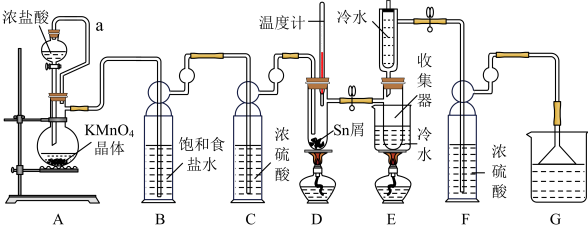
已知:①SnCl2、SnCl4有关物理性质:
②SnCl4极易水解生成 SnO2·xH2O。回答下列问题:
(1)导管 a 的作用是_____ ,装置 A 中发生反应的离子方程式为_____ 。
(2)当观察到装置 F 液面上方_____ 时才开始点燃 D 处的酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的是①_________ ;②_____ 。
(3)若上述装置中缺少装置 C( 其它均相同) ,则D处具支试管中发生的主要副反应化学方程式为_____ 。
(4)Cl2和锡的反应产物有 SnCl4和 SnCl2,为防止产品中带入过多的 SnCl2,可使用的温度范围是_____ 。
(5)滴定分析产品中 Sn(Ⅱ)的含量:用分析天平称取 5.000g 产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用 0.1000 mol·L-1的碘标准溶液滴定至终点时消耗 20.00 mL,则产品中 Sn(Ⅱ)的含量为_____ 。(已知 Sn2++I2=2I-+Sn4+)

已知:①SnCl2、SnCl4有关物理性质:
| 物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
| SnCl2 | 无色晶体 | 246 | 652 |
| SnCl4 | 无色液体 | -33 | 114 |
(1)导管 a 的作用是
(2)当观察到装置 F 液面上方
(3)若上述装置中缺少装置 C( 其它均相同) ,则D处具支试管中发生的主要副反应化学方程式为
(4)Cl2和锡的反应产物有 SnCl4和 SnCl2,为防止产品中带入过多的 SnCl2,可使用的温度范围是
(5)滴定分析产品中 Sn(Ⅱ)的含量:用分析天平称取 5.000g 产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用 0.1000 mol·L-1的碘标准溶液滴定至终点时消耗 20.00 mL,则产品中 Sn(Ⅱ)的含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如下图所示。
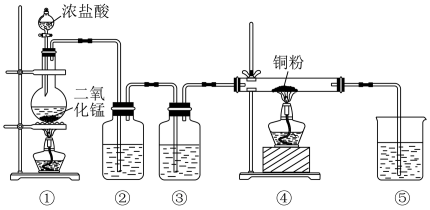
回答下列问题:
(1)写出盛放浓盐酸仪器的名称:_______ 。写出在①中发生反应的化学方程式为_______ 。甲同学用87gMnO2与足量浓盐酸反应制氯气,乙同学用足量MnO2与含146gHCl的浓盐酸反应制氯气,两者制得氯气_______ (填“甲多”,“乙多”,“一样多”)
(2)②中选用试剂是_______ ;③中选用试剂是_______ ;
(3)用如图装置验证氯气漂白性,图中B为开关。先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液可能是_______ 。
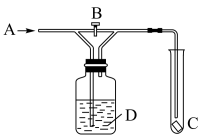
A.浓硫酸 B.浓NaOH溶液 C.饱和食盐水
(4)④中反应的化学方程式是_______ 。
(5)实验室用一种常见的碱溶液吸收氯气,写出⑤中反应的离子方程式是_______ 。

回答下列问题:
(1)写出盛放浓盐酸仪器的名称:
(2)②中选用试剂是
(3)用如图装置验证氯气漂白性,图中B为开关。先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液可能是

A.浓硫酸 B.浓NaOH溶液 C.饱和食盐水
(4)④中反应的化学方程式是
(5)实验室用一种常见的碱溶液吸收氯气,写出⑤中反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验探究;探究碳、硅元素的非金属性的相对强弱。根据要求回答下列问题。
(1)实验装置(部分夹持装置已略)
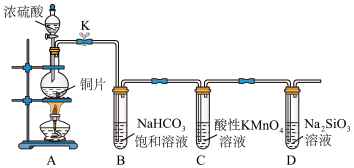
仪器a的名称为__________________ 。
(2)实验步骤
连接装置、__________ 、加药品后,打开K,然后滴入浓硫酸,加热。
(3)问题探究(已知酸性: ,
, 为白色沉淀)
为白色沉淀)
①Cu与浓硫酸反应的化学方程式是________ ;装置C中酸性 溶液的作用是
溶液的作用是_________ 。
②能说明碳元素的非金属性比硅元素的非金属性强的实验现象是___________ 。
③依据装置B中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性________ (填“能”或“否"),装置B中发生反应的离子方程式是______________________ 。
(1)实验装置(部分夹持装置已略)

仪器a的名称为
(2)实验步骤
连接装置、
(3)问题探究(已知酸性:
 ,
, 为白色沉淀)
为白色沉淀)①Cu与浓硫酸反应的化学方程式是
 溶液的作用是
溶液的作用是②能说明碳元素的非金属性比硅元素的非金属性强的实验现象是
③依据装置B中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】有人设计出一种让Na与CuSO4,溶液反应的方法.实验时,往100mL大试管中先加40mL煤油,取3粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加煤油入CuSO4溶液使煤油的液面至胶塞,并夹紧弹簧夹(如图)仔细观察,回答下列问题:

(1)从试剂瓶中取用金属钠需要_______ (填所用工具或耗材名称)。剩余的Na____________ (能/不能)放回原试剂瓶。
(2)有关钠反应的现象是____________
(3)大试管的溶液中出现的现象:____________
(4)装置中液面的变化____________
(5)写出钠与硫酸铜溶液反应的化学方程式:____________

(1)从试剂瓶中取用金属钠需要
(2)有关钠反应的现象是
(3)大试管的溶液中出现的现象:
(4)装置中液面的变化
(5)写出钠与硫酸铜溶液反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。某兴趣小组通过下图所示装置(夹持装置略)对其进行制备、收集、吸收并制取NaClO2。
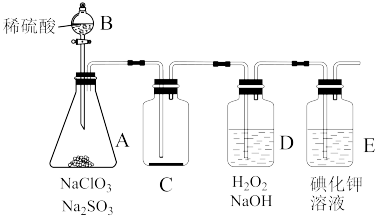
(1)仪器的B名称是___________ 。
(2)打开B的活塞,A中有ClO2生成,若制备1molClO2,理论上消耗的硫酸的物质的量为___________ ;D中吸收ClO2后生成NaClO2,写出D中所发生反应的离子方程式:___________ 。
(3)E中溶液出现黄色___________ (填“能”或“否”)说明ClO2未被 和NaOH的混合溶液充分吸收,说明理由:
和NaOH的混合溶液充分吸收,说明理由:___________ 。
(4)已知:当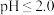 时,ClO
时,ClO 能被I-还原。E装置吸收逸出的少量ClO2气体后所得溶液(pH为5.5~6.5)中存在少量ClO
能被I-还原。E装置吸收逸出的少量ClO2气体后所得溶液(pH为5.5~6.5)中存在少量ClO 。请补充完整检验E装置溶液中存在少量ClO
。请补充完整检验E装置溶液中存在少量ClO 的实验方案:取一定体积E装置中的溶液于分液漏斗中,
的实验方案:取一定体积E装置中的溶液于分液漏斗中,___________ ,则溶液中存在ClO 。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)
。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)

(1)仪器的B名称是
(2)打开B的活塞,A中有ClO2生成,若制备1molClO2,理论上消耗的硫酸的物质的量为
(3)E中溶液出现黄色
 和NaOH的混合溶液充分吸收,说明理由:
和NaOH的混合溶液充分吸收,说明理由:(4)已知:当
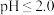 时,ClO
时,ClO 能被I-还原。E装置吸收逸出的少量ClO2气体后所得溶液(pH为5.5~6.5)中存在少量ClO
能被I-还原。E装置吸收逸出的少量ClO2气体后所得溶液(pH为5.5~6.5)中存在少量ClO 。请补充完整检验E装置溶液中存在少量ClO
。请补充完整检验E装置溶液中存在少量ClO 的实验方案:取一定体积E装置中的溶液于分液漏斗中,
的实验方案:取一定体积E装置中的溶液于分液漏斗中, 。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)
。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)
您最近一年使用:0次



