应用电化学原理,回答下列问题:
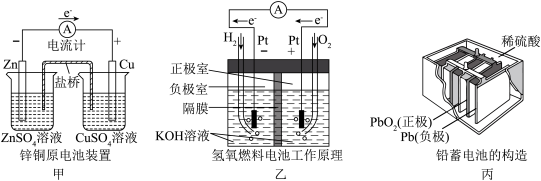
(1)上述三个装置中,负极反应物化学性质上的共同特点是_______ 。
(2)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是_______ 。
(3)乙中正极反应式为_______ ;若将H2换成CH4,则负极反应式为_______ 。
(4)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池的_______ 极相连接。

(1)上述三个装置中,负极反应物化学性质上的共同特点是
(2)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是
(3)乙中正极反应式为
(4)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池的
23-24高二上·全国·课时练习 查看更多[1]
更新时间:2023-08-14 17:08:30
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
2Cu(s)+ O2(g)=Cu2O(s) ΔH=-169 kJ·mol-1;
O2(g)=Cu2O(s) ΔH=-169 kJ·mol-1;
C(s)+ O2(g)=CO(g) ΔH=-110.5 kJ·mol-1;
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1;
2Cu(s)+O2(g)=2CuO(s) ΔH=-314 kJ·mol-1。
工业上用木炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为_______ 。
(2)某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中电解质足量),当闭合该装置的电键K时,观察到电流表的指针发生了偏转。
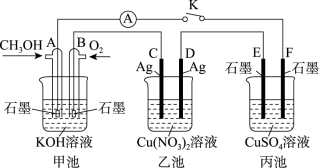
请回答下列问题:
①甲池为_______ (填“原电池”“电解池”或“电镀池”),A极的电极反应式为_______ 。
②丙池中F极为_______ (填“正极”“负极”“阴极”或“阳极”),该池的总反应式为_______ 。
③当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为_______ mL(标准状况)。
(1)纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
2Cu(s)+
 O2(g)=Cu2O(s) ΔH=-169 kJ·mol-1;
O2(g)=Cu2O(s) ΔH=-169 kJ·mol-1;C(s)+
 O2(g)=CO(g) ΔH=-110.5 kJ·mol-1;
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1;2Cu(s)+O2(g)=2CuO(s) ΔH=-314 kJ·mol-1。
工业上用木炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
(2)某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中电解质足量),当闭合该装置的电键K时,观察到电流表的指针发生了偏转。

请回答下列问题:
①甲池为
②丙池中F极为
③当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有铜片、锌片和250mL稀硫酸组成的原电池,当在铜片上放出4.48L(标准状况下)的气体时,硫酸恰好完全反应。
(1)该原电池的负极反应式______________________
(2) 原稀硫酸的物质的量浓度是___________ mol/ L
(3)锌片减少的质量__________
(1)该原电池的负极反应式
(2) 原稀硫酸的物质的量浓度是
(3)锌片减少的质量
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。

①制H2时,连接__________ ; 产生H2的电极方程式是__________ 。
②改变开关连接方式,可得O2。
③结合①和②中电极3的电极反应式,说明电极3的作用:__________ 。
(2)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:

负极区发生的反应有__________ (写反应方程式)。电路中转移1 mol电子,需消耗氧气__________ L(标准状况)。

①制H2时,连接
②改变开关连接方式,可得O2。
③结合①和②中电极3的电极反应式,说明电极3的作用:
(2)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:

负极区发生的反应有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)利用8NH3+6NO2=7N2+12H2O可以消除氮氧化物的污染,若设计成原电池,使用2mol·L-1的KOH溶液为电解质溶液。该电池正极的电极反应式为_______ ,放电一段时间后,负极附近溶液pH将_______ (填“增大”、“减小”或“不变”)。
(2)一种熔融碳酸盐燃料电池原理示意如图所示
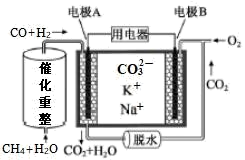
①写出催化重整的化学方程式_______ 。
②电池工作时, 向
向_______ (填A或B)极移动,电极A上H2参与的电极反应为:_______ 。
③用电器中每转移2mol电子,理论上电极B处消耗的气体体积(标准状况下)为_______ L。
(2)一种熔融碳酸盐燃料电池原理示意如图所示

①写出催化重整的化学方程式
②电池工作时,
 向
向③用电器中每转移2mol电子,理论上电极B处消耗的气体体积(标准状况下)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将质量相等的锌片和铜片用导线相连浸入500 mL硫酸铜溶液中构成如图的装置。
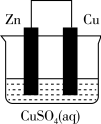
(1)此装置为___________ ,该装置中发生反应总的离子方程式为___________ ,铜片周围溶液会出现___________ 的现象。
(2)Cu电极是___________ (填“正极”或“负极”),写出其电极反应式___________ 。
(3)若2 min后测得锌片质量减少13 g,则导线中流过的电子为___________ mol。

(1)此装置为
(2)Cu电极是
(3)若2 min后测得锌片质量减少13 g,则导线中流过的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】实验室中,学生利用下图装置制作一个简单燃料电池。步骤如下:

①检验装置气密性后向U形管中注入适量的6 mol·L-1稀H2SO4溶液,至接近橡胶塞底部。
②接通学生电源K1,观察实验现象,当一端玻璃导管内的液柱接近溢出时,切断学生电源K1。
③将石英钟内的干电池取出,用导线与石英钟的正负极相连,接入装置中。接通学生电源K2,观察石英钟指针。
回答下列问题:
(1)接通学生电源K1,在右侧石墨棒表面观察到_______ 。
(2)观察到左侧的玻璃导管内的液柱先接近溢出,说明左侧石墨棒所连的是学生电源的_______ (填“正极”或“负极”),该石墨表面的电极方程式是_______ 。
(3)用导线与石英钟的正负极相连接入装置时,石英钟的正极应与_______ (填“左”或“右”)侧的石墨棒连接的导线相连。
(4)出现_______ 的现象,证明该燃料电池制作成功。燃料电池正极的电极方程式是_______ 。

①检验装置气密性后向U形管中注入适量的6 mol·L-1稀H2SO4溶液,至接近橡胶塞底部。
②接通学生电源K1,观察实验现象,当一端玻璃导管内的液柱接近溢出时,切断学生电源K1。
③将石英钟内的干电池取出,用导线与石英钟的正负极相连,接入装置中。接通学生电源K2,观察石英钟指针。
回答下列问题:
(1)接通学生电源K1,在右侧石墨棒表面观察到
(2)观察到左侧的玻璃导管内的液柱先接近溢出,说明左侧石墨棒所连的是学生电源的
(3)用导线与石英钟的正负极相连接入装置时,石英钟的正极应与
(4)出现
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请回答下列问题:
(1)下列各反应中,符合如图所示能量变化的是___________ (填字母)。
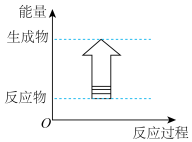
a.H2和Cl2的反应 b.Al和盐酸的反应
c.Na和H2O的反应 d.Ba(OH)2·8H2O和NH4Cl的反应
(2)纽扣式微型银锌电池广泛的应用于电子表和电子计算器中,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。其负极的电极反应式:___________ 正极的电极反应式:___________ ,工作时电池电解质溶液的碱性___________ (填“增强”、“减弱”或“不变”)。
(3)固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。
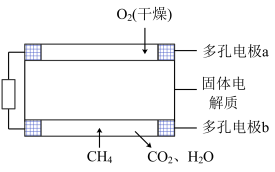
①b电极为电池的___________ 极,固体电解质中的阳离子向___________ 极移动。(填正或负)
②a电极反应式为:___________ ,b电极反应式为:___________ 电池总反应的化学方程式为:___________ 。当电路中有2mol电子转移时,理论上负极消耗的气体在标况下的体积是___________ L。
(1)下列各反应中,符合如图所示能量变化的是

a.H2和Cl2的反应 b.Al和盐酸的反应
c.Na和H2O的反应 d.Ba(OH)2·8H2O和NH4Cl的反应
(2)纽扣式微型银锌电池广泛的应用于电子表和电子计算器中,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。其负极的电极反应式:
(3)固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。

①b电极为电池的
②a电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2019年诺贝尔化学奖授予约翰古迪纳夫、斯坦利惠廷厄姆和吉野彰三位科学家,以表彰他们在锂离子电池研发领域作出的贡献。我国科学家设计了一种锂离子电池,并用此电池来电解含有Na2SO3的工业废水,获得硫酸等物质,如图所示:
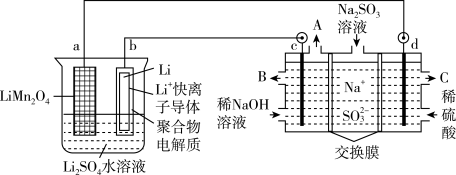
(1)锂离子电池工作时,a极发生____ 反应(填写“氧化”或“还原”),Li+移向__ 极(填写“a”或“b”),写出b极的电极反应式为____________ 。
(2)电解池中物质A的化学式是______ ,其中右侧交换膜应选用______ 交换膜(填写“阳离子”或“阴离子”),该交换膜的作用是________________________ ,写出d极的电极反应式为____________ 。
(3)若电解池左侧溶液的体积为2L,其浓度由2mol•L-1变为4mol•L-1时,理论上电路中通过的电子是______ mol。

(1)锂离子电池工作时,a极发生
(2)电解池中物质A的化学式是
(3)若电解池左侧溶液的体积为2L,其浓度由2mol•L-1变为4mol•L-1时,理论上电路中通过的电子是
您最近一年使用:0次
填空题
|
适中
(0.65)
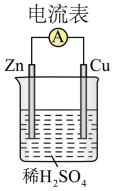
【推荐3】化学电池的发明,是贮能和供能技术的巨大进步。______ (填“正极”或“负极”)。
(2)装置中锌片上发生_____ (“氧化”或“还原”)反应,写出负极发生的电极反应式______ 。
(3)电子流动的方向是________ (“Zn→Cu”或“Cu→Zn”)。
(4)上图所示装置可将_______ (写离子方程式)反应释放的能量 直接转变为电能;能证明产生电能的实验现象是________ 。
(5)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。___________ (填序号)。
①A为电池的正极 ②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
(2)装置中锌片上发生
(3)电子流动的方向是
(4)上图所示装置可将
(5)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。
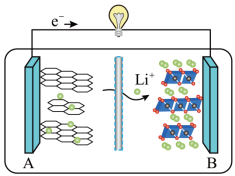
①A为电池的正极 ②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
您最近一年使用:0次



