配平下列方程式。
① S+ KOH K2S+ K2SO3+ H2O
K2S+ K2SO3+ H2O_____ 。
② KClO3 KCl+ O2↑
KCl+ O2↑_____ 。
③ Cl2+ NaOH NaCl+ NaClO3+ H2O
NaCl+ NaClO3+ H2O_____ 。
④ (NH4)2SO4= NH3↑+ SO2↑+ N2↑+ H2O_____ 。
⑤ Fe+ HNO3(浓) Fe(NO3)3+ NO2↑+ H2O
Fe(NO3)3+ NO2↑+ H2O_____ 。
① S+ KOH
 K2S+ K2SO3+ H2O
K2S+ K2SO3+ H2O② KClO3
 KCl+ O2↑
KCl+ O2↑③ Cl2+ NaOH
 NaCl+ NaClO3+ H2O
NaCl+ NaClO3+ H2O④ (NH4)2SO4= NH3↑+ SO2↑+ N2↑+ H2O
⑤ Fe+ HNO3(浓)
 Fe(NO3)3+ NO2↑+ H2O
Fe(NO3)3+ NO2↑+ H2O
更新时间:2023-08-26 11:46:50
|
【知识点】 氧化还原反应方程式的配平解读
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知亚磷酸 是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
 亚磷酸与银离子反应的离子方程式为
亚磷酸与银离子反应的离子方程式为______ 。
 向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式
向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式______ 。
 某温度下,
某温度下, 的亚磷酸溶液的pH为
的亚磷酸溶液的pH为 ,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数
,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数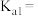
______ 。 亚磷酸第二级电离忽略不计,结果保留两位有效数字
亚磷酸第二级电离忽略不计,结果保留两位有效数字
 是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
是具有强还原性的二元弱酸,可被银离子氧化为磷酸。 亚磷酸与银离子反应的离子方程式为
亚磷酸与银离子反应的离子方程式为 向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式
向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式 某温度下,
某温度下, 的亚磷酸溶液的pH为
的亚磷酸溶液的pH为 ,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数
,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数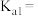
 亚磷酸第二级电离忽略不计,结果保留两位有效数字
亚磷酸第二级电离忽略不计,结果保留两位有效数字
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】图示分析是学习化学重要手段之一,学习过程中常遇到各类“数形结合”问题。结合所给图示回答相关问题:
(1)从元素化合价和物质类别两个维度学习、研究物质的性质及转化,是一种行之有效的方法。下图是氮元素的“价类二维图”的部分信息。
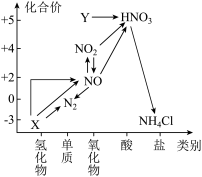
①X的电子式为___________ ;Y的化学式为___________ 。
②图中关于 转化为
转化为 的反应过程,下列说法不正确的是
的反应过程,下列说法不正确的是___________ 。
a.氮元素的化合价不发生变化
b.该转化过程中, 一定既是氧化剂,又是还原剂
一定既是氧化剂,又是还原剂
c.若用 与
与 反应制取
反应制取 ,可生成另一种产物
,可生成另一种产物
③下图为氨气水溶性的探究:利用如图所示的装置进行实验,欲观察的现象是___________ ;合理的验证操作为___________ 。
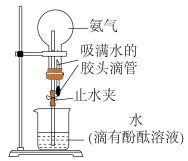
④ 和
和 在固氮酶的作用下转化为氨气,最后生成被植物吸收的
在固氮酶的作用下转化为氨气,最后生成被植物吸收的 ,其中固氮酶的作用是
,其中固氮酶的作用是___________ 。
(2) 、
、 和
和 是大气初期污染物的主要成分,
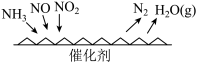
是大气初期污染物的主要成分, 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当 与
与 的物质的量之比为1:1时,与足量氨气在一定条件下发生反应,该反应的化学方程式为
的物质的量之比为1:1时,与足量氨气在一定条件下发生反应,该反应的化学方程式为___________ 。
(3)研究表明硝酸与金属反应时,最容易生成亚硝酸( ,弱酸),然后才转化成
,弱酸),然后才转化成 ,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸,如图为金属在不同浓度的
,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸,如图为金属在不同浓度的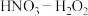 混合溶液中的溶解速率和生成
混合溶液中的溶解速率和生成 的体积V的变化示意图,请回答下列问题:
的体积V的变化示意图,请回答下列问题:

①最佳溶解金属的混合溶液中 的质量分数为
的质量分数为___________ ,理由是___________ 。
②过氧化氢与亚硝酸反应的化学方程式为___________ 。
(1)从元素化合价和物质类别两个维度学习、研究物质的性质及转化,是一种行之有效的方法。下图是氮元素的“价类二维图”的部分信息。

①X的电子式为
②图中关于
 转化为
转化为 的反应过程,下列说法不正确的是
的反应过程,下列说法不正确的是a.氮元素的化合价不发生变化
b.该转化过程中,
 一定既是氧化剂,又是还原剂
一定既是氧化剂,又是还原剂c.若用
 与
与 反应制取
反应制取 ,可生成另一种产物
,可生成另一种产物
③下图为氨气水溶性的探究:利用如图所示的装置进行实验,欲观察的现象是

④
 和
和 在固氮酶的作用下转化为氨气,最后生成被植物吸收的
在固氮酶的作用下转化为氨气,最后生成被植物吸收的 ,其中固氮酶的作用是
,其中固氮酶的作用是(2)
 、
、 和
和 是大气初期污染物的主要成分,
是大气初期污染物的主要成分, 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当 与
与 的物质的量之比为1:1时,与足量氨气在一定条件下发生反应,该反应的化学方程式为
的物质的量之比为1:1时,与足量氨气在一定条件下发生反应,该反应的化学方程式为
(3)研究表明硝酸与金属反应时,最容易生成亚硝酸(
 ,弱酸),然后才转化成
,弱酸),然后才转化成 ,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸,如图为金属在不同浓度的
,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸,如图为金属在不同浓度的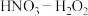 混合溶液中的溶解速率和生成
混合溶液中的溶解速率和生成 的体积V的变化示意图,请回答下列问题:
的体积V的变化示意图,请回答下列问题:
①最佳溶解金属的混合溶液中
 的质量分数为
的质量分数为②过氧化氢与亚硝酸反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】H2O2是重要的化学试剂,在实验室和实际生产中应用广泛。
(1)H2O2有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:______________ 。
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在___________ (填“酸式”或“碱式”)滴定管中,判断到达滴定终点的现象是___________ 。
(2)①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:___________ 。
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是___________ 。
③利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥Cr(Ⅲ)的处理工艺流程如图:
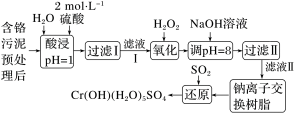
已知:硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。H2O2的作用是将滤液Ⅰ中的Cr3+转化为 ,写出此反应的离子方程式:
,写出此反应的离子方程式: ___________ 。
(3)H2O2是一种二元弱酸,写出其第一步电离的方程式:___________ ,它与过量的Ba(OH)2反应的化学方程式为________________ 。
(1)H2O2有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在
(2)①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是
③利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥Cr(Ⅲ)的处理工艺流程如图:

已知:硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。H2O2的作用是将滤液Ⅰ中的Cr3+转化为
 ,写出此反应的离子方程式:
,写出此反应的离子方程式: (3)H2O2是一种二元弱酸,写出其第一步电离的方程式:
您最近一年使用:0次



