图示分析是学习化学重要手段之一,学习过程中常遇到各类“数形结合”问题。结合所给图示回答相关问题:
(1)从元素化合价和物质类别两个维度学习、研究物质的性质及转化,是一种行之有效的方法。下图是氮元素的“价类二维图”的部分信息。
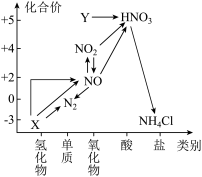
①X的电子式为___________ ;Y的化学式为___________ 。
②图中关于 转化为
转化为 的反应过程,下列说法不正确的是
的反应过程,下列说法不正确的是___________ 。
a.氮元素的化合价不发生变化
b.该转化过程中, 一定既是氧化剂,又是还原剂
一定既是氧化剂,又是还原剂
c.若用 与
与 反应制取
反应制取 ,可生成另一种产物
,可生成另一种产物
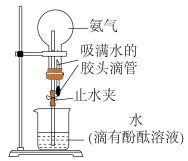
③下图为氨气水溶性的探究:利用如图所示的装置进行实验,欲观察的现象是___________ ;合理的验证操作为___________ 。
④ 和
和 在固氮酶的作用下转化为氨气,最后生成被植物吸收的
在固氮酶的作用下转化为氨气,最后生成被植物吸收的 ,其中固氮酶的作用是
,其中固氮酶的作用是___________ 。
(2) 、
、 和
和 是大气初期污染物的主要成分,
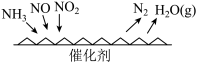
是大气初期污染物的主要成分, 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当 与
与 的物质的量之比为1:1时,与足量氨气在一定条件下发生反应,该反应的化学方程式为
的物质的量之比为1:1时,与足量氨气在一定条件下发生反应,该反应的化学方程式为___________ 。
(3)研究表明硝酸与金属反应时,最容易生成亚硝酸( ,弱酸),然后才转化成
,弱酸),然后才转化成 ,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸,如图为金属在不同浓度的
,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸,如图为金属在不同浓度的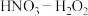 混合溶液中的溶解速率和生成
混合溶液中的溶解速率和生成 的体积V的变化示意图,请回答下列问题:
的体积V的变化示意图,请回答下列问题:

①最佳溶解金属的混合溶液中 的质量分数为
的质量分数为___________ ,理由是___________ 。
②过氧化氢与亚硝酸反应的化学方程式为___________ 。
(1)从元素化合价和物质类别两个维度学习、研究物质的性质及转化,是一种行之有效的方法。下图是氮元素的“价类二维图”的部分信息。

①X的电子式为
②图中关于
 转化为
转化为 的反应过程,下列说法不正确的是
的反应过程,下列说法不正确的是a.氮元素的化合价不发生变化
b.该转化过程中,
 一定既是氧化剂,又是还原剂
一定既是氧化剂,又是还原剂c.若用
 与
与 反应制取
反应制取 ,可生成另一种产物
,可生成另一种产物
③下图为氨气水溶性的探究:利用如图所示的装置进行实验,欲观察的现象是

④
 和
和 在固氮酶的作用下转化为氨气,最后生成被植物吸收的
在固氮酶的作用下转化为氨气,最后生成被植物吸收的 ,其中固氮酶的作用是
,其中固氮酶的作用是(2)
 、
、 和
和 是大气初期污染物的主要成分,
是大气初期污染物的主要成分, 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当 与
与 的物质的量之比为1:1时,与足量氨气在一定条件下发生反应,该反应的化学方程式为
的物质的量之比为1:1时,与足量氨气在一定条件下发生反应,该反应的化学方程式为
(3)研究表明硝酸与金属反应时,最容易生成亚硝酸(
 ,弱酸),然后才转化成
,弱酸),然后才转化成 ,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸,如图为金属在不同浓度的
,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸,如图为金属在不同浓度的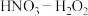 混合溶液中的溶解速率和生成
混合溶液中的溶解速率和生成 的体积V的变化示意图,请回答下列问题:
的体积V的变化示意图,请回答下列问题:
①最佳溶解金属的混合溶液中
 的质量分数为
的质量分数为②过氧化氢与亚硝酸反应的化学方程式为
更新时间:2023-07-15 16:11:10
|
相似题推荐
【推荐1】溴和碘的化合物在生产和生活中有广泛的用途.
(1)市场销售的某种食用精制盐中含碘酸钾。
①碘酸钾与碘化钾在酸性条件下发生如下反应,配平该反应的化学方程式:
( )  +
+( ) KI+( ) 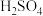 =
=( )  +
+( )  +
+( )
②上述反应生成的I2可用四氯化碳检验,现象为________________________ 。
向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
Na2SO3稀溶液与I2反应的离子方程式是________________________ 。
(2)海水提溴过程中溴元素的变化如下:

①过程I,海水显碱性,调其pH<3.5后,再通入氯气,调节海水pH可提高C12的利用率,用平衡原理解释其原因是_______________________ 。
②过程II,用热空气将溴赶出,再用浓Na2CO3溶液吸收。完成并配平下列方程式。
( ) 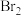 +
+( ) 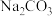 =
=( )  +
+( )  +
+( )
③过程III,用硫酸酸化可得Br2和Na2SO4的混合溶液。相同条件下,若用盐酸酸化,则所得溴的质量减少,原因是_________________________ 。
④NaBrO3是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入 2.6molNaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:

则原溶液中NaI的物质的量为_________ mol.
(1)市场销售的某种食用精制盐中含碘酸钾。
①碘酸钾与碘化钾在酸性条件下发生如下反应,配平该反应的化学方程式:
 +
+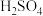 =
= +
+ +
+②上述反应生成的I2可用四氯化碳检验,现象为
向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
Na2SO3稀溶液与I2反应的离子方程式是
(2)海水提溴过程中溴元素的变化如下:

①过程I,海水显碱性,调其pH<3.5后,再通入氯气,调节海水pH可提高C12的利用率,用平衡原理解释其原因是
②过程II,用热空气将溴赶出,再用浓Na2CO3溶液吸收。完成并配平下列方程式。
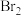 +
+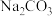 =
= +
+ +
+③过程III,用硫酸酸化可得Br2和Na2SO4的混合溶液。相同条件下,若用盐酸酸化,则所得溴的质量减少,原因是
④NaBrO3是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入 2.6molNaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:

则原溶液中NaI的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成下列问题。
(1)有下列四个反应:
①SO3+H2O=H2SO4 ②Cl2+H2O=HCl+HClO ③2F2+2H2O=4HF+O2 ④SO2+2NaOH=Na2SO3+H2O
上述反应中不属于氧化还原反应的是___________ (填序号,下同);H2O只作还原剂的是___________ ;属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是___________ 。
(2)工业盐的主要成分是NaNO2,以前有许多起因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有___________ 性。下列不能实现这种转化的物质是___________ (填字母)。
a.酸性KMnO4溶液 b.FeCl3 c.O2 d.浓硫酸
(3)已知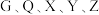 均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
①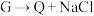 ②
②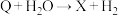 ③
③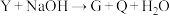 ④
④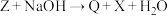
这五种化合物中 元素化合物由低到高的顺序是___________(填字母)
元素化合物由低到高的顺序是___________(填字母)
(4)已知氧化性Fe3+>Cu2+>Fe2+,在溶有Fe2(SO4)3和CuSO4的溶液中加入一定量的铁粉,下列说法正确的是___________。(填字母)
(5)我国古代炼丹术中用的铅丹与硝酸反应方程式是:X(铅丹)+4HNO3=PbO2+2Pb(NO3)2+2H2O,则铅丹的化学式为___________ ,其中+2价的Pb和+4价的Pb含量之比为:___________ 。
(6)治理汽车尾气方法之一是在汽车的排气管上安装“催化转化器”,CO和NO可以转化为两种无毒的气体,写出化学方程式并用单线桥标出电子转移的方向和数目:___________ 。
(1)有下列四个反应:
①SO3+H2O=H2SO4 ②Cl2+H2O=HCl+HClO ③2F2+2H2O=4HF+O2 ④SO2+2NaOH=Na2SO3+H2O
上述反应中不属于氧化还原反应的是
(2)工业盐的主要成分是NaNO2,以前有许多起因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
a.酸性KMnO4溶液 b.FeCl3 c.O2 d.浓硫酸
(3)已知
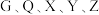 均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):①
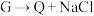 ②
②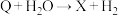 ③
③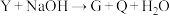 ④
④
这五种化合物中
 元素化合物由低到高的顺序是___________(填字母)
元素化合物由低到高的顺序是___________(填字母)| A.G、Y、Q、Z、X | B.X、Z、Q、G、Y |
| C.X、Z、Q、Y、G | D.G、Q、Y、Z、X |
| A.若铁粉无剩余,且溶液中有Cu2+,则溶液中可能有Fe3+ |
| B.若铁粉无剩余,溶液中一定有Fe2+,一定无Cu2+ |
| C.若铁粉有剩余,则不溶物一定有铜 |
| D.若铁粉有剩余,则溶液中一定有Fe2+和Cu2+ |
(6)治理汽车尾气方法之一是在汽车的排气管上安装“催化转化器”,CO和NO可以转化为两种无毒的气体,写出化学方程式并用单线桥标出电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】亚硝酸钠既有氧化性也有还原性,易溶于水,水溶液显碱性。由于NaNO2有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放,处理方法之一如下:NaNO2 +KI+_____ NO↑+I2+K2SO4+Na2SO4+___________。请回答下列问题:
NO↑+I2+K2SO4+Na2SO4+___________。请回答下列问题:
(1)配平上述化学方程式,请写出其完整方程式___________ 。
(2)鉴于NO是有毒气体,从环保角度来讲,要处理NaNO2,可以选用以下试剂___________
A. FeCl2 B. H2O2 C. KMnO4 D. H2SO4
(3)根据信息,鉴别亚硝酸钠和氯化钠的简单方法是___________ 。
(4)已知亚硝酸钠与氯化铵反应生成氮气、氯化钠和水,写出该反应的化学方程式并用双线桥表示其电子转移的方向和数目:___________ 。
 NO↑+I2+K2SO4+Na2SO4+___________。请回答下列问题:
NO↑+I2+K2SO4+Na2SO4+___________。请回答下列问题:(1)配平上述化学方程式,请写出其完整方程式
(2)鉴于NO是有毒气体,从环保角度来讲,要处理NaNO2,可以选用以下试剂
A. FeCl2 B. H2O2 C. KMnO4 D. H2SO4
(3)根据信息,鉴别亚硝酸钠和氯化钠的简单方法是
(4)已知亚硝酸钠与氯化铵反应生成氮气、氯化钠和水,写出该反应的化学方程式并用双线桥表示其电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】中国科学院官方微信于2017年3月发表《灰霾专题》,提出灰霾中细颗粒物的成因,部分分析如图1所示。

(1)根据图1信息可以看出,下列哪种气体污染物不是由机动车行驶造成的_______
a.SO2 b.NOx c.VOCs d.NH3
(2)机动车大量行驶是污染源之一。汽车发动机废气稀燃控制系统主要工作原理如图2所示;写出稀燃过程中NO发生的主要反应的方程式_______ 。

(3)科学家经过研究发现中国霾呈中性,其主要原因如图3所示:
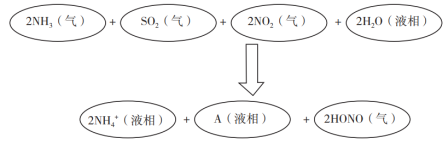
请推断A的化学式为_______ ,并说明理由:_______ 。
(4)在微生物作用下可实现NH →NO
→NO →NO
→NO 转化,称为硝化过程。在碱性条件下,NH
转化,称为硝化过程。在碱性条件下,NH 被氧气氧化为NO
被氧气氧化为NO 的反应离子方程式为
的反应离子方程式为_______ 。
(5)煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NOx的烟气通入盛有NaClO2溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):
①上述转化过程中表现氧化性的物质为_______ ,若该溶液为1000 mL(吸收前后溶液体积不变),该过程转移的电子数为_______ mol。
②表中y=_______ 。

(1)根据图1信息可以看出,下列哪种气体污染物不是由机动车行驶造成的
a.SO2 b.NOx c.VOCs d.NH3
(2)机动车大量行驶是污染源之一。汽车发动机废气稀燃控制系统主要工作原理如图2所示;写出稀燃过程中NO发生的主要反应的方程式

(3)科学家经过研究发现中国霾呈中性,其主要原因如图3所示:

请推断A的化学式为
(4)在微生物作用下可实现NH
 →NO
→NO →NO
→NO 转化,称为硝化过程。在碱性条件下,NH
转化,称为硝化过程。在碱性条件下,NH 被氧气氧化为NO
被氧气氧化为NO 的反应离子方程式为
的反应离子方程式为(5)煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NOx的烟气通入盛有NaClO2溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):
| 离子 | Na+ | SO | NO | H+ | Cl- |
| 浓度/(mol/L) | 5.5×10-3 | y | 6.0×10-4 | 2.0×10-4 | 3.4×10-3 |
①上述转化过程中表现氧化性的物质为
②表中y=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“价-类”二维图具有直观、线索清晰、引导性强等特点,有利于提高统筹思维和概括能力。氮元素的化合价与部分常见含氮物质类别的“价-类”二维图如图所示。

请回答下列问题:
(1)实验室中制备气体A的化学方程式为___________ ;气体A与氧气在红热的铂丝作用下生成D的化学方程式为___________ ,撤去热源后,铂丝继续保持红热的原因是___________ 。
(2)D与A在加热、催化剂作用下能反应生成B和另一种对环境无害的产物,请写出该反应的化学方程式:___________ 。E为红棕色气体,则E的化学式为___________ 。
(3)57.6gCu与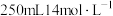 浓硝酸反应,铜全部被消耗后,共收集到D和E的混合气体1mol(不考虑
浓硝酸反应,铜全部被消耗后,共收集到D和E的混合气体1mol(不考虑 的存在),则D、E的物质的量之比是
的存在),则D、E的物质的量之比是___________ ,将该混合气体与足量的水反应后,剩余气体的体积为___________ L(标准状况下)。

请回答下列问题:
(1)实验室中制备气体A的化学方程式为
(2)D与A在加热、催化剂作用下能反应生成B和另一种对环境无害的产物,请写出该反应的化学方程式:
(3)57.6gCu与
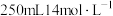 浓硝酸反应,铜全部被消耗后,共收集到D和E的混合气体1mol(不考虑
浓硝酸反应,铜全部被消耗后,共收集到D和E的混合气体1mol(不考虑 的存在),则D、E的物质的量之比是
的存在),则D、E的物质的量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】工业或机动车尾气中的NOx会造成环境问题,可用多种方法脱除。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含NO、NO2),获得副产品NaNO2。
①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为___________ 。
②若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到NaNO2晶体中最有可能混有的杂质是___________ (填化学式)。排放的尾气中含量较高的氮氧化物是___________ (填化学式)。
(2)还原法:尿素水溶液热解产生的NH3可去除尾气中的NOx,流程如下:

①尿素[CO(NH2)2]中氮元素的化合价为___________ 。
②写出“催化反应”过程中NH3还原NO2的化学方程式___________ 。
③若氧化处理后的尾气中混有SO2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低NOx的去除率。试分析硫酸盐的产生过程___________ 。
④“催化反应”过程中需控制温度在250℃~380℃之间。温度过高,NH3发生催化氧化反应,写出该化学方程式___________ 。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含NO、NO2),获得副产品NaNO2。
①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为
②若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到NaNO2晶体中最有可能混有的杂质是
(2)还原法:尿素水溶液热解产生的NH3可去除尾气中的NOx,流程如下:

①尿素[CO(NH2)2]中氮元素的化合价为
②写出“催化反应”过程中NH3还原NO2的化学方程式
③若氧化处理后的尾气中混有SO2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低NOx的去除率。试分析硫酸盐的产生过程
④“催化反应”过程中需控制温度在250℃~380℃之间。温度过高,NH3发生催化氧化反应,写出该化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】A是一种酸式盐,它与 溶液共热,放出无色气体B,用圆底烧瓶收集干燥的气体B,按如图所示装置进行喷泉实验,挤压胶头滴管,可得到蓝色喷泉。若向A中加入稀盐酸,产生的无色气体C能使品红溶液褪色。
溶液共热,放出无色气体B,用圆底烧瓶收集干燥的气体B,按如图所示装置进行喷泉实验,挤压胶头滴管,可得到蓝色喷泉。若向A中加入稀盐酸,产生的无色气体C能使品红溶液褪色。

请回答下列问题:
(1)A的化学式为_______ 。
(2) 大气污染物之一,气体B与
大气污染物之一,气体B与 在加热和催化剂作用下可以生产
在加热和催化剂作用下可以生产 ,写出相关化学方程式
,写出相关化学方程式_______ ,收集气体B的方法是_______ 。
(3)写出反应A→C的离子方程式:_______ 。
(4)A与过量 溶液共热反应的离子方程式为
溶液共热反应的离子方程式为_______ 。
 溶液共热,放出无色气体B,用圆底烧瓶收集干燥的气体B,按如图所示装置进行喷泉实验,挤压胶头滴管,可得到蓝色喷泉。若向A中加入稀盐酸,产生的无色气体C能使品红溶液褪色。
溶液共热,放出无色气体B,用圆底烧瓶收集干燥的气体B,按如图所示装置进行喷泉实验,挤压胶头滴管,可得到蓝色喷泉。若向A中加入稀盐酸,产生的无色气体C能使品红溶液褪色。
请回答下列问题:
(1)A的化学式为
(2)
 大气污染物之一,气体B与
大气污染物之一,气体B与 在加热和催化剂作用下可以生产
在加热和催化剂作用下可以生产 ,写出相关化学方程式
,写出相关化学方程式(3)写出反应A→C的离子方程式:
(4)A与过量
 溶液共热反应的离子方程式为
溶液共热反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某学习小组欲制取氨气并探究其性质。请回答:
(1)实验室利用固体与固体反应制取氨气的化学方程式是___________ 。
(2)①如图是进行氨气喷泉实验的装置,引发喷泉的操作步骤是___________ 。
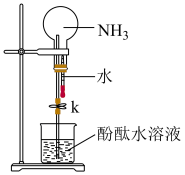
②氨气使烧杯中溶液由无色变为红色,其原因是(用方程式表示)___________ 。
(3)在上图的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是___________。
(1)实验室利用固体与固体反应制取氨气的化学方程式是
(2)①如图是进行氨气喷泉实验的装置,引发喷泉的操作步骤是

②氨气使烧杯中溶液由无色变为红色,其原因是(用方程式表示)
(3)在上图的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是___________。
A.HCl和 | B. 和 和 | C. 和苯 和苯 | D. 和烧碱溶液。 和烧碱溶液。 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁是生活中常用的金属,利用铁的相关知识回答下列相关问题。
(1)生活中常使用铁锅炒菜,所利用的金属的物理性质是_______ 。
(2)在食品的包装袋中,经常放一小袋颗粒极细的铁粉,俗称“双吸粉”。铁粉能够吸收的物质是_______ (填写化学式)。
(3)铁的氧化物之一氧化铁的用途有_______ (写出一种),将少量的氧化铁固体加入到氢碘酸中,发生反应的离子方程式是_______ 。
(4)将一定量的 、
、 和
和 的混合物放入体积为
的混合物放入体积为 ,浓度为
,浓度为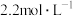 的
的 溶液中,充分反应后,生成气体
溶液中,充分反应后,生成气体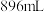 (标准状况),得到不溶固体
(标准状况),得到不溶固体 。过滤后,滤液中的金属离子只有
。过滤后,滤液中的金属离子只有 (假设滤液体积仍为
(假设滤液体积仍为 )。向滤液中加入
)。向滤液中加入 溶液至
溶液至 时开始出现沉淀。则未滴加
时开始出现沉淀。则未滴加 溶液前滤液中
溶液前滤液中 的物质的量浓度为
的物质的量浓度为_______ 。
(5)已知稀硝酸具有强氧化性,通常被还原成 ,向一定量的稀硝酸中加入足量的铁粉,发生氧化还原反应,写出对应的离子反应方程式
,向一定量的稀硝酸中加入足量的铁粉,发生氧化还原反应,写出对应的离子反应方程式_______ 。
(6)绿矾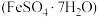 受热分解可以生成氧化铁、二氧化硫、三氧化硫、水。取少量绿矾固体加热一段时间后,某同学欲检验绿矾是否完全分解,取分解后的固体样品少许溶解在稀硫酸中,然后取样加入检验试剂,该同学需要用到的检验试剂是
受热分解可以生成氧化铁、二氧化硫、三氧化硫、水。取少量绿矾固体加热一段时间后,某同学欲检验绿矾是否完全分解,取分解后的固体样品少许溶解在稀硫酸中,然后取样加入检验试剂,该同学需要用到的检验试剂是_______ 。(写出检验试剂名称)
(1)生活中常使用铁锅炒菜,所利用的金属的物理性质是
(2)在食品的包装袋中,经常放一小袋颗粒极细的铁粉,俗称“双吸粉”。铁粉能够吸收的物质是
(3)铁的氧化物之一氧化铁的用途有
(4)将一定量的
 、
、 和
和 的混合物放入体积为
的混合物放入体积为 ,浓度为
,浓度为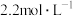 的
的 溶液中,充分反应后,生成气体
溶液中,充分反应后,生成气体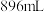 (标准状况),得到不溶固体
(标准状况),得到不溶固体 。过滤后,滤液中的金属离子只有
。过滤后,滤液中的金属离子只有 (假设滤液体积仍为
(假设滤液体积仍为 )。向滤液中加入
)。向滤液中加入 溶液至
溶液至 时开始出现沉淀。则未滴加
时开始出现沉淀。则未滴加 溶液前滤液中
溶液前滤液中 的物质的量浓度为
的物质的量浓度为(5)已知稀硝酸具有强氧化性,通常被还原成
 ,向一定量的稀硝酸中加入足量的铁粉,发生氧化还原反应,写出对应的离子反应方程式
,向一定量的稀硝酸中加入足量的铁粉,发生氧化还原反应,写出对应的离子反应方程式(6)绿矾
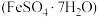 受热分解可以生成氧化铁、二氧化硫、三氧化硫、水。取少量绿矾固体加热一段时间后,某同学欲检验绿矾是否完全分解,取分解后的固体样品少许溶解在稀硫酸中,然后取样加入检验试剂,该同学需要用到的检验试剂是
受热分解可以生成氧化铁、二氧化硫、三氧化硫、水。取少量绿矾固体加热一段时间后,某同学欲检验绿矾是否完全分解,取分解后的固体样品少许溶解在稀硫酸中,然后取样加入检验试剂,该同学需要用到的检验试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
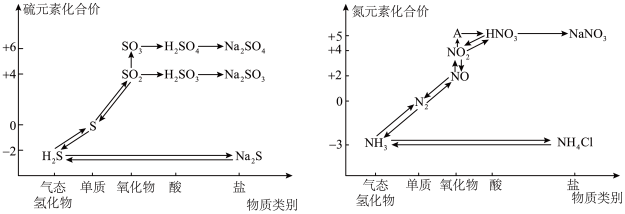
【推荐2】硫、氮的氧化物都会引起环境问题,越来越引起人们的重视。如图是硫、氮元素的各种价态与物质类别的对应关系:
(1)从硫元素的化合价变化的角度判断,图中只有还原性的含硫化合物为_________ 。
(2)写出浓硫酸与木炭在加热条件下反应的化学方程式:_________________________ ;若要除去 中的
中的 可以使用
可以使用_________ (填试剂名称)。
(3)根据A对应的化合价和物质类别,A为_________ (写分子式)。
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择_________ ,反应的离子方程式为__________________ 。
(5)工业生产中利用氨水吸收 和
和 ,流程如图所示:
,流程如图所示: 被吸收过程的离子方程式是
被吸收过程的离子方程式是_______________________ 。
(6)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下: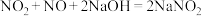
 ;
; 。现有V L某NaOH溶液能完全吸收含m mol NO和n mol
。现有V L某NaOH溶液能完全吸收含m mol NO和n mol  的大气污染物,则NaOH溶液的物质的量浓度至少为
的大气污染物,则NaOH溶液的物质的量浓度至少为________  。若所得溶液
。若所得溶液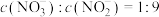 ,则原混合气体中NO和
,则原混合气体中NO和 物质的量之比m∶n=
物质的量之比m∶n=_____ 。
(1)从硫元素的化合价变化的角度判断,图中只有还原性的含硫化合物为
(2)写出浓硫酸与木炭在加热条件下反应的化学方程式:
 中的
中的 可以使用
可以使用(3)根据A对应的化合价和物质类别,A为
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
(5)工业生产中利用氨水吸收
 和
和 ,流程如图所示:
,流程如图所示: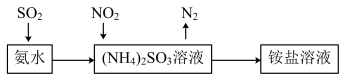
 被吸收过程的离子方程式是
被吸收过程的离子方程式是(6)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
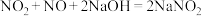
 ;
; 。现有V L某NaOH溶液能完全吸收含m mol NO和n mol
。现有V L某NaOH溶液能完全吸收含m mol NO和n mol  的大气污染物,则NaOH溶液的物质的量浓度至少为
的大气污染物,则NaOH溶液的物质的量浓度至少为 。若所得溶液
。若所得溶液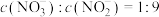 ,则原混合气体中NO和
,则原混合气体中NO和 物质的量之比m∶n=
物质的量之比m∶n=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:

回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是______________________ ,还可使用________ 代替硝酸。
(2)沉淀A的主要成分是________ ,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为_______________________________ 。

回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
(2)沉淀A的主要成分是
您最近一年使用:0次



