某温度下,纯水中的c平(H+)=2×10-7 mol/L,则此时c平(OH-)=___________ 。若温度不变,滴入稀盐酸使c平(H+)=5×10-6 mol/L,则c平(OH-)=___________ ,由水电离出的c平(H+)为___________ 。
更新时间:2023-08-27 16:20:53
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某温度下纯水的pH=7,按要求回答下列问题:
(1)pH=7的溶液呈_______ (填“酸性”“中性”或“碱性”)。
(2)该温度下某溶液中由水电离出的c(OH-)=10-9mol/L的pH=_______ 。
(3)pH=3的H2SO4溶液与pH=6的HCl溶液的等体积混合,溶液的pH=_______ 。
(4)将pH=2的盐酸和pH=11的氢氧化钠溶液,以体积比1∶9混合后,溶液的pH=_______ 。
(1)pH=7的溶液呈
(2)该温度下某溶液中由水电离出的c(OH-)=10-9mol/L的pH=
(3)pH=3的H2SO4溶液与pH=6的HCl溶液的等体积混合,溶液的pH=
(4)将pH=2的盐酸和pH=11的氢氧化钠溶液,以体积比1∶9混合后,溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
(1)常温下,用0.01 mol·L-1的NaOH溶液滴定10 mL0.01 mol·L-1的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
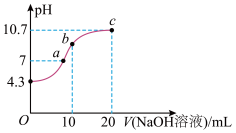
①写出H2N2O2在水溶液中的电离方程式:_____________________________ 。
②b点时溶液中c(H2N2O2)________ (填“>”“<”或“=”)c(N2O )。
)。
③a点时溶液中 c(Na+)_________ (填“>”“<”或“=”)c(HN2O )+c(N2O
)+c(N2O )。
)。
(2)温度为T℃时水的离子积常数为Kw,该温度下,将浓度为a mol·L-1的H2SO4与b mol·L-1的一元碱AOH等体积混合。则可判断溶液呈中性的是________ (填序号)。
①混合溶液的pH ②c( )=
)= c(A+)
c(A+)
③混合溶液中c(H+)·c(OH-)=Kw ④混合溶液中c(OH-)=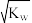
(1)常温下,用0.01 mol·L-1的NaOH溶液滴定10 mL0.01 mol·L-1的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。

①写出H2N2O2在水溶液中的电离方程式:
②b点时溶液中c(H2N2O2)
 )。
)。 ③a点时溶液中 c(Na+)
 )+c(N2O
)+c(N2O )。
)。(2)温度为T℃时水的离子积常数为Kw,该温度下,将浓度为a mol·L-1的H2SO4与b mol·L-1的一元碱AOH等体积混合。则可判断溶液呈中性的是
①混合溶液的pH ②c(
 )=
)= c(A+)
c(A+)③混合溶液中c(H+)·c(OH-)=Kw ④混合溶液中c(OH-)=
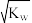
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知水在25 ℃和95 ℃时,水电离平衡曲线如图所示:
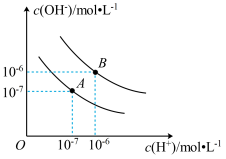
(1)95 ℃时,水的电离平衡曲线应为B,请说明理由:_______________________________ 。25 ℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为____________ 。
(2)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1________ (填“大于”“小于”“等于”或“无法确定”)α2。
(3)曲线B对应温度下,将0.02 mol·L-1Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合后,混合溶液的pH=________ 。

(1)95 ℃时,水的电离平衡曲线应为B,请说明理由:
(2)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1
(3)曲线B对应温度下,将0.02 mol·L-1Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合后,混合溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某温度下纯水中的c(H+)=2×10-7mol/L,则此时溶液中的c(OH-)=____ ;在该温度下,0.04mol/L的NaOH溶液的pH=____ ;该温度下,某溶液中由水电离产生的[OH-]和[H+]的乘积为1.6×10-17,则该溶液的pH=____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是不同温度下水的离子积常数:
试回答以下问题:
(1)若25℃<T1<T2,则a___________ 1×10-14(填“>”、“<”或“=”),做此判断的理由是___________ 。
(2)25℃时,某Na2SO4溶液中c(SO )=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=
)=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=___________ 。
(3)若T2温度下,向水中滴入稀盐酸,测得溶液中c(H+)=1.0×10-3mol/L,则溶液中c(OH-)=___________ mol/L。
| 温度/℃ | 25 | T1 | T2 |
| 水的离子积常数 | 1×10-14 | a | 1×10-12 |
(1)若25℃<T1<T2,则a
(2)25℃时,某Na2SO4溶液中c(SO
 )=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=
)=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=(3)若T2温度下,向水中滴入稀盐酸,测得溶液中c(H+)=1.0×10-3mol/L,则溶液中c(OH-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)某温度(t ℃)时,水的Kw=1×10-12,则该温度_______ 25 ℃(填“>”、“<”或“=”),其理由是_______ 。
(2)该温度下,c(H+)=1×10-7 mol·L-1的溶液呈_______ (填“酸性”、“碱性”或“中性”);若该溶液中只存在NaOH溶质,则由H2O电离出来的c(OH-)=_______ mol·L-1。
(3)若在25 ℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH与强碱的pH之间应满足的关系是_______ 。
(1)某温度(t ℃)时,水的Kw=1×10-12,则该温度
(2)该温度下,c(H+)=1×10-7 mol·L-1的溶液呈
(3)若在25 ℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH与强碱的pH之间应满足的关系是
您最近一年使用:0次



