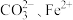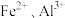下列说法正确的是
| A.金属原子失电子越多,其还原性越强 |
| B.已知①Fe+Cu2+=Fe2++Cu;②2Fe3++Cu=2Fe2++Cu2+,则氧化性强弱顺序为:Fe3+>Cu2+>Fe2+ |
| C.氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 |
| D.非金属单质在反应中即可作氧化剂又可作还原剂 |
更新时间:2023-07-30 20:32:59
|
相似题推荐
【推荐1】对于白磷引起的中毒,硫酸铜溶液是一种解毒剂,有关反应如下:P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平),关于该反应下列说法正确的是
| A.CuSO4既不作氧化剂,也不作还原剂 |
| B.11个P被氧化时,该反应中有30个电子发生转移 |
| C.氧化性:CuSO4>H3PO4 |
| D.该反应的氧化剂和还原剂的个数之比为10:3 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3===K2O+5Na2O+16N2↑。有关该反应,下列叙述正确的是
| A.上述反应中KNO3是还原剂 |
| B.每生成1.6molN2,转移的电子为1 mol |
| C.NaN3中N的化合价为-3 |
| D.若被氧化的N原子的物质的量为3mol,则氧化产物比还原产物多1.4 mol |
您最近一年使用:0次
【推荐3】氰化物是剧毒物质,传统生产工艺的电镀废水中含一定浓度的CN-,无害化排放时必须对这种废水进行处理。 可采用碱性条件下的Cl2氧化法处理这种废水,涉及两个反应:反应i,CN- +OH-+Cl2 OCN- +Cl-+H2O(未配平);
OCN- +Cl-+H2O(未配平);
反应ii,OCN- + OH-+ Cl2 X + Y + Cl-+ H2O(未配平)。
X + Y + Cl-+ H2O(未配平)。
其中反应i中N元素的化合价没有变化,常温下,X、Y是两种无毒的气体。下列判断正确的是
 OCN- +Cl-+H2O(未配平);
OCN- +Cl-+H2O(未配平);反应ii,OCN- + OH-+ Cl2
 X + Y + Cl-+ H2O(未配平)。
X + Y + Cl-+ H2O(未配平)。其中反应i中N元素的化合价没有变化,常温下,X、Y是两种无毒的气体。下列判断正确的是
| A.反应i中氧化剂与还原剂的化学计量数之比为1: 1 |
| B.X、Y是CO2、N2,且均为反应ii的氧化产物 |
| C.该废水处理工艺过程中须采取措施,防止Cl2逸出到空气中 |
| D.处理c(CN-) =0.000 1 mol·L-1的废水106 L,消耗标况下的Cl2 4.48×103L |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】铅位于ⅣA族,PbO偏碱性,易溶于硝酸,PbO2偏酸性,难溶于硝酸。
已知:PbS与稀HNO3发生反应Ⅰ:3PbS+8HNO3(稀)=3Pb(NO3)2+3S↓+2NO↑+4H2O;
PbS与浓HNO3发生反应Ⅱ:PbS+8HNO3(浓)=PbSO4+8NO2↑+4H2O。
下列推断正确的是( )
已知:PbS与稀HNO3发生反应Ⅰ:3PbS+8HNO3(稀)=3Pb(NO3)2+3S↓+2NO↑+4H2O;
PbS与浓HNO3发生反应Ⅱ:PbS+8HNO3(浓)=PbSO4+8NO2↑+4H2O。
下列推断正确的是( )
| A.Pb3O4与HNO3溶液发生反应:Pb3O4+4H+=PbO2+2Pb2++2H2O |
| B.由反应Ⅰ、Ⅱ可知,氧化性:HNO3(浓)>HNO3(稀)>PbO2 |
| C.反应Ⅰ若生成4.48LNO,转移0.6NA电子 |
D.S可以与浓硝酸反应:S+6HNO3(浓) H2SO4+6NO2↑+2H2O H2SO4+6NO2↑+2H2O |
您最近一年使用:0次
【推荐2】高铁酸钾(K2FeO4)是一种既能杀菌、消毒,又能絮凝净水的水处理剂,工业制备高铁酸钾的反应离子方程式为Fe(OH)3+ClO-+OH-→ +Cl-+H2O(未配平)。下列有关说法不正确的是
+Cl-+H2O(未配平)。下列有关说法不正确的是
 +Cl-+H2O(未配平)。下列有关说法不正确的是
+Cl-+H2O(未配平)。下列有关说法不正确的是A.由上述反应可知,ClO-的氧化性强于 |
| B.高铁酸钾中铁显+4价 |
| C.上述反应中氧化剂和还原剂的物质的量之比为2∶3 |
| D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+与水反应形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
您最近一年使用:0次
多选题
|
适中
(0.64)
【推荐3】根据表中信息,判断下列叙述中正确的是 ( )。
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Fe3+、Br2 | |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| A.由表中①组的信息可知通入Cl2的量不同,氧化产物可能不同 |
| B.氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2 |
| C.表中②组反应的还原产物是KCl,电子转移数目是6e- |
| D.表中③组反应的离子方程式为2MnO4—+5H2O2+6H+=2Mn2++5O2↑+8H2O |
您最近一年使用:0次
【推荐1】含氰化物的废液乱倒或与酸混合,均易生成有剧毒且易挥发的氰化氢。工业上,常采用碱性氯化法( 过量)来处理高浓度氰化物污水,将废水中的有害物质转化为无毒物质,发生的总反应为
过量)来处理高浓度氰化物污水,将废水中的有害物质转化为无毒物质,发生的总反应为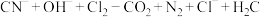 (未配平)。下列说法正确的是
(未配平)。下列说法正确的是
 过量)来处理高浓度氰化物污水,将废水中的有害物质转化为无毒物质,发生的总反应为
过量)来处理高浓度氰化物污水,将废水中的有害物质转化为无毒物质,发生的总反应为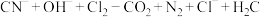 (未配平)。下列说法正确的是
(未配平)。下列说法正确的是A.还原性: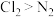 |
| B.氧化剂、还原剂的物质的量之比为5∶2 |
C.该反应中,每生成1mol  转移2mol电子 转移2mol电子 |
D.若将该反应设计成原电池,则 在负极区生成 在负极区生成 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】已知有如下反应:
①
②
③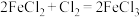
根据上述反应,判断下列结论中错误的是
①

②

③
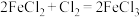
根据上述反应,判断下列结论中错误的是
A. 是在反应②中既是氧化产物又是还原产物 是在反应②中既是氧化产物又是还原产物 |
B. 在①、③反应中均作氧化剂 在①、③反应中均作氧化剂 |
C.氧化性强弱的顺序为: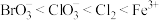 |
D.溶液中可能发生: |
您最近一年使用:0次

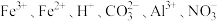 六种离子中的几种,向溶液中逐滴加入一定量1mol/L的NaOH溶液的过程中,开始没有沉淀,而后有沉淀.下列判断
六种离子中的几种,向溶液中逐滴加入一定量1mol/L的NaOH溶液的过程中,开始没有沉淀,而后有沉淀.下列判断