铅位于ⅣA族,PbO偏碱性,易溶于硝酸,PbO2偏酸性,难溶于硝酸。
已知:PbS与稀HNO3发生反应Ⅰ:3PbS+8HNO3(稀)=3Pb(NO3)2+3S↓+2NO↑+4H2O;
PbS与浓HNO3发生反应Ⅱ:PbS+8HNO3(浓)=PbSO4+8NO2↑+4H2O。
下列推断正确的是( )
已知:PbS与稀HNO3发生反应Ⅰ:3PbS+8HNO3(稀)=3Pb(NO3)2+3S↓+2NO↑+4H2O;
PbS与浓HNO3发生反应Ⅱ:PbS+8HNO3(浓)=PbSO4+8NO2↑+4H2O。
下列推断正确的是( )
| A.Pb3O4与HNO3溶液发生反应:Pb3O4+4H+=PbO2+2Pb2++2H2O |
| B.由反应Ⅰ、Ⅱ可知,氧化性:HNO3(浓)>HNO3(稀)>PbO2 |
| C.反应Ⅰ若生成4.48LNO,转移0.6NA电子 |
D.S可以与浓硝酸反应:S+6HNO3(浓) H2SO4+6NO2↑+2H2O H2SO4+6NO2↑+2H2O |
20-21高三上·山东青岛·阶段练习 查看更多[2]
更新时间:2020-10-27 17:50:43
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】酸性 溶液和CuS混合时,发生的反应如下:
溶液和CuS混合时,发生的反应如下: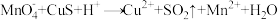 (未配平),下列有关该反应的说法中正确的是
(未配平),下列有关该反应的说法中正确的是
 溶液和CuS混合时,发生的反应如下:
溶液和CuS混合时,发生的反应如下: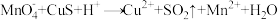 (未配平),下列有关该反应的说法中正确的是
(未配平),下列有关该反应的说法中正确的是| A.被氧化的元素是Cu和S |
B. 的氧化性强于SO2的氧化性 的氧化性强于SO2的氧化性 |
| C.还原产物与氧化产物的物质的量之比为5:6 |
| D.若生成1.12L (标准状况下) SO2,转移电子的物质的量是0.3mol |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.金属原子失电子越多,其还原性越强 |
| B.已知①Fe+Cu2+=Fe2++Cu;②2Fe3++Cu=2Fe2++Cu2+,则氧化性强弱顺序为:Fe3+>Cu2+>Fe2+ |
| C.氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 |
| D.非金属单质在反应中即可作氧化剂又可作还原剂 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】下列反应的离子方程式正确的是
| A.向100mL0.1mol/LFeBr2溶液中通入0.025mol的Cl2 ,充分反应2Fe2++4Br-+3Cl2→2Fe3++2Br2+6Cl- |
| B.向Fe(NO3)3溶液中加入过量的HI溶液 2NO3-+8H++6I-→3I2+2NO↑+4H2O |
| C.将碳与足量的浓硫酸共热反应后的气体混合物,通入过量氢氧化钠溶液中CO2+SO2+4OH-→SO32-+CO32-+2H2O |
| D.将等体积等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合HCO-3+Ba2++OH-→BaCO3↓+H2O |
您最近一年使用:0次
【推荐2】高铁酸钾是一种新型、高效、多功能水处理剂,工业上采用向 KOH 溶液中通入氯气,然后再加入Fe(NO3)3溶液的方法制备 K2FeO4,发生反应:①Cl2+KOH→KCl+KClO+KClO3+H2O(未配平);②2Fe(NO3)3+3KClO+10KOH=2K2FeO4+6KNO3+3KCl+5H2O。下列说法正确的是
| A.反应①中每消耗4个KOH,会吸收2个Cl2 |
| B.氧化性:K2FeO4>KClO |
C.若反应①中ClO-与 个数比为 5:1,则氧化剂与还原剂的个数之比为 5:3 个数比为 5:1,则氧化剂与还原剂的个数之比为 5:3 |
| D.若反应①的氧化产物只有KClO,则得到2个 K2FeO4时消耗6个Cl2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】碘量法测定水中的溶解氧的步骤如下;①氧的固定∶101 kPa、25℃时,取 100.00mL水样与 Mn(OH)2碱性悬浊液(含 KI)混合,反应生成 MnO(OH)2;②酸化、滴定∶将固氧后的水样用适量稀硫酸酸化,MnO(OH)2被 I-还原为 Mn2+,在暗处静置5min,然后用amol·L-1  标准液滴定(
标准液滴定( ),达到滴定终点时消耗
),达到滴定终点时消耗 标准液 b mL。下列说法正确的是
标准液 b mL。下列说法正确的是
 标准液滴定(
标准液滴定( ),达到滴定终点时消耗
),达到滴定终点时消耗 标准液 b mL。下列说法正确的是
标准液 b mL。下列说法正确的是| A.氧的固定时,每固定 16mgO2转移电子的物质的量为4×10-3mol |
B.酸化时主要反应的离子方程式为∶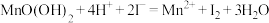 |
| C.滴定时溶液酸性太强,所测水样中溶解氧的含量偏低 |
| D.水样中溶解氧的含量为 80ab mg·L-1 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】用以下三种途径来制取等质量的硝酸铜。
①铜与稀硝酸反应;②铜与浓硝酸反应;③铜先与氧气反应生成氧化铜,氧化铜再与硝酸反应。以下叙述不正确的是
①铜与稀硝酸反应;②铜与浓硝酸反应;③铜先与氧气反应生成氧化铜,氧化铜再与硝酸反应。以下叙述不正确的是
| A.三种途径所消耗铜的质量相等 |
| B.三种途径所消耗硝酸的物质的量是①>②>③ |
| C.途径③的制备方法最符合“绿色化学“理念 |
| D.途径①中还原剂与氧化剂的物质的量之比是3: 8 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
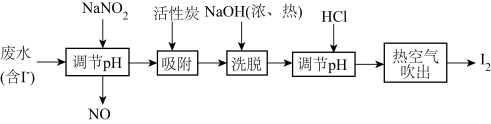
【推荐2】生活污水中的氮和磷主要以铵盐和磷酸盐的形式存在,可用电解法从溶液中除去。有Cl-存在时。除氮原理如图1所示。主要依靠有效氯(HClO、ClO-)将 或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度与溶液pH的关系如图2所示。
或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度与溶液pH的关系如图2所示。

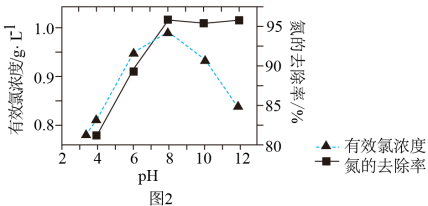
下列说法不正确的是
 或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度与溶液pH的关系如图2所示。
或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度与溶液pH的关系如图2所示。

下列说法不正确的是
| A.pH=3时,主要发生ClO-氧化NH3的反应 |
| B.pH>8时,有效氯浓度随pH的增大而增大 |
C.pH>8时, 转变为NH3·H2O,且有利于NH3逸出 转变为NH3·H2O,且有利于NH3逸出 |
| D.pH<8时,氮的去除率随pH的减少而下降的原因是c(HClO)减小 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】向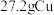 和
和 的混合物中加入某浓度的稀硝酸
的混合物中加入某浓度的稀硝酸 ,固体物质完全反应,生成
,固体物质完全反应,生成 和
和 。向所得溶液中加入
。向所得溶液中加入 的
的 溶液
溶液 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列说法正确的是
。下列说法正确的是
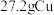 和
和 的混合物中加入某浓度的稀硝酸
的混合物中加入某浓度的稀硝酸 ,固体物质完全反应,生成
,固体物质完全反应,生成 和
和 。向所得溶液中加入
。向所得溶液中加入 的
的 溶液
溶液 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列说法正确的是
。下列说法正确的是A. 和 和 的物质的量之比为 的物质的量之比为 |
B.产生的 的体积为 的体积为 |
C.原硝酸的物质的量浓度为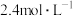 |
D. 和 和 与硝酸反应后剩余的 与硝酸反应后剩余的 的物质的量浓度为 的物质的量浓度为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列关于氮及其化合物的说法错误的是
| A.NO2与水反应生成HNO3,但NO2不属于酸性氧化物 |
| B.某盐与强碱的浓溶液混合加热,产生的气体遇HCl气体冒白烟,可证明是铵盐 |
| C.浓硝酸与铜或碳反应时均体现其酸性和强氧化性 |
D.加热NH4Cl和 的固体混合物,可用CaCl2干燥生成的气体 的固体混合物,可用CaCl2干燥生成的气体 |
您最近一年使用:0次

 +10Z-+16H+=2X2++5Z2+8H2O,根据上述反应,判断下列结论中正确的是
+10Z-+16H+=2X2++5Z2+8H2O,根据上述反应,判断下列结论中正确的是 、
、 和
和 混合溶液中的
混合溶液中的
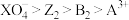
 是
是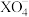 的氧化产物,
的氧化产物,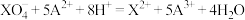
 计测定
计测定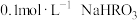 溶液的
溶液的
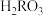 为二元酸
为二元酸 晶体溶解于稀硫酸后,滴加
晶体溶解于稀硫酸后,滴加 溶液
溶液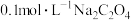 溶液中滴加等体积的
溶液中滴加等体积的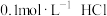 溶液
溶液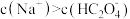

 淀粉试纸上滴2滴某黄色溶液
淀粉试纸上滴2滴某黄色溶液


