用化学知识解答问题:
(1)铜器在潮湿的空气中,表面会慢慢地生成一层铜锈(碱式碳酸铜),该反应的化学方程式为___________ 。
(2)在日常生活中常用一些铝制器皿,在清洗铝制器皿表面的污垢时,不能使用热的碱性溶液的原因时(用化学方程式解释)___________ 。
(3)发射卫星的火箭用联氨( )作燃料,以四氧化二氮作氧化剂,燃烧尾气由氮气与水蒸气组成,该反应的化学方程式为
)作燃料,以四氧化二氮作氧化剂,燃烧尾气由氮气与水蒸气组成,该反应的化学方程式为___________ 。
(4)比较甲酸、乙酸、丙酸的酸性大小,并解释原因___________
(5)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
比较两元素的 、
、 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是___________ 。
(1)铜器在潮湿的空气中,表面会慢慢地生成一层铜锈(碱式碳酸铜),该反应的化学方程式为
(2)在日常生活中常用一些铝制器皿,在清洗铝制器皿表面的污垢时,不能使用热的碱性溶液的原因时(用化学方程式解释)
(3)发射卫星的火箭用联氨(
 )作燃料,以四氧化二氮作氧化剂,燃烧尾气由氮气与水蒸气组成,该反应的化学方程式为
)作燃料,以四氧化二氮作氧化剂,燃烧尾气由氮气与水蒸气组成,该反应的化学方程式为(4)比较甲酸、乙酸、丙酸的酸性大小,并解释原因
(5)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
电离能/ |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
 、
、 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是
更新时间:2023-08-19 19:26:01
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.单选题
(1) 溶液中通入适量
溶液中通入适量 ,反应的离子方程式为
,反应的离子方程式为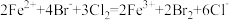 。下列各离子的电子排布式正确的是
。下列各离子的电子排布式正确的是
(2)下列各组比较中,正确的是
(3)已知 的结构为
的结构为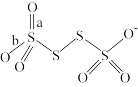 ,下列叙述不正确的是
,下列叙述不正确的是
Ⅱ.非选择题
结构决定性质,研究元素及物质的结构和性质是化学工作者永恒的课题。
(4) 原子核外共有
原子核外共有___________ 种运动状态不同的电子,其基态原子的电子排布式为___________ ,最高能层电子的电子云轮廓形状为___________ 。
(5)我国科学家屠呦呦以研究“青蒿素”获诺贝尔奖。青蒿素的结构简式如图所示,其组成元素的电负性由大到小的顺序为___________ 。
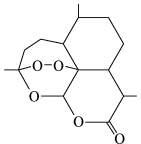
(6)已知,可用异氰酸苯酯与 氯
氯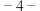 氨基吡啶反应生成氯吡苯脲:
氨基吡啶反应生成氯吡苯脲:
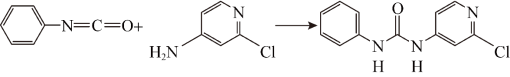
反应过程中,每生成 氯吡苯脲,断裂
氯吡苯脲,断裂___________  键,断裂
键,断裂___________  键。
键。
(7)计算: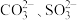 的中心原子上的孤电子对数分别是
的中心原子上的孤电子对数分别是___________ 、___________ 。
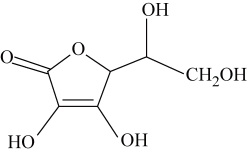
(8)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为___________ ;推测抗坏血酸在水中的溶解性:___________ (填“难溶”或“易溶”)于水;坏血酸分子___________ (填“是”或“不是”)手性分子。
(1)
 溶液中通入适量
溶液中通入适量 ,反应的离子方程式为
,反应的离子方程式为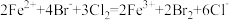 。下列各离子的电子排布式正确的是
。下列各离子的电子排布式正确的是A. 为 为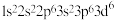 | B. 为 为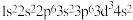 |
C. 为 为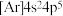 | D. 为 为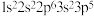 |
A.分子的极性: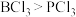 |
B. 比 比 稳定 稳定 |
| C.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能 |
D.在 中的溶解度: 中的溶解度: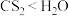 |
 的结构为
的结构为 ,下列叙述不正确的是
,下列叙述不正确的是A. 的结构中,两边的S原子无孤对电子 的结构中,两边的S原子无孤对电子 |
B. 的结构中,中间的两个S原子均有两对孤对电子 的结构中,中间的两个S原子均有两对孤对电子 |
C. 的结构中a、b为键长,则 的结构中a、b为键长,则 |
D.沸点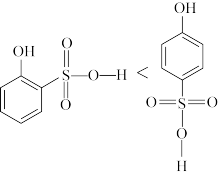 |
Ⅱ.非选择题
结构决定性质,研究元素及物质的结构和性质是化学工作者永恒的课题。
(4)
 原子核外共有
原子核外共有(5)我国科学家屠呦呦以研究“青蒿素”获诺贝尔奖。青蒿素的结构简式如图所示,其组成元素的电负性由大到小的顺序为
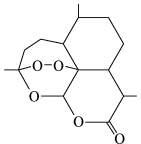
(6)已知,可用异氰酸苯酯与
 氯
氯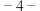 氨基吡啶反应生成氯吡苯脲:
氨基吡啶反应生成氯吡苯脲:
反应过程中,每生成
 氯吡苯脲,断裂
氯吡苯脲,断裂 键,断裂
键,断裂 键。
键。(7)计算:
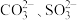 的中心原子上的孤电子对数分别是
的中心原子上的孤电子对数分别是(8)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)用“>”或“<”填写下表。
(2)一种制取NH2OH的反应为2NO2-+4SO2 + 6H2O+ 6NH3 = 4SO +6NH4++2NH2OH。
+6NH4++2NH2OH。
①N、H、O的电负性从小 到大 的顺序为____ 。
②NH3分子的空间构型为____ 。
③NH2OH极易溶于H2O,除因为它们都是极性分子外,还因为____ 。
(3)配合物K[PtCl3(NH3)]中[PtCl3(NH3)]-的结构可用示意图表示为____ (不考虑空间构型)。
(1)用“>”或“<”填写下表。
| 第一电离能 | 熔点 | 沸点(同压) | 键能 |
| P | MgO | CF4 | H-Cl |
(2)一种制取NH2OH的反应为2NO2-+4SO2 + 6H2O+ 6NH3 = 4SO
 +6NH4++2NH2OH。
+6NH4++2NH2OH。①N、H、O的电负性从
②NH3分子的空间构型为
③NH2OH极易溶于H2O,除因为它们都是极性分子外,还因为
(3)配合物K[PtCl3(NH3)]中[PtCl3(NH3)]-的结构可用示意图表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
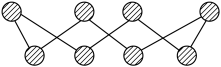
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是___________ ;
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为________________ ;
(3)Se原子序数为___________ ,其核外M层电子的排布式为___________ ;
(4)H2Se的酸性比H2S_____________ (填“强”或“弱”)。气态SeO3分子的立体构型为___________ 。
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是______________ 。
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是

(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为
(3)Se原子序数为
(4)H2Se的酸性比H2S
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是
您最近一年使用:0次
【推荐1】(1)C、N、O、Al、Si、Cu是常见的六种元素。
①Si位于元素周期表第__ 周期第__ 族。
②Cu的基态原子最外层有__ 个电子。
③用“>”或“<”填空:
(2)①N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
则该元素是___ (填写元素符号)。
②Ge的最高价氯化物的分子式是__ 。
③Ge元素可能的性质或应用有__ 。
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其最高价氯化物的沸点低于其溴化物的沸点
①Si位于元素周期表第
②Cu的基态原子最外层有
③用“>”或“<”填空:
| 原子半径 | 电负性 | 熔点 | 沸点 |
| Al | N | 金刚石 | CH4 |
(2)①N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | …… |
| In/(kJ·mol-1) | 578 | 1817 | 2745 | 11578 | …… |
则该元素是
②Ge的最高价氯化物的分子式是
③Ge元素可能的性质或应用有
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其最高价氯化物的沸点低于其溴化物的沸点
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出14种元素的X的数值:
试结合元素周期律知识完成下列问题(放射性元素除外):
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。判断下列物质是离子化合物还是共价化合物?
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
①属于离子化合物的是______________ ; ②属于共价化合物的是______________ .
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系______________________________ ;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系_____________________________________________ 。
(3)请你预测Br与I元素的X数值的大小关系______________________________ 。
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于_____ 原子(元素符号)。
(5)上表中元素形成的AB型化合物中,离子性最强的是_____________________
(6)请你预测周期表中X的数值最小的元素的位置________ 周期,______ 族
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | N |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 | 3.0 |
试结合元素周期律知识完成下列问题(放射性元素除外):
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。判断下列物质是离子化合物还是共价化合物?
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
①属于离子化合物的是
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系
(3)请你预测Br与I元素的X数值的大小关系
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于
(5)上表中元素形成的AB型化合物中,离子性最强的是
(6)请你预测周期表中X的数值最小的元素的位置
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
元素M化合态常见化合价是___________ 价,其基态原子电子排布式为____________ 。
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]S04溶液,该溶液可用于溶解纤维素。
①[Cu (NH3) 4 ] S04中阴离子的立体构型是______________ 。
②除硫元素外,[Cu( NH3) 4 ] S04中所含元素的电负性由小到大的顺序为________________ 。
③NF3与NH3的空间构型相同,中心原子的轨道杂化类型均为___________ 。NF3不易与Cu2 +形成化学键,其原因是________________________ 。
(1)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能(kJ/mol) | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]S04溶液,该溶液可用于溶解纤维素。
①[Cu (NH3) 4 ] S04中阴离子的立体构型是
②除硫元素外,[Cu( NH3) 4 ] S04中所含元素的电负性由小到大的顺序为
③NF3与NH3的空间构型相同,中心原子的轨道杂化类型均为
您最近一年使用:0次



