VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是___________ ;
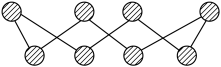
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为________________ ;
(3)Se原子序数为___________ ,其核外M层电子的排布式为___________ ;
(4)H2Se的酸性比H2S_____________ (填“强”或“弱”)。气态SeO3分子的立体构型为___________ 。
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是______________ 。
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是

(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为
(3)Se原子序数为
(4)H2Se的酸性比H2S
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是
更新时间:2019-04-09 09:12:14
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列问题
(1)基态 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有_______ 种。
(2)基态铁原子核外电子运动状态有_______ 种;基态 较基态
较基态 稳定的原因是
稳定的原因是_______ 。
(3)我国自主研发的氟硼铍酸钾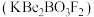 晶体制造的深紫外固体激光器可用于高温超导、催化剂等研究领域。其中
晶体制造的深紫外固体激光器可用于高温超导、催化剂等研究领域。其中 核外电子的运动状态有
核外电子的运动状态有_______ 种。
(1)基态
 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有(2)基态铁原子核外电子运动状态有
 较基态
较基态 稳定的原因是
稳定的原因是(3)我国自主研发的氟硼铍酸钾
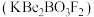 晶体制造的深紫外固体激光器可用于高温超导、催化剂等研究领域。其中
晶体制造的深紫外固体激光器可用于高温超导、催化剂等研究领域。其中 核外电子的运动状态有
核外电子的运动状态有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】单质硅是制造太阳能电池板的主要原料,制备电池板时还需添加硼、氮、钛、钴、钙等多种化学物质。
请回答下列问题:
(1)基态硼原子的电子排布式为___________ ,下列钴原子的价层电子轨道表示式中,不符合洪特规则的是___________ (填选项字母)。
A.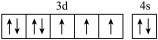 B.
B.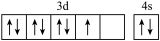
C.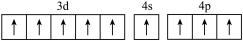 D.
D.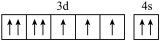
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)钛元素位于元素周期表___________ 区;基态钛原子中,最外层电子的电子云轮廓图为___________ 。
请回答下列问题:
(1)基态硼原子的电子排布式为
A.
 B.
B.
C.
 D.
D.
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为
(3)钛元素位于元素周期表
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】完成下列问题
(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利原理?_______ ;哪些违反了洪特规则?_______ 。
① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤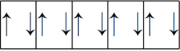 ;⑥
;⑥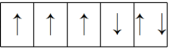
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为_______ ;其最高价氧化物对应水化物的化学式是_______ 。
(3)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列。轨道能量由低到高排列顺序是_______ (填序号)。
①2s ②3d ③4s ④3s ⑤4p ⑥3p
(4)在HX(X为F、Cl、Br、I)分子中,键长最短的是_______ ;
(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利原理?
①
 ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为
(3)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列。轨道能量由低到高排列顺序是
①2s ②3d ③4s ④3s ⑤4p ⑥3p
(4)在HX(X为F、Cl、Br、I)分子中,键长最短的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】CaC2可用于固氮:CaC2+N2 CaCN2+C,CaCN2(氰氨化钙)和水反应可生成NH3。
CaCN2+C,CaCN2(氰氨化钙)和水反应可生成NH3。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:______ 。
(2)C、N、O三种元素的第一电离能由小到大的顺序是______ 。
(3)NH3中N原子的杂化方式为______ ;根据价层电子对互斥理论推测CO 的空间构型为
的空间构型为______ 。
(4)CaCN2中阴离子为CN ,与CN
,与CN 互为等电子体的分子有
互为等电子体的分子有______ (填写一种化学式即可);写出CaCN2水解反应的化学方程式______ 。
 CaCN2+C,CaCN2(氰氨化钙)和水反应可生成NH3。
CaCN2+C,CaCN2(氰氨化钙)和水反应可生成NH3。(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:
(2)C、N、O三种元素的第一电离能由小到大的顺序是
(3)NH3中N原子的杂化方式为
 的空间构型为
的空间构型为(4)CaCN2中阴离子为CN
 ,与CN
,与CN 互为等电子体的分子有
互为等电子体的分子有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮的化合物应用广泛。
(1)Reineckesalt的结构如图所示:
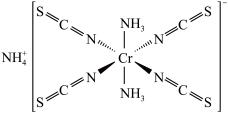
其中配位原子为___________ (填元素符号),阳离子的空间结构为___________ , 中碳原子杂化方式为
中碳原子杂化方式为___________ 。
(2)重铬酸铵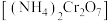 为桔黄色单斜结晶,常用作有机合成催化剂,
为桔黄色单斜结晶,常用作有机合成催化剂, 的结构如图。
的结构如图。
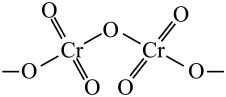
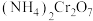 中N、O、Cr三种元素第一电离能由大到小的顺序是
中N、O、Cr三种元素第一电离能由大到小的顺序是___________ (填元素符号)
(3) 是
是 的一种配合物,
的一种配合物, 的结构为
的结构为 。
。 的某种衍生物与甘氨酸形成的离子化合物
的某种衍生物与甘氨酸形成的离子化合物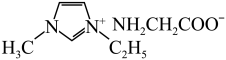 常温下为液态而非固态,原因是
常温下为液态而非固态,原因是___________ 。
(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域 键”(或大
键”(或大 键)。大
键)。大 键可用
键可用 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的原子个数和电子数,如苯分子中大
键的原子个数和电子数,如苯分子中大 键表示为
键表示为 。
。
①下列微粒中存在“离域 键”的是
键”的是___________ 。
A. B.
B.  C.
C.  D.
D.
② 中阴离子
中阴离子 与
与 互为等电子体,均为直线型结构,
互为等电子体,均为直线型结构, 中的2个大
中的2个大 键可表示为
键可表示为___________ 。
(5)符号“ ”没有给出的信息是___________。
”没有给出的信息是___________。
(6)下列实验事实不能用氢键来解释的是___________。
(1)Reineckesalt的结构如图所示:

其中配位原子为
 中碳原子杂化方式为
中碳原子杂化方式为(2)重铬酸铵
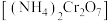 为桔黄色单斜结晶,常用作有机合成催化剂,
为桔黄色单斜结晶,常用作有机合成催化剂, 的结构如图。
的结构如图。
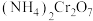 中N、O、Cr三种元素第一电离能由大到小的顺序是
中N、O、Cr三种元素第一电离能由大到小的顺序是(3)
 是
是 的一种配合物,
的一种配合物, 的结构为
的结构为 。
。 的某种衍生物与甘氨酸形成的离子化合物
的某种衍生物与甘氨酸形成的离子化合物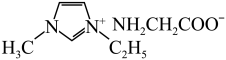 常温下为液态而非固态,原因是
常温下为液态而非固态,原因是(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域
 键”(或大
键”(或大 键)。大
键)。大 键可用
键可用 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的原子个数和电子数,如苯分子中大
键的原子个数和电子数,如苯分子中大 键表示为
键表示为 。
。①下列微粒中存在“离域
 键”的是
键”的是A.
 B.
B.  C.
C.  D.
D.
②
 中阴离子
中阴离子 与
与 互为等电子体,均为直线型结构,
互为等电子体,均为直线型结构, 中的2个大
中的2个大 键可表示为
键可表示为(5)符号“
 ”没有给出的信息是___________。
”没有给出的信息是___________。| A.能层 | B.能级 |
| C.电子云在空间的伸展方向 | D.电子的自旋方向 |
(6)下列实验事实不能用氢键来解释的是___________。
A. 比 比 稳定 稳定 |
| B.乙醇能与水以任意比互溶 |
| C.邻羟基苯甲醛的沸点低于对羟基苯甲醛 |
| D.接近沸点的水蒸气的相对分子质量测量值大于18 |
您最近一年使用:0次
【推荐3】开发新型储氢材料是开发利用氢能的重要研究方向。
(1) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
①基态Cl原子中,电子占据的最高电子层符号为_______ ,该电子层具有的原子轨道数为 _______ 。
②Li、B、H元素的电负性由大到小的排列顺序为___________ 。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+___________ (填“>”“=”或“<”)H-。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如表所示:
则M是 ______________ (填元素符号)。
(1)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。①基态Cl原子中,电子占据的最高电子层符号为
②Li、B、H元素的电负性由大到小的排列顺序为
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如表所示:
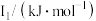 | 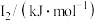 | 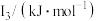 | 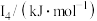 | 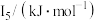 |
| 738 | 1451 | 7733 | 10540 | 13630 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)H、B、N中,原子半径最大的是_________ 。根据对角线规则,B的一些化学性质与元素________ 的相似。
(2)氨硼烷在催化剂作用下水解释放氢气: ,
, 的结构
的结构 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由________ 变为________ 。
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ- ),电负性大小顺序是________ 。
(1)H、B、N中,原子半径最大的是
(2)氨硼烷在催化剂作用下水解释放氢气:
 ,
, 的结构
的结构 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ- ),电负性大小顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩。
(1)基态砷原子的电子排布式为_______ ;砷与溴的第一电离能较大的是_______ 。
(2)AsH3是无色稍有大蒜味气体。AsH3的沸点高于PH3,其主要原因是_______ 。
(3)Na3AsO4可作杀虫剂。AsO 的空间构型为
的空间构型为____ ,与其互为等电子体的一种分子为_____ 。
(4)某砷的氧化物俗称“砒霜”,其分子结构如图所示。该化合物的分子式为_______ ,As原子采取_______ 杂化。
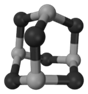
(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与_______ 个Ga相连,As与Ga之间存在的化学键有_______ (填字母)。
A.离子键 B.氢键 C.配位键 D.金属键 E.极性键
(1)基态砷原子的电子排布式为
(2)AsH3是无色稍有大蒜味气体。AsH3的沸点高于PH3,其主要原因是
(3)Na3AsO4可作杀虫剂。AsO
 的空间构型为
的空间构型为(4)某砷的氧化物俗称“砒霜”,其分子结构如图所示。该化合物的分子式为
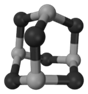
(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与
A.离子键 B.氢键 C.配位键 D.金属键 E.极性键
您最近一年使用:0次

 中碳原子的杂化轨道类型是
中碳原子的杂化轨道类型是

