MnSO4∙H2O是一种易溶于水的微红色斜方晶体,实验室用SO2还原MnO2制备MnSO4.甲同学设计如图所示装置制备硫酸锰。请回答下列有关问题:___________ 。
(2)装置B中的试剂为___________ ,装置E的作用为___________ 。
(3)装置D中发生反应的化学方程式为___________ 。要从D中获得纯净的MnSO4∙H2O,应在观察到___________ 现象时停止通入SO2。
(4)装置D中水浴温度应控制在80°C左右,温度不能过高的原因是___________ 。
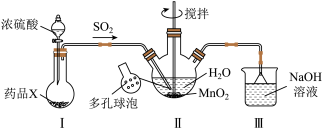
(5)乙同学认为甲同学的设计过于复杂,设计了仅用如图所示装置制备硫酸锰:___________ 。
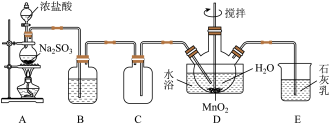
(2)装置B中的试剂为
(3)装置D中发生反应的化学方程式为
(4)装置D中水浴温度应控制在80°C左右,温度不能过高的原因是
(5)乙同学认为甲同学的设计过于复杂,设计了仅用如图所示装置制备硫酸锰:
2023·河北秦皇岛·模拟预测 查看更多[3]
河北省昌黎第一中学2023届高三下学期第五次调研考试化学试题(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)福建省南平市建阳第二中学2023-2024学年高三上学期第二次月考化学试题
更新时间:2023-08-19 19:26:01
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】高锰酸钾俗称灰锰氧、PP粉。它是一种强氧化剂,可以杀灭细菌,为家庭必备的常用消毒药。某实验室按如图装置制备高锰酸钾。
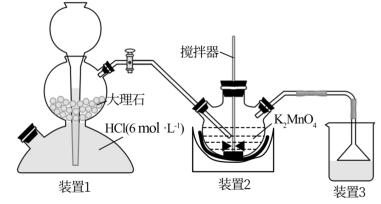
(1)装置1的名称是___________ 。
(2)向装置2中通入足量CO2,生成高锰酸钾的同时也生成了MnO2,用化学方程式表示制备反应的原理___________ 。
(3)反应结束后,将装置2中的物质___________ 、蒸发浓缩、冷却、结晶、烘干,即得到高锰酸钾晶体。蒸发浓缩时温度不宜过高,因为___________ 。
(4)准确称取m g KMnO4产品,配成100 mL溶液,用KMnO4溶液滴定草酸钠溶液,原理为: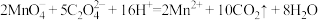 ,已知草酸钠的质量为a g,滴定前滴定管中高锰酸钾溶液的读数为V1 mL,滴定后滴定管中高锰酸钾溶液的读数为V2 mL。判断滴定终点的方法是
,已知草酸钠的质量为a g,滴定前滴定管中高锰酸钾溶液的读数为V1 mL,滴定后滴定管中高锰酸钾溶液的读数为V2 mL。判断滴定终点的方法是___________ ,所得高锰酸钾产品的纯度=___________ 。
(5)实验室所得KMnO4产率较低,请提出优化该装置的措施以提高KMnO4产率___________ 。

(1)装置1的名称是
(2)向装置2中通入足量CO2,生成高锰酸钾的同时也生成了MnO2,用化学方程式表示制备反应的原理
(3)反应结束后,将装置2中的物质
(4)准确称取m g KMnO4产品,配成100 mL溶液,用KMnO4溶液滴定草酸钠溶液,原理为:
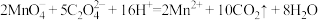 ,已知草酸钠的质量为a g,滴定前滴定管中高锰酸钾溶液的读数为V1 mL,滴定后滴定管中高锰酸钾溶液的读数为V2 mL。判断滴定终点的方法是
,已知草酸钠的质量为a g,滴定前滴定管中高锰酸钾溶液的读数为V1 mL,滴定后滴定管中高锰酸钾溶液的读数为V2 mL。判断滴定终点的方法是(5)实验室所得KMnO4产率较低,请提出优化该装置的措施以提高KMnO4产率
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
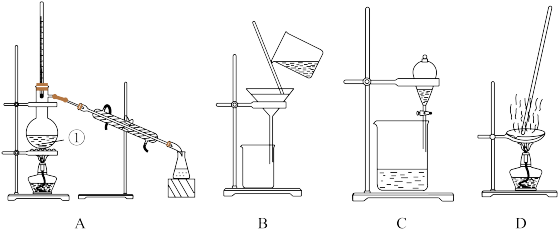
Ⅰ.(1)从碘水中分离出I2,选择装置_______ ,该分离方法的名称为_________ 。
(2)写出上图中仪器①的名称___________________ ;
(3)冷凝管中冷却水的方向为________________________ 。
Ⅱ.实验室要配制2mol/L稀硫酸240mL。
(1)量取18.4mol/L的浓硫酸时,用下面哪种规格的量筒___ (填序号)
①10mL ②50mL ③100mL ④500mL
(2)配制该稀硫酸时使用的仪器除量筒、烧杯外,还必须用到的仪器有玻璃棒、胶头滴管、________ 。
(3)在配制过程中,如果出现下列情况,将对所配溶液的物质的量浓度有何影响?(填“偏高”、“偏低”或“无影响”)
①用量筒量取浓硫酸时,仰视量筒进行读数________ ;
②定容时,液面超过刻度线后用胶头滴管吸至液面处______ ;
Ⅲ.200mL 5mol/L NaOH溶液中,取出20mL溶液,其溶质的质量是___________ ;将取出的溶液稀释至100mL,其溶质的物质的量浓度是_____________ 。

Ⅰ.(1)从碘水中分离出I2,选择装置
(2)写出上图中仪器①的名称
(3)冷凝管中冷却水的方向为
Ⅱ.实验室要配制2mol/L稀硫酸240mL。
(1)量取18.4mol/L的浓硫酸时,用下面哪种规格的量筒
①10mL ②50mL ③100mL ④500mL
(2)配制该稀硫酸时使用的仪器除量筒、烧杯外,还必须用到的仪器有玻璃棒、胶头滴管、
(3)在配制过程中,如果出现下列情况,将对所配溶液的物质的量浓度有何影响?(填“偏高”、“偏低”或“无影响”)
①用量筒量取浓硫酸时,仰视量筒进行读数
②定容时,液面超过刻度线后用胶头滴管吸至液面处
Ⅲ.200mL 5mol/L NaOH溶液中,取出20mL溶液,其溶质的质量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】图示装置制取少量乙酸乙酯,请填空:

(1)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是:___________
(2)写出a中反应的化学方程式,并注明反应类型___________ 、___________
(3)试管b中装有饱和Na2CO3溶液,其作用是___________ 、___________ 、___________
(4)若要把试管b中制得的乙酸乙酯分离出来,应采用的实验操作是___________

(1)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是:
(2)写出a中反应的化学方程式,并注明反应类型
(3)试管b中装有饱和Na2CO3溶液,其作用是
(4)若要把试管b中制得的乙酸乙酯分离出来,应采用的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】四氧化三铁在生产和生活中有着广泛的应用,人们工作中常用的打印机、复印 机使用的墨粉主要成分就是 Fe3O4,下图是某企业用氧化沉淀法生产 Fe3O4的工艺流程:
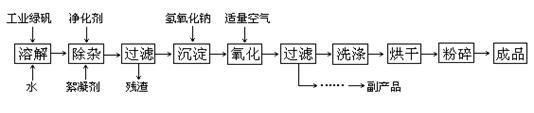
已知:① 工业绿矾中 FeSO4的含量为 52.5%,其中的杂质不参与反应;
②Fe(OH)2+2Fe(OH)3=Fe3O4·4H2O 请回答下列问题:
请回答下列问题
(1)铁的氧化物除Fe3O4·外,还有__________ 。
(2)检验Fe3O4与稀盐酸反应后的溶液中含Fe2+的试剂是___________ ;
(3)在工艺流程中,通入适量空气“氧化”时的化学方程式是:______________ ;
(4)流程图中所示的副产品的化学式是______________ ,从过滤所得滤液中提取该副产品需要的操作依次是_________ (填写序号)。
a.过滤 b.加热浓缩 c.冷却结晶 d.洗涤

已知:① 工业绿矾中 FeSO4的含量为 52.5%,其中的杂质不参与反应;
②Fe(OH)2+2Fe(OH)3=Fe3O4·4H2O 请回答下列问题:
请回答下列问题
(1)铁的氧化物除Fe3O4·外,还有
(2)检验Fe3O4与稀盐酸反应后的溶液中含Fe2+的试剂是
(3)在工艺流程中,通入适量空气“氧化”时的化学方程式是:
(4)流程图中所示的副产品的化学式是
a.过滤 b.加热浓缩 c.冷却结晶 d.洗涤
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得铝。铝土矿的主要成分是Al2O3和SiO2等,从铝土矿中提炼Al2O3的流程如图:
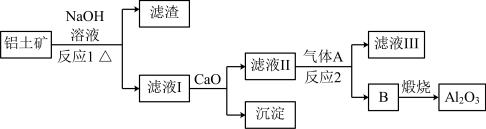
①滤液Ⅰ中加入CaO生成的沉淀是___ (写化学式);反应2的离子方程式为___ 。
②Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为___ 。
(2)工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7)。工艺流程及相关物质溶解度曲线如图所示:
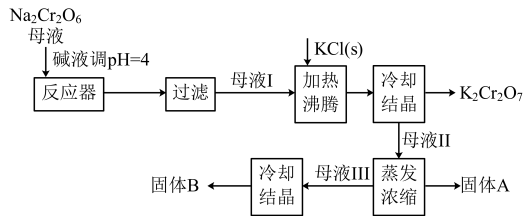
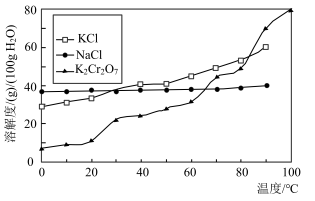
①由Na2Cr2O7生产K2Cr2O7的化学方程式为___ 。冷却到___ (填标号)得到的K2Cr2O7固体产品最多。
a.80℃ b.60℃ c.40℃ d.10℃
②向Na2Cr2O7母液中加碱液调pH的目的是___ 。
③固体A主要为___ (填化学式)。固体B主要为___ (填化学式)。

①滤液Ⅰ中加入CaO生成的沉淀是
②Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为
(2)工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7)。工艺流程及相关物质溶解度曲线如图所示:


①由Na2Cr2O7生产K2Cr2O7的化学方程式为
a.80℃ b.60℃ c.40℃ d.10℃
②向Na2Cr2O7母液中加碱液调pH的目的是
③固体A主要为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】用含钴废料(主要成分为 ,含有少量
,含有少量 杂质)制备
杂质)制备 的流程如图所示。
的流程如图所示。
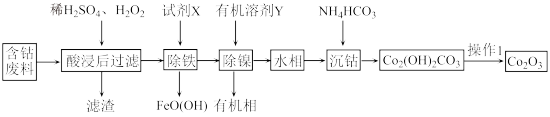
已知: 的氢氧化物沉淀
的氢氧化物沉淀 范围为
范围为 ;在
;在 为
为 时,
时, 水解生成含
水解生成含 胶粒的胶体。(注:
胶粒的胶体。(注: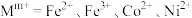 )请回答下列问题:
)请回答下列问题:
(1)“酸浸”步骤中可以有效提高废料利用率的方法有___________ (写出一种方法即可)。“过滤”所得滤渣的主要成分是___________ (填化学式)。
(2)“酸浸”时 与
与 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
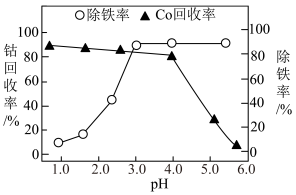
(3)“除铁”中,溶液 对除铁率和钴回收率影响如图乙所示。该步骤应控制
对除铁率和钴回收率影响如图乙所示。该步骤应控制 范围为
范围为___________ ,下图中钴回收率骤降的可能原因是___________ 。
(4)实验室中进行“操作1”用到的硅酸盐仪器有玻璃棒、酒精灯、泥三角、___________ 。
(5)“沉钴”时温度不能太低也不能太高,原因是___________ 。
(6)写出沉钴时的化学反应方程式___________ 。
 ,含有少量
,含有少量 杂质)制备
杂质)制备 的流程如图所示。
的流程如图所示。
已知:
 的氢氧化物沉淀
的氢氧化物沉淀 范围为
范围为 ;在
;在 为
为 时,
时, 水解生成含
水解生成含 胶粒的胶体。(注:
胶粒的胶体。(注: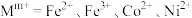 )请回答下列问题:
)请回答下列问题:(1)“酸浸”步骤中可以有效提高废料利用率的方法有
(2)“酸浸”时
 与
与 发生反应的离子方程式为
发生反应的离子方程式为(3)“除铁”中,溶液
 对除铁率和钴回收率影响如图乙所示。该步骤应控制
对除铁率和钴回收率影响如图乙所示。该步骤应控制 范围为
范围为
(4)实验室中进行“操作1”用到的硅酸盐仪器有玻璃棒、酒精灯、泥三角、
(5)“沉钴”时温度不能太低也不能太高,原因是
(6)写出沉钴时的化学反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】过氧化尿素是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素:反应的方程式为:
CO(NH2)2+H2O2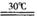 CO(NH)2·H2O2。过氧化尿素的部分性质如下:
CO(NH)2·H2O2。过氧化尿素的部分性质如下:
合成过氧化尿素的流程及反应装置图如下:
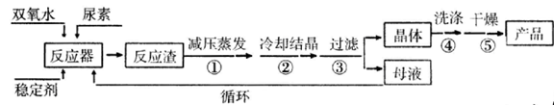
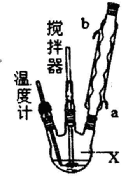
请回答下列问题:
(1)仪器X的名称是____________ ;冷凝管中冷却水从____________ (填“a”或“b”)口进入。
(2)反应器的加热方式是_______________ 。
(3)搅拌器是否可用铁质材料___________ (填“是”或“否”),原因是_______________ 。
(4)步骤① 采用减压蒸发的原因是___________ 。
(5)下列选项中,最适合作为步骤④ 的洗涤液是_______ 。
a.冰水 b.热水 c.饱和NaCl溶液 d.酒精和水的混合液
(6)准确称取0.5000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL 6mol/L H2SO4,用0.1000 mol/L KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应)。
① 滴定终点的现象是______________ 。
② 则产品中CO(NH)2·H2O2的质量分数为______________ 。
③ 若滴定前仰视,滴定后俯视,则测得的过氧化尿素含量_________ (填“偏高”、“偏低”或“不变”)。
CO(NH2)2+H2O2
 CO(NH)2·H2O2。过氧化尿素的部分性质如下:
CO(NH)2·H2O2。过氧化尿素的部分性质如下:
合成过氧化尿素的流程及反应装置图如下:


请回答下列问题:
(1)仪器X的名称是
(2)反应器的加热方式是
(3)搅拌器是否可用铁质材料
(4)步骤① 采用减压蒸发的原因是
(5)下列选项中,最适合作为步骤④ 的洗涤液是
a.冰水 b.热水 c.饱和NaCl溶液 d.酒精和水的混合液
(6)准确称取0.5000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL 6mol/L H2SO4,用0.1000 mol/L KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应)。
① 滴定终点的现象是
② 则产品中CO(NH)2·H2O2的质量分数为
③ 若滴定前仰视,滴定后俯视,则测得的过氧化尿素含量
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如图所示。回答下列问题:
,实验流程如图所示。回答下列问题:
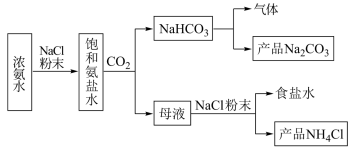
(1)下图装置A中用于盛装稀盐酸的仪器名称是___________ 。
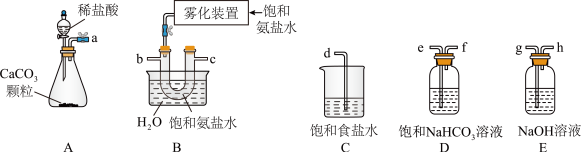
(2)从A~E中选择合适的仪器制备 ,正确的连接顺序是a→e→f→
,正确的连接顺序是a→e→f→___________ →__________ →g(按气流方向填写)。
(3)B中使用雾化装置的原因是______________________________________ 。
(4)生成 总反应的化学方程式为
总反应的化学方程式为______________________ 。
(5)反应完成后,将B中U形管内的混合物处理得到固体 和滤液:
和滤液:
①对固体 充分加热,产生的气体先通过足量浓硫酸,再通过足量
充分加热,产生的气体先通过足量浓硫酸,再通过足量 ,
, 增重0.14g,则固体
增重0.14g,则固体 的质量为
的质量为___________ g。
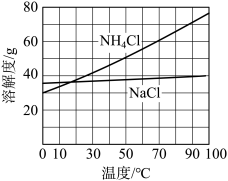
②向滤液中加入NaCl粉末,存在 过程。为使
过程。为使 沉淀充分析出并分离,根据NaCl和
沉淀充分析出并分离,根据NaCl和 溶解度曲线,需采用的操作为
溶解度曲线,需采用的操作为___________ 、___________ 、洗涤、干燥。
 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如图所示。回答下列问题:
,实验流程如图所示。回答下列问题:
(1)下图装置A中用于盛装稀盐酸的仪器名称是

(2)从A~E中选择合适的仪器制备
 ,正确的连接顺序是a→e→f→
,正确的连接顺序是a→e→f→(3)B中使用雾化装置的原因是
(4)生成
 总反应的化学方程式为
总反应的化学方程式为(5)反应完成后,将B中U形管内的混合物处理得到固体
 和滤液:
和滤液:①对固体
 充分加热,产生的气体先通过足量浓硫酸,再通过足量
充分加热,产生的气体先通过足量浓硫酸,再通过足量 ,
, 增重0.14g,则固体
增重0.14g,则固体 的质量为
的质量为②向滤液中加入NaCl粉末,存在
 过程。为使
过程。为使 沉淀充分析出并分离,根据NaCl和
沉淀充分析出并分离,根据NaCl和 溶解度曲线,需采用的操作为
溶解度曲线,需采用的操作为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室常用如图装置来进行铜跟浓硫酸反应等一系列实验。
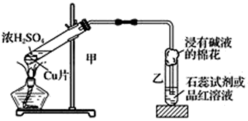
(1)根据什么现象可判断铜跟浓硫酸反应有二氧化硫生成:_______ ;根据什么现象可判断铜跟浓硫酸反应有硫酸铜生成:_______ ;制备硫酸铜时该方法易造成污染,经常采用下面方法代替:将铜屑加入热的稀硫酸,同时向其中滴加双氧水,写出该方法的化学反应方程式_______ 写出甲装置中发生的主要反应的化学方程式:_______ 。
(2)你在实验室中进行这个实验时,除了(1)小题中指到的实验现象外,还可以观察到许多其他的实验现象,请写出两种:_______ 。
(3)装置乙的试管口部放有一团浸有碱液的棉花,棉花中通常是浸有饱和碳酸钠溶液,写出棉花中发生反应的化学方程式:_______ 。
(4)测定空气中SO2含量时,常采用酸性高锰酸钾溶液溶液吸收后进行测定。写出用酸性高锰酸钾溶液吸收SO2反应的离子方程式_______ 。

(1)根据什么现象可判断铜跟浓硫酸反应有二氧化硫生成:
(2)你在实验室中进行这个实验时,除了(1)小题中指到的实验现象外,还可以观察到许多其他的实验现象,请写出两种:
(3)装置乙的试管口部放有一团浸有碱液的棉花,棉花中通常是浸有饱和碳酸钠溶液,写出棉花中发生反应的化学方程式:
(4)测定空气中SO2含量时,常采用酸性高锰酸钾溶液溶液吸收后进行测定。写出用酸性高锰酸钾溶液吸收SO2反应的离子方程式
您最近一年使用:0次



