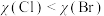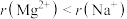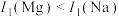某化合物结构如图所示。其中M、X、Y、Z为原子序数依次增大的短周期非金属元素,X是有机分子的骨架元素,W基态原子的M层为全充满、N层只有一个电子。下列说法正确的是
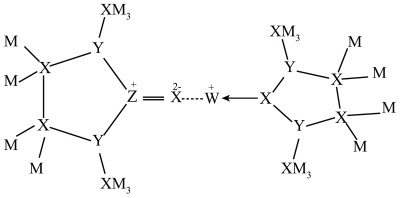

| A.原子半径: X>Y>Z | B.第一电离能: X>Y>M>W |
| C.该配合物中X均满足8电子稳定结构 | D.最简单的氢化物的沸点:Y>Z |
更新时间:2023-08-21 20:55:08
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】如表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、−2 | −1 | −1 |
| A.A、B的简单离子的半径:B>A |
| B.D、E形成的简单离子的还原性:E>D |
| C.气态氢化物的稳定性:D<C |
| D.最高价氧化物对应的水化物的酸性:C>E |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列关于氯、溴两种元素及其组成的物质的比较中,不正确的是
| A.稳定性:HCl<HBr | B.非金属性:Cl>Br |
| C.酸性:HClO4>HBrO4 | D.氧化性:Cl2>Br2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】短周期元素 W、X、Y、Z 在元素周期表中的相对位置如图所示,若 Y 元素原子的最外层电子数是内层电子数的 3 倍,则下列说法正确的是
| X | Y | ||||
| W | Z |
| A.原子半径大小:Z>W>Y |
| B.W 可与 X 和 Y 形成的一种化合物发生反应 |
| C.Y 分别与 X、W 形成的化合物中化学键类型完全相同 |
| D.工业上电解熔融的 W 与 Y 所形成的化合物来制取 W 的单质 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物,一种 配合物的结构如图所示,下列说法正确的是
配合物的结构如图所示,下列说法正确的是

 配合物的结构如图所示,下列说法正确的是
配合物的结构如图所示,下列说法正确的是
| A.该螯合物内存在氢键 |
| B.1mol该螯合物通过螯合作用形成的配位键有3mol |
| C.该螯合物中N的杂化方式只有1种 |
D.原子半径,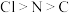 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】以下有关元素性质的说法中正确的是
| A.以下原子中,①1s22s22p63s23p2,②1s22s22p3,③1s22s22p2,④1s22s22p63s23p4,原子半径最大的是④ |
| B.下列原子中,①1s2,②1s22s22p6,③1s22s22p63s23p6对应的第一电离能最大的元素是③ |
| C.某短周期元素的逐级电离能(kJ/mol)分别为578、1817、2745、11575、14830、18376、23293,该元素可能位于第三周期IIA族 |
| D.①Na、K、Rb,②C、S、P,③Na、P、O元素的电负性依次递增的是③ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】M、R均为主族元素,已知M的一个原子失去2个电子,R的一个原子得到1个电子后形成稀有气体元素的电子层结构。下列关于M与R形成的化合物的叙述正确的是( )
| A.M与R可以形成MR2型离子化合物 |
| B.在MR2中M的离子半径比R的离子半径大 |
| C.形成的两种离子分别是M+和R2- |
D.MR2的电子式为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】短周期元素X、Y、Z、W在元素周期表中的位置如图所示,X原子最外层电子数为6,下列说法正确的是
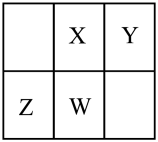

| A.X的最高化合价为+6 |
| B.Y的氢化物稳定性弱于X |
| C.X的非金属性强于W的非金属性 |
| D.Z的最高价氧化物对应的水化物酸性强于W |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其电子层数的2倍,Y的焰色反应为黄色,Z原子的最外层有6个电子。下列叙述正确的是
| A.原子半径:r(Y)<r(Z)<r(W) |
| B.XW4属于离子化合物 |
| C.工业上常用电解熔融YW的方法制备元素Y的单质 |
| D.元素X的最高价氧化物对应水化物的酸性比W的强 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】中国科学家对量子材料的研究处于国际领先水平,近年来对石墨烯、硅烯、锗烯等低维量子材料的研究发展迅速。下列说法不正确 的是
| A.碳、硅、锗属于同主族元素 |
B.第一电离能: |
| C.红外光谱法可直接确定石墨烯的晶体结构 |
| D.硅和锗常用作半导体材料 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列关于元素周期表、原子结构或元素性质的说法中错误的是
| A.共价化合物中,电负性大的成键元素表现为负价 |
| B.电负性越大,元素的非金属性越强,第一电离能也越大 |
| C.目前的元素周期表共有7个周期,7个主族,8个副族,1个0族 |
| D.主族元素的价电子即最外层电子,过渡元素的价电子还包括次外层甚至倒数第三层电子 |
您最近一年使用:0次