下列说法正确的是
| A.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 |
| B.向盛有NaCl溶液的试管中滴入AgNO3,再加入氨水,先产生白色沉淀,后沉淀溶解 |
| C.凡是AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键 |
D.根据“相似相溶规则”, 在水中的溶解度小于其在 在水中的溶解度小于其在 中的溶解度 中的溶解度 |
更新时间:2023-08-26 09:56:27
|
相似题推荐
【推荐1】已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是原子半径最小的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布式为 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是| A.A、B、C三种元素的电负性:C<B<A |
| B.B、C、D、E四种元素的第一电离能:B>C>E>D |
| C.B元素单质分子中π键和σ键的个数比为1:2 |
| D.F元素位于元素周期表d区 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.所有非金属元素都分布在p区 |
| B.电负性越大,元素的非金属性越强,第一电离能也越大 |
| C.元素周期表中从第ⅢB族到第ⅡB族的10个纵列的元素都是金属元素 |
| D.第四周期的金属元素从左到右,元素的金属性依次减弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一种矿石的化学组成为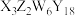 。
。 、
、 、
、 、
、 为原于序数依次增加的短周期元素,且价层电子数之和为15,
为原于序数依次增加的短周期元素,且价层电子数之和为15, 、
、 、
、 处于相邻的主族,
处于相邻的主族, 和
和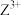 的电荷与半径之比相近,导致两元素性质相似。下列说法正确的是
的电荷与半径之比相近,导致两元素性质相似。下列说法正确的是
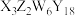 。
。 、
、 、
、 、
、 为原于序数依次增加的短周期元素,且价层电子数之和为15,
为原于序数依次增加的短周期元素,且价层电子数之和为15, 、
、 、
、 处于相邻的主族,
处于相邻的主族, 和
和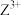 的电荷与半径之比相近,导致两元素性质相似。下列说法正确的是
的电荷与半径之比相近,导致两元素性质相似。下列说法正确的是A.与 同周期的元素中,第一电离能比 同周期的元素中,第一电离能比 大的元素有5种 大的元素有5种 |
B.原子半径大小: |
C. 、 、 的简单氢化物中,中心原子都采取 的简单氢化物中,中心原子都采取 杂化 杂化 |
D. 的单质可以和盐酸反应,不能与氢氧化钠溶液反应 的单质可以和盐酸反应,不能与氢氧化钠溶液反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】法匹拉韦是治疗新冠肺炎的一种药物,其结构简式如图所示。下列说法正确的是

| A.该分子中C-N键的键长大于C-F键的键长 | B.该有机物属于芳香族化合物 |
C.该分子中C原子的杂化方式有 、 、 | D.该分子中存在手性碳原子 |
您最近一年使用:0次
【推荐1】化合物Q的结构如图所示。X、Y、Z、W为原子序数依次增大的短周期主族元素,下列说法正确的是


A.简单离子半径: | B. 化合物Q中存在 化合物Q中存在 配位键 配位键 |
| C.Y的最高价氧化物对应的水化物是三元酸 | D.同周期元素中第一电离能比Z大的元素有2种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】配离子[Cu(NH3)4(H2O)2]2+的结构如图所示。下列说法正确的是


| A.该配离子中Cu2+的配位数是4 |
| B.基态Cu原子的价电子排布式是3d94s2 |
| C.加热时,该离子首先失去的组分是H2O |
| D.该配离子中存在的化学键有:离子键、共价键、配位键和氢键 |
您最近一年使用:0次
【推荐1】生活中的化学无处不在,下列关于生活中的化学描述错误的是
| A.可以用光谱分析的方法来确定太阳的组成元素是否含氦 |
| B.壁虎在天花板上爬行自如是因为壁虎的脚与墙体之间有范德华力 |
| C.碘易溶于四氯化碳,难溶于水,因为碘、四氯化碳都是非极性分子 |
| D.“挑尽寒灯梦不成”所看到的灯光和原子核外电子跃迁无关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验操作、现象和结论都正确且有相关性的是
| 选项 | 操作及现象 | 结论 |
| A | 向含酚酞的NaOH溶液中通入 ,溶液褪色 ,溶液褪色 |  具有漂白性 具有漂白性 |
| B | 收集一试管干燥的 并倒置于盛水的水槽中,液体充满试管 并倒置于盛水的水槽中,液体充满试管 |  和 和 反应,气体体积减小 反应,气体体积减小 |
| C | 在苯酚溶液中加入足量浓溴水,产生白色沉淀 | 苯酚和溴发生化学反应 |
| D | 在碘水中加入氯仿( ,振荡、静置,上层为浅色的水相 ,振荡、静置,上层为浅色的水相 | 氯仿极性强于水且密度大于水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 ;②
;②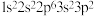 ;③
;③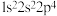 ;④
;④ 。下列有关比较中正确的是
。下列有关比较中正确的是 )可与HCl反应生成氯乙烷(
)可与HCl反应生成氯乙烷( )。下列说法错误的是
)。下列说法错误的是 键为s-s
键为s-s  键
键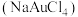 溶液与泪液中的葡萄糖发生反应生成纳米金单质颗粒(直径为
溶液与泪液中的葡萄糖发生反应生成纳米金单质颗粒(直径为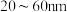 ),下列说法
),下列说法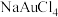 中含有离子键和配位键
中含有离子键和配位键

