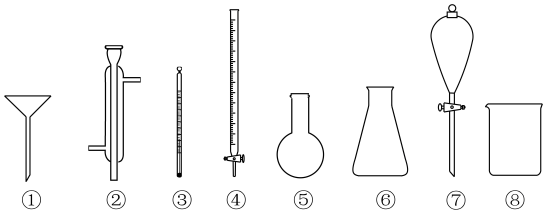
实验室模拟工业提碘,路线如下:
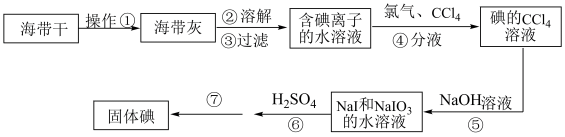
| A.操作①为研磨,主要仪器为研钵 |
| B.可使用淀粉溶液检验步骤③过滤后的水溶液中是否含有 I- |
| C.操作④~⑥的目的是为了富集碘 |
D.步骤⑥反应离子方程式为I-+IO +6H+=I2+3H2O +6H+=I2+3H2O |
更新时间:2023/09/01 15:29:42
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】能用离子方程式H++ OH-→ H2O 表示的反应是
| A.氨水和盐酸 | B.氢氧化钠溶液和醋酸 |
| C.硫酸和氢氧化钡溶液 | D.硝酸和澄清石灰水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的个数是
①常温下,氯水和液氯都可以用钢瓶储存
② 和
和 均可用于制作膨松剂
均可用于制作膨松剂
③用湿润的蓝色石蕊试纸可检验 中是否混有
中是否混有
④将 和
和 分别放入
分别放入 溶液中,均会有蓝色沉淀生成并有无色气体放出
溶液中,均会有蓝色沉淀生成并有无色气体放出
⑤ 胶体和
胶体和 溶液都是混合物
溶液都是混合物
⑥ 和
和 均属于可溶性盐,可用澄清石灰水鉴别
均属于可溶性盐,可用澄清石灰水鉴别
⑦蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
⑧因为胶粒比溶液中溶质粒子大,所以胶体可以用过滤的方法把胶粒分离出来
①常温下,氯水和液氯都可以用钢瓶储存
②
 和
和 均可用于制作膨松剂
均可用于制作膨松剂③用湿润的蓝色石蕊试纸可检验
 中是否混有
中是否混有
④将
 和
和 分别放入
分别放入 溶液中,均会有蓝色沉淀生成并有无色气体放出
溶液中,均会有蓝色沉淀生成并有无色气体放出⑤
 胶体和
胶体和 溶液都是混合物
溶液都是混合物⑥
 和
和 均属于可溶性盐,可用澄清石灰水鉴别
均属于可溶性盐,可用澄清石灰水鉴别⑦蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
⑧因为胶粒比溶液中溶质粒子大,所以胶体可以用过滤的方法把胶粒分离出来
| A.3个 | B.4个 | C.5个 | D.6个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学利用下列装置探究Na与CO2反应的还原产物,已知PdCl2+CO+H2O=Pd(黑色)↓+CO2+2HCl。下列相关分析错误的是
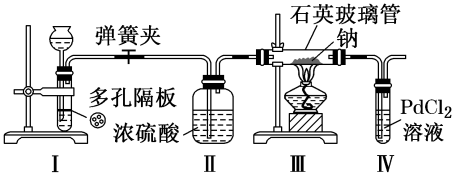

| A.步骤IV的目的是证明还原产物是否有CO |
| B.II中浓硫酸的目的是干燥CO2 |
| C.实验时,III中石英玻璃管容易受到腐蚀 |
| D.I中发生反应可以是Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某兴趣小组在实验室中利用菱镁矿设计制备氧化镁的流程如下。已知菱镁矿主要成分为 ,含有少量
,含有少量 和难溶性杂质。下列说法错误的是
和难溶性杂质。下列说法错误的是

 ,含有少量
,含有少量 和难溶性杂质。下列说法错误的是
和难溶性杂质。下列说法错误的是
| A.步骤(1)前需将菱镁矿粉碎,以提高原料利用率 |
| B.步骤(1)和步骤(2)中要用到的玻璃仪器有漏斗、玻璃棒、烧杯 |
C.步骤(2)中获得 沉淀,说明 沉淀,说明 不与NaOH溶液反应。 不与NaOH溶液反应。 |
| D.步骤(3)中需使用到坩埚等仪器 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验所采取的分离方法与对应原理都正确的是
选项 | 目的 | 分离方法 | 原理 |
A | 由海水(含 )获得蒸馏水 )获得蒸馏水 | 蒸馏 | 加热时 难挥发 难挥发 |
B | 分离汽油和水 | 萃取 | 汽油和水的密度不同 |
C | 除去 固体中混杂的 固体中混杂的 | 蒸发结晶 |  在水中的溶解度随温度变化不大 在水中的溶解度随温度变化不大 |
D | 分离溶于水的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列操作中不正确的是
| A.除去NaCl固体中的少量KNO3,应将固体溶解后蒸发结晶,趁热过滤,洗涤干燥 |
| B.蒸馏操作时,应使温度计水银球放在蒸馏头支管口略下方处 |
| C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
| D.分液操作时,分液漏斗下端紧靠烧杯内壁 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
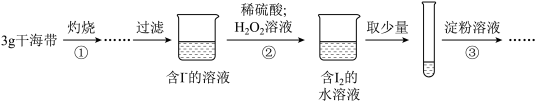
【推荐1】某学习小组按如下实验过程证明了海带中存在的碘元素:
下列说法不正确的是

下列说法不正确的是
| A.步骤①需要将干海带放入坩埚中灼烧 |
| B.步骤②反应的离子方程式为:2I- +2H++H2O2=I2+2H2O |
| C.步骤③操作后,观察到试管中溶液变为蓝色,可以说明海带中含有碘元素 |
| D.若步骤②仅滴加稀硫酸后放置一会儿,步骤③操作后,试管中溶液不变成蓝色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知苯的密度为0.81g/cm3; 。从海带中提取碘的实验过程如下:
。从海带中提取碘的实验过程如下:
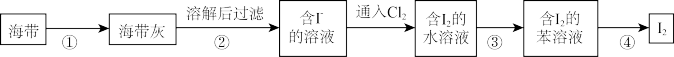
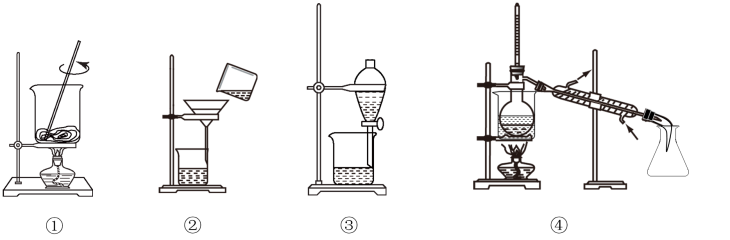
以上过程中,涉及到下列操作的示意图,其中正确的是
 。从海带中提取碘的实验过程如下:
。从海带中提取碘的实验过程如下: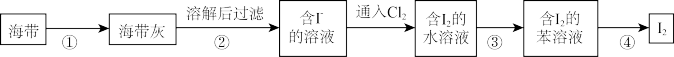
以上过程中,涉及到下列操作的示意图,其中正确的是

| A.①将海带灼烧成灰 | B.②过滤得含 的溶液 的溶液 |
| C.③碘的苯溶液从下层放出 | D.④分离碘并回收苯 |
您最近一年使用:0次

 的
的 和
和 溶液的性质。
溶液的性质。 固体滴入少量
固体滴入少量
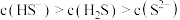
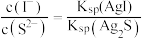

 ,含
,含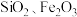 等杂质)冶炼铝的主要流程如下:
等杂质)冶炼铝的主要流程如下: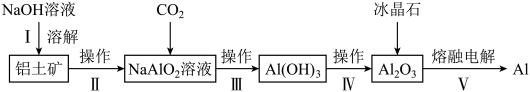
 碱溶时转变为铝硅酸钠沉淀)
碱溶时转变为铝硅酸钠沉淀) 溶液用量可提高
溶液用量可提高 的离子方程式为
的离子方程式为