已知下列热化学方程式:
①

②

③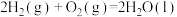

则反应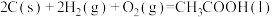 的焓变为
的焓变为
①


②


③
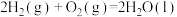

则反应
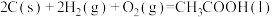 的焓变为
的焓变为| A.−488.3kJ/mol | B.−244.15kJ/mol | C.488.3kJ/mol | D.244.15kJ/mol |
更新时间:2023-09-04 07:17:11
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】某反应过程中体系的能量变化如图所示,下列说法错误的是


A.反应过程可表示为     |
| B.E1为反应物的能量与过渡态的能量差,称为正反应的活化能 |
| C.正反应的热效应为ΔH=E1−E2,且E2>E1,所以正反应为放热反应 |
| D.此图中逆反应的热效应为ΔH=E1−E2,逆反应为吸热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】 氨是一种重要的化工原料,广泛用于硝酸、纯碱、制药、化肥等工业。合成氨反应为 ,
, 在催化剂作用下发生一系列转化的示意图如下:
在催化剂作用下发生一系列转化的示意图如下:
 ,
, 在催化剂作用下发生一系列转化的示意图如下:
在催化剂作用下发生一系列转化的示意图如下: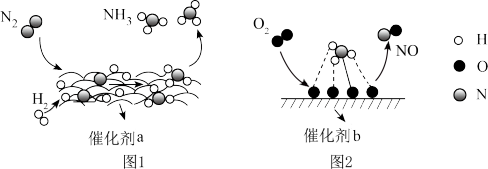
A.催化剂b表面发生的反应利用了 的氧化性 的氧化性 |
| B.催化剂a、b表面发生的反应过程中均发生了非极性共价键的断裂 |
C.合成氨反应的热效应为 (E表示键能) (E表示键能) |
D.22.4L 在催化剂a表面充分反应,转移电子数一定为 在催化剂a表面充分反应,转移电子数一定为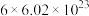 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】火电厂利用燃煤发电,煤燃烧中的热化学方程式有:
C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
CO(g)+ O2(g)=CO2(g) ΔH2=-283 kJ/mol
O2(g)=CO2(g) ΔH2=-283 kJ/mol
C(s)+ O2(g)=CO(g) ΔH3=?
O2(g)=CO(g) ΔH3=?
下列有关说法中不正确的是
C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
CO(g)+
 O2(g)=CO2(g) ΔH2=-283 kJ/mol
O2(g)=CO2(g) ΔH2=-283 kJ/molC(s)+
 O2(g)=CO(g) ΔH3=?
O2(g)=CO(g) ΔH3=?下列有关说法中不正确的是
| A.CO的燃烧热为283 kJ/mol |
| B.二氧化碳分解为一氧化碳和氧气的反应是吸热反应 |
| C.ΔH3=ΔH2-ΔH1=110.5 kJ/mol |
| D.ΔH3=ΔH1-ΔH2=-110.5 kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知:CO2(g)+C(s)=2CO(g) ΔH1
C(s)+H2O(g)=CO(g)+H2(g) ΔH2
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3
CuO(s)+CO(g)=Cu(s)+CO2(g) ΔH4
2CuO(s)+C(s)=2Cu(s)+CO2(g) ΔH5
下列关于上述反应焓变的判断中不正确的是
C(s)+H2O(g)=CO(g)+H2(g) ΔH2
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3
CuO(s)+CO(g)=Cu(s)+CO2(g) ΔH4
2CuO(s)+C(s)=2Cu(s)+CO2(g) ΔH5
下列关于上述反应焓变的判断中不正确的是
| A.ΔH1>0 | B.ΔH2=ΔH1+ΔH3 | C.ΔH2<ΔH3 | D.ΔH5=2ΔH4+ΔH1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】工业上用CO生产甲醇的反应为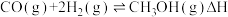 。图1表示反应中能量的变化;图2表示一定温度下,在体积固定为2L的密闭容器中加入4molH2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化;图3表示不同压强P1、P2下平衡时甲醇百分含量随温度变化的情况。下列叙述不正确的
。图1表示反应中能量的变化;图2表示一定温度下,在体积固定为2L的密闭容器中加入4molH2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化;图3表示不同压强P1、P2下平衡时甲醇百分含量随温度变化的情况。下列叙述不正确的

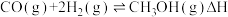 。图1表示反应中能量的变化;图2表示一定温度下,在体积固定为2L的密闭容器中加入4molH2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化;图3表示不同压强P1、P2下平衡时甲醇百分含量随温度变化的情况。下列叙述不正确的
。图1表示反应中能量的变化;图2表示一定温度下,在体积固定为2L的密闭容器中加入4molH2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化;图3表示不同压强P1、P2下平衡时甲醇百分含量随温度变化的情况。下列叙述不正确的
| A.此反应在低温时自发进行,图1中曲线b表示使用催化剂的能量变化 |
B.若CO、H2、CH3OH(g)的燃烧热△H分别为akJ·mol-1、bkJ·mol-1、ckJ·mol-1,则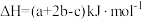 |
C.由图2知,其他条件不变,再充入1molCO和2molH2,反应达到新平衡时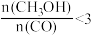 |
| D.P1<P2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是
A.H2O(g)=H2(g)+ O2(g) △H=+484kJ/mol O2(g) △H=+484kJ/mol |
| B.2H2(g)+O2(g)=2H2O(l) △H=-484kJ/mol |
C.H2(g)+ O2(g)=H2O(l) △H=+242kJ/mol O2(g)=H2O(l) △H=+242kJ/mol |
D.H2O(g)=H2(g)+ O2(g) △H=+242kJ/mol O2(g) △H=+242kJ/mol |
您最近一年使用:0次
【推荐2】下列关于热化学反应的描述中正确的是
| A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g) △H=+283.0kJ/mol |
| C.需要加热才能发生的反应不一定是吸热反应 |
| D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列说法正确的是
| A.已知25℃、101kPa条件下:4Al(s)+3O2(g)=2Al2O3(s) ΔH=-2834.9kJ/mol,4Al(s)+2O3(g)=2Al2O3(s) ΔH=-3119.1kJ/mol,则O3比O2稳定 |
| B.C2H5OH(l)的燃烧热是1366.8kJ/mol,则反应C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)的ΔH=-1366.8kJ/mol |
| C.已知中和热为57.3kJ/mol,则反应H2SO4(aq)+Ba(OH)2(aq)=2H2O(l)+BaSO4(s)的ΔH=-114.6kJ/mol |
| D.在一定温度和压强下,将0.5mol N2和1.5molH2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,则其热化学方程式为N2(g)+3H2(g)⇌2NH3(g) ΔH=-38.6kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是
| A.任何酸与碱发生中和反应生成1molH2O的过程中,能量变化均相同 |
| B.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
| C.已知:①2H2(g)+O2(g)=2H2O(g) ΔH1=-amol/L②2H2(g)+O2(g)=2H2O(1) ΔH2=-bmol/L则a>b |
| D.已知:①C(s石墨)+O2(g)=CO2(g) ΔH1=-393.5mol/L②C(s,金刚石)+O2(g)=CO2(g) ΔH2=-395.0mol/L,则金刚石比石墨稳定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知热化学方程式:SO2(g)+1/2O2(g) SO3(g) ΔH=-98.32 kJ·mol-1,在一定温度的密闭容器中充入2 mol SO2和1molO2充分反应,经过一段时间放出的热量为98.32 kJ,则容器中的压强与起始时压强的比值为( )
SO3(g) ΔH=-98.32 kJ·mol-1,在一定温度的密闭容器中充入2 mol SO2和1molO2充分反应,经过一段时间放出的热量为98.32 kJ,则容器中的压强与起始时压强的比值为( )
 SO3(g) ΔH=-98.32 kJ·mol-1,在一定温度的密闭容器中充入2 mol SO2和1molO2充分反应,经过一段时间放出的热量为98.32 kJ,则容器中的压强与起始时压强的比值为( )
SO3(g) ΔH=-98.32 kJ·mol-1,在一定温度的密闭容器中充入2 mol SO2和1molO2充分反应,经过一段时间放出的热量为98.32 kJ,则容器中的压强与起始时压强的比值为( )| A.3/2 | B.2/3 | C.6/5 | D.5/6 |
您最近一年使用:0次

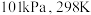 下,有关水分子断键过程的能量变化:下列说法正确的是
下,有关水分子断键过程的能量变化:下列说法正确的是
 ,且
,且
 是
是 的键能
的键能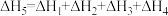
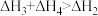
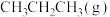 (用RH表示)的氯代和溴代反应能量图及产率关系如图(图中物质均为气态)。下列说法正确的是
(用RH表示)的氯代和溴代反应能量图及产率关系如图(图中物质均为气态)。下列说法正确的是

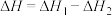
 分子中有一个手性碳原子
分子中有一个手性碳原子

