含氮化合物对环境、生产和人类活动有很大影响。
(1)NH 具有还原性。饱和NaNO2(aq)与饱和NH4Cl(aq)混合加热,会产生无色无味气体,写出该过程的化学方程式:
具有还原性。饱和NaNO2(aq)与饱和NH4Cl(aq)混合加热,会产生无色无味气体,写出该过程的化学方程式:___________ ,请设计一个实验方案检验某固体中的阳离子为NH :
:___________ 。
(2)NF3为无色、无味的气体,在潮湿的环境中易变质生成HF、NO、HNO3,写出反应的化学方程式:___________ ;该反应中氧化剂与还原剂的物质的量之比为___________ 。
(3)有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H2SO4)=2.0mol·L-1,c(HNO3)=1.0mol·L-1.取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为___________ L。
(4)某课题组用间接电解法除NO,其原理如图所示:
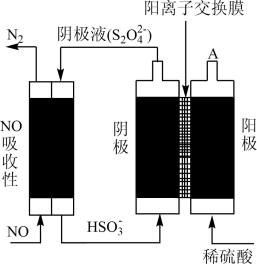
①电解过程中透过阳离子交换膜的离子是___________ 。
②写出电解池阴极的电极反应式:___________ 。
(1)NH
 具有还原性。饱和NaNO2(aq)与饱和NH4Cl(aq)混合加热,会产生无色无味气体,写出该过程的化学方程式:
具有还原性。饱和NaNO2(aq)与饱和NH4Cl(aq)混合加热,会产生无色无味气体,写出该过程的化学方程式: :
:(2)NF3为无色、无味的气体,在潮湿的环境中易变质生成HF、NO、HNO3,写出反应的化学方程式:
(3)有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H2SO4)=2.0mol·L-1,c(HNO3)=1.0mol·L-1.取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为
(4)某课题组用间接电解法除NO,其原理如图所示:

①电解过程中透过阳离子交换膜的离子是
②写出电解池阴极的电极反应式:
更新时间:2023/10/07 08:21:42
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.按要求填空:(用化学方程式表示)
(1)工业合成氨___________
(2)氨的催化氧化反应___________
(3)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为:___________
(4)氢氟酸不能使用玻璃瓶盛装的原因:___________
II.请自选试剂完成不同价态含硫物质的转化方程式(化学或离子均可)
(5)S(-2)→S(0)___________
(6)S(+6)→S(+4)___________
(1)工业合成氨
(2)氨的催化氧化反应
(3)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为:
(4)氢氟酸不能使用玻璃瓶盛装的原因:
II.请自选试剂完成不同价态含硫物质的转化方程式(化学或离子均可)
(5)S(-2)→S(0)
(6)S(+6)→S(+4)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学工业为医药行业提供了强有力的物质支撑。请按要求回答下列问题:
(1)研究表明病毒可通过气溶胶传播,气溶胶中粒子的直径大小为___________ ,可以用___________ 来鉴别气溶胶。
(2)常温下, 、乙醇、
、乙醇、 、NaClO溶液都为常用的消毒剂,其中能导电的是
、NaClO溶液都为常用的消毒剂,其中能导电的是___________ ,属于电解质的是___________ 。
(3)熔喷布是一次性医用口罩的关键材料,由熔融态聚丙烯电喷形成的超细纤维经驻极静电处理制成。由丙烯制得聚丙烯的化学方程式是___________ 。
(4)家用制氧机“氧立得”使用的是过碳酸钠( ),该药品被称为固体双氧水,兼具碳酸钠和双氧水的双重性质,可以利用过氧化氢在二氧化锰的催化下分解产生氧气。
),该药品被称为固体双氧水,兼具碳酸钠和双氧水的双重性质,可以利用过氧化氢在二氧化锰的催化下分解产生氧气。
①写出过碳酸钠在二氧化锰催化下产生氧气的化学方程式:___________ 。
②下列物质不会使过碳酸钠失效的是___________ (填标号)。
A.HCl B. C.
C. D.
D.
(5)消毒能力一般用单位质量的消毒剂所得电子的数量来衡量, 、NaClO等含氯消毒剂进行反应时最终都转化为
、NaClO等含氯消毒剂进行反应时最终都转化为 ,则
,则 与NaClO的消毒能力之比为
与NaClO的消毒能力之比为___________ (写出最简整数比)。
(6)医药行业中测温枪发挥了极大的作用。在测温枪电池制备过程中会生成 (Ti为+4价),1mol
(Ti为+4价),1mol 中过氧键的数目为
中过氧键的数目为___________ 。
(1)研究表明病毒可通过气溶胶传播,气溶胶中粒子的直径大小为
(2)常温下,
 、乙醇、
、乙醇、 、NaClO溶液都为常用的消毒剂,其中能导电的是
、NaClO溶液都为常用的消毒剂,其中能导电的是(3)熔喷布是一次性医用口罩的关键材料,由熔融态聚丙烯电喷形成的超细纤维经驻极静电处理制成。由丙烯制得聚丙烯的化学方程式是
(4)家用制氧机“氧立得”使用的是过碳酸钠(
 ),该药品被称为固体双氧水,兼具碳酸钠和双氧水的双重性质,可以利用过氧化氢在二氧化锰的催化下分解产生氧气。
),该药品被称为固体双氧水,兼具碳酸钠和双氧水的双重性质,可以利用过氧化氢在二氧化锰的催化下分解产生氧气。①写出过碳酸钠在二氧化锰催化下产生氧气的化学方程式:
②下列物质不会使过碳酸钠失效的是
A.HCl B.
 C.
C. D.
D.
(5)消毒能力一般用单位质量的消毒剂所得电子的数量来衡量,
 、NaClO等含氯消毒剂进行反应时最终都转化为
、NaClO等含氯消毒剂进行反应时最终都转化为 ,则
,则 与NaClO的消毒能力之比为
与NaClO的消毒能力之比为(6)医药行业中测温枪发挥了极大的作用。在测温枪电池制备过程中会生成
 (Ti为+4价),1mol
(Ti为+4价),1mol 中过氧键的数目为
中过氧键的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮及其化合物在生产、生活中有重要的应用。回答下列问题:
(1)下列选项可作为比较氮和氧非金属性强弱的判断依据的是_______
a.氢化物稳定性:H2O>NH3 b.沸点:H2O>NH3
c.NO中N为+2价,O为-2价 d.碱性:NH3>H2O
(2)氢氰酸(HCN)可用于制造丙烯腈和丙烯酸树脂,HCN分子的电子式为_______ 。
(3)NaNO2是一种白色易溶于水的固体,俗称工业盐。其水溶液显碱性,则该溶液中离子浓度由大到小的顺序是_______ 。
(4)氰化钠是一种剧毒物质,处理该物质的方法之一是在碱性条件下通入氯气,其中CN-被氧化成CO 和N2,写出该反应的离子方式
和N2,写出该反应的离子方式_______ 。
(1)下列选项可作为比较氮和氧非金属性强弱的判断依据的是
a.氢化物稳定性:H2O>NH3 b.沸点:H2O>NH3
c.NO中N为+2价,O为-2价 d.碱性:NH3>H2O
(2)氢氰酸(HCN)可用于制造丙烯腈和丙烯酸树脂,HCN分子的电子式为
(3)NaNO2是一种白色易溶于水的固体,俗称工业盐。其水溶液显碱性,则该溶液中离子浓度由大到小的顺序是
(4)氰化钠是一种剧毒物质,处理该物质的方法之一是在碱性条件下通入氯气,其中CN-被氧化成CO
 和N2,写出该反应的离子方式
和N2,写出该反应的离子方式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下列反应或者现象主要体现了硝酸的什么性质?久置浓硝酸显黄色________ (填序号,下同),用稀硝酸清洗试管壁上的银________ ,稀硝酸清洗石灰水试剂瓶壁上的固体________ ,用浓硝酸清洗积碳的试管________ 。
①(强)氧化性 ②酸性 ③还原性 ④不稳定性 ⑤挥发性 ⑥脱水性 ⑦吸水性
①(强)氧化性 ②酸性 ③还原性 ④不稳定性 ⑤挥发性 ⑥脱水性 ⑦吸水性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知: 为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:
为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:
(1)若镁条在 中燃烧生成黑色粉末(单质)和白色粉末,则
中燃烧生成黑色粉末(单质)和白色粉末,则 的化学式为
的化学式为_______ 。
(2)若常温下, 能与氢氟酸反应生成一种气体和一种液态化合物。
能与氢氟酸反应生成一种气体和一种液态化合物。 和纯碱混合在铁坩埚中熔融生成R的含氧酸盐,
和纯碱混合在铁坩埚中熔融生成R的含氧酸盐, 和纯碱反应的化学方程式为
和纯碱反应的化学方程式为_______ 。
(3)若向酸性 溶液、含酚酞的烧碱溶液中分别通入无色气体
溶液、含酚酞的烧碱溶液中分别通入无色气体 ,两溶液颜色均逐渐褪去。酸性
,两溶液颜色均逐渐褪去。酸性 溶液吸收
溶液吸收 的离子方程式为
的离子方程式为_______ ;向烧碱溶液中通入过量 的离子方程式为
的离子方程式为_______ 。
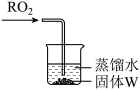
(4)设NA为阿伏加德罗常数的值。若烧杯中固体W为银粉,向该烧杯中通入 ,固体W逐渐溶解(如图所示),则
,固体W逐渐溶解(如图所示),则 的化学式为
的化学式为_______ ,向某密闭容器中充入 和
和 ,则产物的分子数
,则产物的分子数_______ (填“大于”、“小于”或“等于”)2NA。
(5)若 是一种绿色饮用水消毒剂,则
是一种绿色饮用水消毒剂,则 具有
具有_______ 性而能杀菌消毒;工业上,常用+5价R的含氧酸的钠盐和HR的浓溶液在常温下反应制备气态 ,同时还有R单质和水生成,该反应的离子方程式为
,同时还有R单质和水生成,该反应的离子方程式为_______ 。
 为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:
为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:(1)若镁条在
 中燃烧生成黑色粉末(单质)和白色粉末,则
中燃烧生成黑色粉末(单质)和白色粉末,则 的化学式为
的化学式为(2)若常温下,
 能与氢氟酸反应生成一种气体和一种液态化合物。
能与氢氟酸反应生成一种气体和一种液态化合物。 和纯碱混合在铁坩埚中熔融生成R的含氧酸盐,
和纯碱混合在铁坩埚中熔融生成R的含氧酸盐, 和纯碱反应的化学方程式为
和纯碱反应的化学方程式为(3)若向酸性
 溶液、含酚酞的烧碱溶液中分别通入无色气体
溶液、含酚酞的烧碱溶液中分别通入无色气体 ,两溶液颜色均逐渐褪去。酸性
,两溶液颜色均逐渐褪去。酸性 溶液吸收
溶液吸收 的离子方程式为
的离子方程式为 的离子方程式为
的离子方程式为(4)设NA为阿伏加德罗常数的值。若烧杯中固体W为银粉,向该烧杯中通入
 ,固体W逐渐溶解(如图所示),则
,固体W逐渐溶解(如图所示),则 的化学式为
的化学式为 和
和 ,则产物的分子数
,则产物的分子数
(5)若
 是一种绿色饮用水消毒剂,则
是一种绿色饮用水消毒剂,则 具有
具有 ,同时还有R单质和水生成,该反应的离子方程式为
,同时还有R单质和水生成,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铜是生命必需的元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响。在化学反应中,铜元素可表现为0、+1、+2价。
(1)火法炼铜的原理:Cu2S+O2=2Cu+SO2 在Cu2S中铜的化合价为_______ 。
(2)《宋史·食货志》中有这样一段话:“浸铜之法,以生铁煅成薄铁片,排置胆水槽中,浸渍数日,铁片为胆水所薄,上生赤煤。去刮赤煤,入炉三炼成铜。大率用铁二斤四两得铜一斤。”文中胆水是_______ ,赤煤是_______ ,试写出该反应的化学方程式:_______ 。
(3)尽管铜比铁稳定,但铜器表面经常会生成铜锈[即铜绿,化学式为Cu2(OH)2CO3],其中生成铜绿的反应物除铜外还有O2、CO2和H2O。试写出保护铜制品的方法:_______ ;这层铜绿可用化学方法除去,试写出除去铜绿而不伤器物的离子方程式:_______ 。
(4)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析为什么铜常用于制造货币(铜的熔点是1 083.4 ℃,铁的熔点是1 534.8 ℃)。_______
(1)火法炼铜的原理:Cu2S+O2=2Cu+SO2 在Cu2S中铜的化合价为
(2)《宋史·食货志》中有这样一段话:“浸铜之法,以生铁煅成薄铁片,排置胆水槽中,浸渍数日,铁片为胆水所薄,上生赤煤。去刮赤煤,入炉三炼成铜。大率用铁二斤四两得铜一斤。”文中胆水是
(3)尽管铜比铁稳定,但铜器表面经常会生成铜锈[即铜绿,化学式为Cu2(OH)2CO3],其中生成铜绿的反应物除铜外还有O2、CO2和H2O。试写出保护铜制品的方法:
(4)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析为什么铜常用于制造货币(铜的熔点是1 083.4 ℃,铁的熔点是1 534.8 ℃)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。请根据题中提供的信息,回答下列问题:
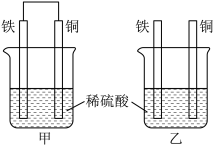
(1)将纯铁片和纯铜片按图甲、乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
①下列说法正确的是___________ 。
A.甲、乙均为化学能转变为电能的装置
B.甲、乙中铜片上均没有明显现象
C.甲、乙中铁片质量均减少
D.甲、乙两烧杯中 均减小
均减小
②在相同时间内,两烧杯中产生气泡的速度:甲___________ 乙(填“>”、“<”或“=”、“无法判断”)。
③请写出甲、乙中构成原电池的正极电极反应式:___________ 。电池工作时,溶液中 向
向___________ 极(填“铜极”或“铁极”)移动。当构成原电池的溶液质量增重27g时,电极上转移电子数目为___________ 。
④若将甲中的稀硫酸换为浓硝酸,则电池总反应的离子方程式为___________ 。
(2)燃料电池是目前电池研究的热点之一,某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。

①正极是___________ (填“a”或“b”),a极发生的电极反应式是___________ 。
②将上图 改成甲烷,电解质溶液改成
改成甲烷,电解质溶液改成 溶液。通甲烷电极反应式为
溶液。通甲烷电极反应式为___________ 。
(3)用燃料电池做电源,用惰性电极电解饱和食盐水,电解总反应方程式为___________ 。
(1)将纯铁片和纯铜片按图甲、乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
①下列说法正确的是

A.甲、乙均为化学能转变为电能的装置
B.甲、乙中铜片上均没有明显现象
C.甲、乙中铁片质量均减少
D.甲、乙两烧杯中
 均减小
均减小②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出甲、乙中构成原电池的正极电极反应式:
 向
向④若将甲中的稀硫酸换为浓硝酸,则电池总反应的离子方程式为
(2)燃料电池是目前电池研究的热点之一,某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。

①正极是
②将上图
 改成甲烷,电解质溶液改成
改成甲烷,电解质溶液改成 溶液。通甲烷电极反应式为
溶液。通甲烷电极反应式为(3)用燃料电池做电源,用惰性电极电解饱和食盐水,电解总反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如下图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)─空气燃料电池(如图甲)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。
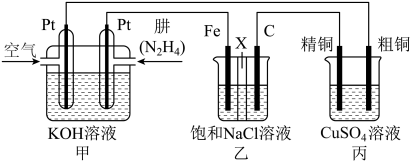
根据要求回答相关问题:
(1)甲装置中通入____ 气体的一极为正极,其电极反应式为:__________ 。
(2)乙装置中石墨电极为_____ 极(填“阳”或“阴”,其电极反应式为_____ ;可以用_____ 检验该反应产物,电解一段时间后,乙池中的溶液呈_________ 性。
(3)图中用丙装置模拟工业中的_________ 原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为_________ g。
(4)如果将丙中的粗铜电极换为Pt电极,则丙中总化学方程式为________ 。

根据要求回答相关问题:
(1)甲装置中通入
(2)乙装置中石墨电极为
(3)图中用丙装置模拟工业中的
(4)如果将丙中的粗铜电极换为Pt电极,则丙中总化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】锂—空气电池能够提供相当于普通锂离子电池l0倍的能量,因此它是最有前途的电池技术。下图是锂—空气电池放电和充电时的工作示意图。
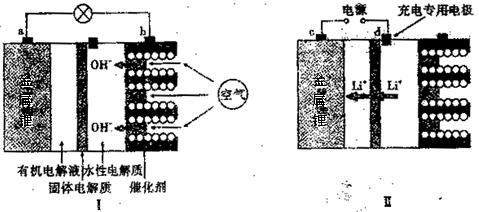
(1)图I中电极a是_____________ 极。
(2)用锂一空气电池电解100mL 0.5mol/L CuSO4溶液,当电池中消耗1.4g Li时,在阴极会析出_________ g铜。
(3)电池中间的固体电解质(含阳离子交换膜)能阻止H2O、N2、O2等物质的通过,防止Li和这些物质反应。Li和水在常温下发生反应的化学方程式为_____ 。
(4)当给图Ⅱ中的锂空气电池充电时,d极应接电源的_______ 极,该电极的电极反应式为___________ 。

(1)图I中电极a是
(2)用锂一空气电池电解100mL 0.5mol/L CuSO4溶液,当电池中消耗1.4g Li时,在阴极会析出
(3)电池中间的固体电解质(含阳离子交换膜)能阻止H2O、N2、O2等物质的通过,防止Li和这些物质反应。Li和水在常温下发生反应的化学方程式为
(4)当给图Ⅱ中的锂空气电池充电时,d极应接电源的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】将25.0g  、
、 、
、 、
、 、
、 和少量杂质(不含钠,不与水、酸、碱反应)的混合物投入到大量水中充分反应,然后向所得溶液中逐滴加入2.5mol/L、200mL盐酸。已知:a.加酸之前,生成气体的体积为1.68L(标况下);b.加酸之后,酸的体积小于140mL时无气体生成;c.全部酸加完之后,所得溶液为中性。
和少量杂质(不含钠,不与水、酸、碱反应)的混合物投入到大量水中充分反应,然后向所得溶液中逐滴加入2.5mol/L、200mL盐酸。已知:a.加酸之前,生成气体的体积为1.68L(标况下);b.加酸之后,酸的体积小于140mL时无气体生成;c.全部酸加完之后,所得溶液为中性。
(1)写出加水后发生的氧化还原反应的离子方程式___________ ;
(2)检验加水后所得溶液中阳离子的方法是___________ ;
(3)则原混合物中钠元素的质量分数为___________ 。
 、
、 、
、 、
、 、
、 和少量杂质(不含钠,不与水、酸、碱反应)的混合物投入到大量水中充分反应,然后向所得溶液中逐滴加入2.5mol/L、200mL盐酸。已知:a.加酸之前,生成气体的体积为1.68L(标况下);b.加酸之后,酸的体积小于140mL时无气体生成;c.全部酸加完之后,所得溶液为中性。
和少量杂质(不含钠,不与水、酸、碱反应)的混合物投入到大量水中充分反应,然后向所得溶液中逐滴加入2.5mol/L、200mL盐酸。已知:a.加酸之前,生成气体的体积为1.68L(标况下);b.加酸之后,酸的体积小于140mL时无气体生成;c.全部酸加完之后,所得溶液为中性。(1)写出加水后发生的氧化还原反应的离子方程式
(2)检验加水后所得溶液中阳离子的方法是
(3)则原混合物中钠元素的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)0.3molNH3分子中所含原子数与___________ 个H2O分子中所含原子数相等。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有______________ (填“氧化性”或“还原性”);
(3)现有一含有FeCl2 和FeCl3的混合样品,实验测得n(Fe)∶n(Cl)=1∶2.1,则该样品中FeCl3 的物质的量分数为_________ 。
(4)某无色透明溶液中可能大量存在Ag+,Mg2+,Cu2+中的几种离子:
a. 取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,
取滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是_________ ,
b. 原溶液中可能大量存在的阴离子是下列A-D中的(填序号)_________ 。
A.Cl- B.NO3- C.CO32- D.OH-
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有
(3)现有一含有FeCl2 和FeCl3的混合样品,实验测得n(Fe)∶n(Cl)=1∶2.1,则该样品中FeCl3 的物质的量分数为
(4)某无色透明溶液中可能大量存在Ag+,Mg2+,Cu2+中的几种离子:
a. 取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,
取滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是
b. 原溶液中可能大量存在的阴离子是下列A-D中的(填序号)
A.Cl- B.NO3- C.CO32- D.OH-
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有一混合溶液,只可能含有以下离子中的若干种:K+、 、Cl-、Ba2+、
、Cl-、Ba2+、 、
、 取三份各100mL该混合溶液进行如下实验。
取三份各100mL该混合溶液进行如下实验。
实验①:向第一份混合溶液中加入AgNO3溶液,有沉淀产生;
实验②:向第二份混合溶液中加入足量NaOH溶液,加热,收集到0.08mol气体;
实验③:向第三份混合溶液中加入足量BaCl2溶液后,得到干燥的沉淀12.54g,经足量稀盐酸洗涤、干燥后,沉淀质量为4.66g。
(已知: +OH-
+OH- H2O+NH3↑)
H2O+NH3↑)
根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液__________ (填“一定”或“不一定”)含有Cl-。
(2)由实验②推断该混合溶液中应含有__________ (填离子符号),其物质的量浓度为______________ 。
(3)由实验③可知12.54g沉淀的成分为_______________ (填化学式)。
(4)综合上述实验,你认为以下结论正确的是______________ (填标号)。
A.该混合溶液中一定含有K+、 、
、 、
、 ,可能含Cl-,且n(K+)≥0.04mol
,可能含Cl-,且n(K+)≥0.04mol
B.该混合溶液中一定含有 、
、 、
、 ,可能含Ba2+、K+、Cl-
,可能含Ba2+、K+、Cl-
C.该混合溶液中一定含有 、
、 、
、 ,可能含K+、Cl-
,可能含K+、Cl-
D.该混合溶液中一定含有 、
、 ,可能含K+、Cl-
,可能含K+、Cl-
 、Cl-、Ba2+、
、Cl-、Ba2+、 、
、 取三份各100mL该混合溶液进行如下实验。
取三份各100mL该混合溶液进行如下实验。实验①:向第一份混合溶液中加入AgNO3溶液,有沉淀产生;
实验②:向第二份混合溶液中加入足量NaOH溶液,加热,收集到0.08mol气体;
实验③:向第三份混合溶液中加入足量BaCl2溶液后,得到干燥的沉淀12.54g,经足量稀盐酸洗涤、干燥后,沉淀质量为4.66g。
(已知:
 +OH-
+OH- H2O+NH3↑)
H2O+NH3↑)根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液
(2)由实验②推断该混合溶液中应含有
(3)由实验③可知12.54g沉淀的成分为
(4)综合上述实验,你认为以下结论正确的是
A.该混合溶液中一定含有K+、
 、
、 、
、 ,可能含Cl-,且n(K+)≥0.04mol
,可能含Cl-,且n(K+)≥0.04molB.该混合溶液中一定含有
 、
、 、
、 ,可能含Ba2+、K+、Cl-
,可能含Ba2+、K+、Cl-C.该混合溶液中一定含有
 、
、 、
、 ,可能含K+、Cl-
,可能含K+、Cl-D.该混合溶液中一定含有
 、
、 ,可能含K+、Cl-
,可能含K+、Cl-
您最近一年使用:0次



