氮、氧、硫、氯是四种重要的非金属元素,研究它们的性质及用途对生产、生活、科研具有重要意义。
(1) 、
、 、
、 、
、 等物质常被用作消毒剂。
等物质常被用作消毒剂。
①一氯胺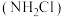 是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质
是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质 ,请写出物质
,请写出物质 的电子式
的电子式___________ 。
②二氧化氯 是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用
是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用 氧化
氧化 溶液制取
溶液制取 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为___________ 。
③等物质的量下列物质消毒效率最高的是___________ (填序号;已知:消毒效率可用单位物质的量的消毒剂的氧化能力衡量)。
a. b.
b. c.
c. d.
d.
(2) 、
、 两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收
两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收 能得到含
能得到含 和
和 的吸收液。写出生成
的吸收液。写出生成 的离子方程式:
的离子方程式:___________ 。若向吸收液中通入过量 ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(3) 与
与 溶液反应可制取“84”消毒液。用过量的冷
溶液反应可制取“84”消毒液。用过量的冷 溶液吸收氯气,制得
溶液吸收氯气,制得 溶液(不含
溶液(不含 ),此时
),此时 的浓度为
的浓度为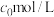 ;加热时
;加热时 能转化为
能转化为 ,测得
,测得 时刻溶液中
时刻溶液中 的浓度为
的浓度为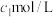 (不考虑加热前后溶液体积的变化)。
(不考虑加热前后溶液体积的变化)。
①写出溶液中 分解生成
分解生成 的化学方程式:
的化学方程式:___________ 。
② 时刻溶液中
时刻溶液中
___________  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
(1)
 、
、 、
、 、
、 等物质常被用作消毒剂。
等物质常被用作消毒剂。①一氯胺
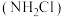 是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质
是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质 ,请写出物质
,请写出物质 的电子式
的电子式②二氧化氯
 是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用
是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用 氧化
氧化 溶液制取
溶液制取 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为③等物质的量下列物质消毒效率最高的是
a.
 b.
b. c.
c. d.
d.
(2)
 、
、 两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收
两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收 能得到含
能得到含 和
和 的吸收液。写出生成
的吸收液。写出生成 的离子方程式:
的离子方程式: ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(3)
 与
与 溶液反应可制取“84”消毒液。用过量的冷
溶液反应可制取“84”消毒液。用过量的冷 溶液吸收氯气,制得
溶液吸收氯气,制得 溶液(不含
溶液(不含 ),此时
),此时 的浓度为
的浓度为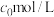 ;加热时
;加热时 能转化为
能转化为 ,测得
,测得 时刻溶液中
时刻溶液中 的浓度为
的浓度为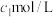 (不考虑加热前后溶液体积的变化)。
(不考虑加热前后溶液体积的变化)。①写出溶液中
 分解生成
分解生成 的化学方程式:
的化学方程式:②
 时刻溶液中
时刻溶液中
 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
更新时间:2023-10-09 11:12:50
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氮的很多化合物都是重要的化工原料。
(1)羟胺( )可看成是氨分子内的一个氢原子被羟基取代的衍生物。
)可看成是氨分子内的一个氢原子被羟基取代的衍生物。 的电子式为
的电子式为___________ 。写出两种与羟胺的价电子数相同的双核分子的化学式___________ 。纯羟胺很不稳定,受热即分解为 、
、 和
和 ,则
,则 分解反应的化学方程式:
分解反应的化学方程式:___________ 。
(2)“肼合成酶”以其中的 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼(
转化为肼(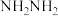 ),其反应历程如下所示。
),其反应历程如下所示。

下列说法正确的是___________ 。
a.反应涉及 、
、 键断裂和
键断裂和 键生成
键生成
b. 、
、 和
和 均为极性分子
均为极性分子
c.催化中心的 先被氧化为
先被氧化为 ,后又被还原为
,后又被还原为
若将 替换为
替换为 ,则表示该过程的化学方程式为:
,则表示该过程的化学方程式为:___________ (催化剂可用“ ”表示)。
”表示)。
(3)联氨(又称肼, ,无色液体)是一种应用广泛的化工原料,实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为
,无色液体)是一种应用广泛的化工原料,实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________ 。联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的平衡常数值为___________ (已知: 的
的 ;
; )。联氨与硫酸形成的酸式盐的化学式为
)。联氨与硫酸形成的酸式盐的化学式为___________ 。
(1)羟胺(
 )可看成是氨分子内的一个氢原子被羟基取代的衍生物。
)可看成是氨分子内的一个氢原子被羟基取代的衍生物。 的电子式为
的电子式为 、
、 和
和 ,则
,则 分解反应的化学方程式:
分解反应的化学方程式:(2)“肼合成酶”以其中的
 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼(
转化为肼(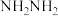 ),其反应历程如下所示。
),其反应历程如下所示。
下列说法正确的是
a.反应涉及
 、
、 键断裂和
键断裂和 键生成
键生成b.
 、
、 和
和 均为极性分子
均为极性分子c.催化中心的
 先被氧化为
先被氧化为 ,后又被还原为
,后又被还原为
若将
 替换为
替换为 ,则表示该过程的化学方程式为:
,则表示该过程的化学方程式为: ”表示)。
”表示)。(3)联氨(又称肼,
 ,无色液体)是一种应用广泛的化工原料,实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为
,无色液体)是一种应用广泛的化工原料,实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为 的
的 ;
; )。联氨与硫酸形成的酸式盐的化学式为
)。联氨与硫酸形成的酸式盐的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】含碳元素的物质是化学世界中最庞大的家族,请填写下列空格。
(1)用电子式表示CO2的形成过程____ 。
(2)已知CN-与N2结构相似,则NaCN的电子式为_____ 。
(3)C60分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则C60分子中σ键和π键的数目之比为_____ 。
(4)乙酸乙酯分子中含有的σ键和π键数目之比为____ ,碳原子的杂化方式为____ 。
(1)用电子式表示CO2的形成过程
(2)已知CN-与N2结构相似,则NaCN的电子式为
(3)C60分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则C60分子中σ键和π键的数目之比为
(4)乙酸乙酯分子中含有的σ键和π键数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
(6) ②、③、⑦的气态氢化物中最不稳定的是___________ (填化学式);
(7)用电子式表示H2O的形成过程___________________ 。
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)写出③和⑥两种元素的元素符号:③
(2)②和④两种元素形成的共价化合物的电子式是
(3)元素②的气态氢化物的分子式为
元素⑨最高价氧化物对应水化物的分子式为
(4)④、⑤、⑧的原子半径由大到小的顺序为
(5) ②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(6) ②、③、⑦的气态氢化物中最不稳定的是
(7)用电子式表示H2O的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)常温常压下,将 与
与 的混合气体10L与25L氧气混合,点燃后充分反应,则剩余气体为24L(恢复为常温常压),则原来混合气体中
的混合气体10L与25L氧气混合,点燃后充分反应,则剩余气体为24L(恢复为常温常压),则原来混合气体中 与
与 的体积比为
的体积比为___________ 。
(2)氨气极易溶于水,氨气溶于水得到的溶液称为氨水。将标准状况下11.2L氨气溶于100mL水中,得到密度为 的氨水。求所得氨水的物质的量浓度
的氨水。求所得氨水的物质的量浓度___________ 。
(1)常温常压下,将
 与
与 的混合气体10L与25L氧气混合,点燃后充分反应,则剩余气体为24L(恢复为常温常压),则原来混合气体中
的混合气体10L与25L氧气混合,点燃后充分反应,则剩余气体为24L(恢复为常温常压),则原来混合气体中 与
与 的体积比为
的体积比为(2)氨气极易溶于水,氨气溶于水得到的溶液称为氨水。将标准状况下11.2L氨气溶于100mL水中,得到密度为
 的氨水。求所得氨水的物质的量浓度
的氨水。求所得氨水的物质的量浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】将4g铁粉与2.5g硫粉在研钵中充分混合后装入试管中,在试管口塞上带长导管的橡皮塞,并在导管末端放入一小团蘸有NaOH溶液的棉花,加热试管。


(1)写出铁与硫反应的化学方程式___________ 。
(2)已知硫的熔点为106.8℃、沸点为444.7℃,解释试管口为什么向上倾斜___________ 。
(3)棉花中的NaOH用于吸收反应过程中产生的二氧化硫,写出该反应的离子方程式___________ 。
(4)工业上通常用接触法制硫酸。在制硫酸的生产中,若有32吨硫黄最终全部转化为硫酸,则可以制得质量分数为98%的浓硫酸为___________ 吨。已知98%的硫酸密度为1.84g/cm3,计算此溶液的物质的量浓度为___________ mol/L。


(1)写出铁与硫反应的化学方程式
(2)已知硫的熔点为106.8℃、沸点为444.7℃,解释试管口为什么向上倾斜
(3)棉花中的NaOH用于吸收反应过程中产生的二氧化硫,写出该反应的离子方程式
(4)工业上通常用接触法制硫酸。在制硫酸的生产中,若有32吨硫黄最终全部转化为硫酸,则可以制得质量分数为98%的浓硫酸为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)最近材料科学家发现了首例带结晶水的晶体在5K下呈现超导性。该晶体的化学式为Na0.35CoO2·1.3H2O(该晶体的摩尔质量为122g·mol-1),若用NA表示阿伏加 德罗常数,则12.2g该晶体中含氧原子数为___ ,氢原子的物质的量为___ mol。
(2)FeCl3溶液可以用来净水,用100mL2mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数___ (填“大于”“等于”或“小于”)0.2NA。
(3)在标准状况下,VL某气体(摩尔质量为Mg/mol)溶解在1L水(水的密度近似为1g/cm3)中,假设气体完全溶解且不与水发生反应,所得溶液的密度为ρg/cm3,则所得溶液的物质的量浓度c=___ mol/L(用以上字母表示,且必须化简)。
(4)工业上用亚氯酸钠和稀盐酸为原料制备ClO2反应:NaClO2+HCl→ClO2↑+NaCl+H2O。写出配平的化学方程式____ 。
(5)向100mL的FeBr2溶液中通入标准状况下Cl23.36L(已知还原性:Fe2+>Br-),反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为____ mol/L。反应的离子方程式为____ 。
(6)若向盛有10mL1mol·L-1NH4Al(SO4)2溶液的烧杯中加20mL1.2mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为____ mol。
(2)FeCl3溶液可以用来净水,用100mL2mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数
(3)在标准状况下,VL某气体(摩尔质量为Mg/mol)溶解在1L水(水的密度近似为1g/cm3)中,假设气体完全溶解且不与水发生反应,所得溶液的密度为ρg/cm3,则所得溶液的物质的量浓度c=
(4)工业上用亚氯酸钠和稀盐酸为原料制备ClO2反应:NaClO2+HCl→ClO2↑+NaCl+H2O。写出配平的化学方程式
(5)向100mL的FeBr2溶液中通入标准状况下Cl23.36L(已知还原性:Fe2+>Br-),反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为
(6)若向盛有10mL1mol·L-1NH4Al(SO4)2溶液的烧杯中加20mL1.2mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
【推荐1】通过“价类二维图”研究物质性质是化学研究的重要方法,下图是氯元素的部分化合价与物质类别的对应关系。

请回答:
(1)X化学式为___________ 。
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为 ,则
,则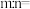
___________ 。
(3) 与Z都可用于消毒,等物质的量的两种物质,消毒效率
与Z都可用于消毒,等物质的量的两种物质,消毒效率
___________ Z(填“<”或“=”或“>”,消毒效率以单位物质的量得到的电子数表示)。
(4)Y可用于实验室制取 ,其焰色试验为紫色(透过蓝色钴玻璃观察),请写出由Y与盐酸在加热条件下制备Z的离子方程式
,其焰色试验为紫色(透过蓝色钴玻璃观察),请写出由Y与盐酸在加热条件下制备Z的离子方程式___________ 。

请回答:
(1)X化学式为
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为
 ,则
,则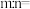
(3)
 与Z都可用于消毒,等物质的量的两种物质,消毒效率
与Z都可用于消毒,等物质的量的两种物质,消毒效率
(4)Y可用于实验室制取
 ,其焰色试验为紫色(透过蓝色钴玻璃观察),请写出由Y与盐酸在加热条件下制备Z的离子方程式
,其焰色试验为紫色(透过蓝色钴玻璃观察),请写出由Y与盐酸在加热条件下制备Z的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】漂白粉的主要成分是次氯酸钙和氯化钙。请回答下列问题:
(1)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式(若涉及氧化还原反应,请标注电子转移情况):____________________________ 。
(2)某化学小组将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,共收集到标准状况下448mL气体,则该漂白粉中所含有效成份的质量为_____________ (假设漂白粉中的其它成份不与硝酸反应)。
(1)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式(若涉及氧化还原反应,请标注电子转移情况):
(2)某化学小组将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,共收集到标准状况下448mL气体,则该漂白粉中所含有效成份的质量为
您最近一年使用:0次
【推荐3】回答下列问题:
(1)实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为2KMnO4 K2MnO4+MnO2+O2↑,其中被氧化的元素是
K2MnO4+MnO2+O2↑,其中被氧化的元素是___________ (填元素符号),还原产物是___________ (填化学式)。
(2)反应方程式:K2Cr2O7+14HCl 2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是
2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是___________ ,氧化产物是___________ 。
(3)下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
1、反应②的离子方程式为___________ 。
II、反应①中,氧化产物与还原产物的质量比为___________ 。
III、已知反应④:4HCl+O2 2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为___________ 。
IV、配平③______KMnO4+_____HCl(浓)=_____KCl+____MnCl2+_____Cl2↑+____H2O,___________
(1)实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为2KMnO4
 K2MnO4+MnO2+O2↑,其中被氧化的元素是
K2MnO4+MnO2+O2↑,其中被氧化的元素是(2)反应方程式:K2Cr2O7+14HCl
 2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是
2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是(3)下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
1、反应②的离子方程式为
II、反应①中,氧化产物与还原产物的质量比为
III、已知反应④:4HCl+O2
 2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为IV、配平③______KMnO4+_____HCl(浓)=_____KCl+____MnCl2+_____Cl2↑+____H2O,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体体积在同温同压下测定)。试回答问题:
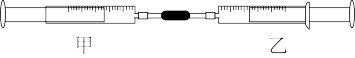
(1)实验1中发生反应的离子方程式为:___________ 。
(2)实验2反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入___________ 溶液中。
(3)实验3中能看见有白烟产生并生成一种气体(空气主要成分之一),该化学反应方程式___________ ,写出检验所得白色固体中阳离子的操作方法:___________ ,充分反应后甲针筒内剩余气体成分为___________ (填化学式)。

| 实验序号 | 甲针筒内物质 | 乙针筒内物质 |
| 1 | 溴水 | SO2 |
| 2 | H2S | SO2 |
| 3 | 15mLCl2 | 35mLNH3 |
(2)实验2反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入
(3)实验3中能看见有白烟产生并生成一种气体(空气主要成分之一),该化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学知识,按要求填空。

(1)上述第一级分类标准(分成A、B组)的依据为___ 。
(2)C组中某一物质常温能与冷水反应,其离子方程式为___ 。
(3)D组中与水反应时氧化剂和还原剂物质的量之比为1:1的物质有____ 。
(4)F组中某一物质的水溶液呈弱碱性,用电离方程式表示呈弱碱性的原因:___ 。
(5)E组中某一物质的水溶液可使酸性KMnO4溶液褪色,用离子方程式表示褪色的原因:___ 。

(1)上述第一级分类标准(分成A、B组)的依据为
(2)C组中某一物质常温能与冷水反应,其离子方程式为
(3)D组中与水反应时氧化剂和还原剂物质的量之比为1:1的物质有
(4)F组中某一物质的水溶液呈弱碱性,用电离方程式表示呈弱碱性的原因:
(5)E组中某一物质的水溶液可使酸性KMnO4溶液褪色,用离子方程式表示褪色的原因:
您最近一年使用:0次



