1,3—丁二烯( )是一种重要化工原料。回答下列问题:
)是一种重要化工原料。回答下列问题:
(1)1,3—丁二烯与乙烯___________ (填“互为”或“不互为”)同系物。
(2)1,3—丁二烯完全燃烧生成 和液态水,将气体产物通入足量澄清石灰水中生成4.0g沉淀,放出热量为akJ,写出表示其燃烧热的热化学方程式:
和液态水,将气体产物通入足量澄清石灰水中生成4.0g沉淀,放出热量为akJ,写出表示其燃烧热的热化学方程式:___________ 。
(3)1,3-丁二烯与溴化氢1:1发生反应时有两种产物,能量变化如图:
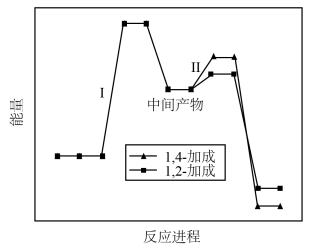
(a)1,2—加成: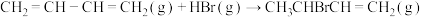

(b)1,4—加成: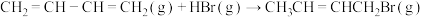

①速控反应活化能:E(a)______ (填“>”“<”或“=”,下同)E(b)。
②

___________ 0。
③热稳定性: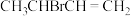
___________ 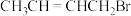 。
。
 )是一种重要化工原料。回答下列问题:
)是一种重要化工原料。回答下列问题:(1)1,3—丁二烯与乙烯
(2)1,3—丁二烯完全燃烧生成
 和液态水,将气体产物通入足量澄清石灰水中生成4.0g沉淀,放出热量为akJ,写出表示其燃烧热的热化学方程式:
和液态水,将气体产物通入足量澄清石灰水中生成4.0g沉淀,放出热量为akJ,写出表示其燃烧热的热化学方程式:(3)1,3-丁二烯与溴化氢1:1发生反应时有两种产物,能量变化如图:

(a)1,2—加成:
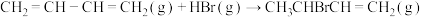

(b)1,4—加成:
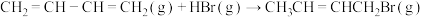

①速控反应活化能:E(a)
②


③热稳定性:
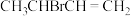
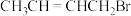 。
。
更新时间:2023-10-10 07:11:51
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1) 根据所学化学反应原理填空:
①升高温度时,水的pH________ (填“增大”“减小”或“不变”)
②体积、pH均相同的盐酸和醋酸溶液,中和等浓度的NaOH溶液时所需体积分别为V1、V2 。则V1_______ V2(填“<”、“>”或“=”)
③某反应放热且熵增加,该反应_________ 自发进行(用“能”或“不能”表示)
(2)依据事实,用化学用语填空:
①1 mol NO2气体与水完全反应生成硝酸溶液和NO气体,放出热量46 kJ。该反应的热化学方程式______________________________________ 。
②用离子方程式表示氯化铵溶液的酸碱性:_________________________________ 。
③用离子方程式表示向碳酸镁沉淀中加入NaOH溶液后的沉淀转化:
_______________________________________________________ 。
①升高温度时,水的pH
②体积、pH均相同的盐酸和醋酸溶液,中和等浓度的NaOH溶液时所需体积分别为V1、V2 。则V1
③某反应放热且熵增加,该反应
(2)依据事实,用化学用语填空:
①1 mol NO2气体与水完全反应生成硝酸溶液和NO气体,放出热量46 kJ。该反应的热化学方程式
②用离子方程式表示氯化铵溶液的酸碱性:
③用离子方程式表示向碳酸镁沉淀中加入NaOH溶液后的沉淀转化:
您最近一年使用:0次
【推荐2】按要求填空
(1) 是一种无色气体,在空气中能发生爆炸性自燃生成固态
是一种无色气体,在空气中能发生爆炸性自燃生成固态 和液态
和液态 。已知室温下
。已知室温下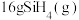 自燃放出热量713.5kJ。写出室温下
自燃放出热量713.5kJ。写出室温下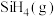 自燃的热化学方程式
自燃的热化学方程式__________ 。
(2)在101kPa时, 在
在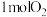 中完全燃烧生成2mol液态水,放出571.6kJ的热量,
中完全燃烧生成2mol液态水,放出571.6kJ的热量, 的燃烧热为
的燃烧热为__________ ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为__________ 。
(3)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量 ,燃烧生成的
,燃烧生成的 用过量饱和石灰水吸收可得
用过量饱和石灰水吸收可得 沉淀,则在此条件下,1mol乙醇完全燃烧的
沉淀,则在此条件下,1mol乙醇完全燃烧的
__________ kJ/mol。
(4)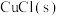 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应每转移
和一种黑色固体。在25℃、101kPa下,已知该反应每转移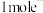 ,放热44.5kJ,该反应的热化学方程式
,放热44.5kJ,该反应的热化学方程式__________ 。
(5)已知反应:

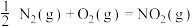



则反应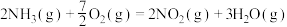 的
的 为
为__________ kJ/mol(用 ,
, ,
, 表示)
表示)
(1)
 是一种无色气体,在空气中能发生爆炸性自燃生成固态
是一种无色气体,在空气中能发生爆炸性自燃生成固态 和液态
和液态 。已知室温下
。已知室温下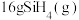 自燃放出热量713.5kJ。写出室温下
自燃放出热量713.5kJ。写出室温下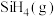 自燃的热化学方程式
自燃的热化学方程式(2)在101kPa时,
 在
在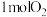 中完全燃烧生成2mol液态水,放出571.6kJ的热量,
中完全燃烧生成2mol液态水,放出571.6kJ的热量, 的燃烧热为
的燃烧热为 燃烧热的热化学方程式为
燃烧热的热化学方程式为(3)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量
 ,燃烧生成的
,燃烧生成的 用过量饱和石灰水吸收可得
用过量饱和石灰水吸收可得 沉淀,则在此条件下,1mol乙醇完全燃烧的
沉淀,则在此条件下,1mol乙醇完全燃烧的
(4)
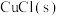 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应每转移
和一种黑色固体。在25℃、101kPa下,已知该反应每转移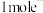 ,放热44.5kJ,该反应的热化学方程式
,放热44.5kJ,该反应的热化学方程式(5)已知反应:


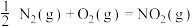



则反应
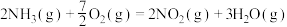 的
的 为
为 ,
, ,
, 表示)
表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)写出下列反应的热化学方程式:
①32g铜粉在足量氧气中反应生成氧化铜固体时放出78.5kJ热量:____ 。
②一氧化碳气体还原Fe3O4得到1mol单质铁时放出14.7kJ热量:____ 。
(2)工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)=CH3OH(g),反应过程中的能量变化情况如图所示。
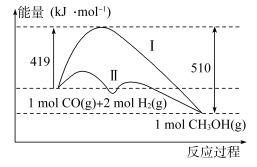
①曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。计算当反应生成1.5molCH3OH(g)时,能量变化值是____ kJ。
②选择适宜的催化剂____ (填“能”或“不能”)改变该反应的反应热。
(3)断开1molH—H键、1molN—H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、946kJ,则1molH2与足量N2反应生成NH3需____ (填“吸收”或“放出”)能量____ kJ。(小数点后保留两位数字),事实上,反应的热量总小于理论值,理由是____ 。
(1)写出下列反应的热化学方程式:
①32g铜粉在足量氧气中反应生成氧化铜固体时放出78.5kJ热量:
②一氧化碳气体还原Fe3O4得到1mol单质铁时放出14.7kJ热量:
(2)工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)=CH3OH(g),反应过程中的能量变化情况如图所示。

①曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。计算当反应生成1.5molCH3OH(g)时,能量变化值是
②选择适宜的催化剂
(3)断开1molH—H键、1molN—H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、946kJ,则1molH2与足量N2反应生成NH3需
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】汽车尾气中的氮氧化物是城市空气的主要污染物之一,如何降低汽车尾气污染已成为环保领域的热点。
回答下列问题:
(1)科技工作者用甲烷将氮氧化物还原为 N2和 H2O,涉及的反应如下:
CH4(g)+4NO2(g) =4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ/mol
CH4(g)+2NO2(g) =CO2(g)+2H2O(g)+N2(g) ΔH2=-867 kJ/mol
则 CH4(g)还原 NO(g)生成 N2(g)的热化学方程式为___________ 。
(2)使用氢能源可以减少汽车尾气中有害气体的排放。利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g) =CO2(g)+3H2(g) ΔH,该反应过程中的能量变化如图:
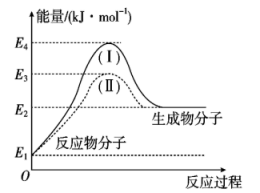
①ΔH___________ 0(填“>”“=”或“<”)。
②途径(Ⅰ)的活化能 E=___________ 。
③途径(Ⅰ)变为途径(Ⅱ):改变的条件是___________ ,反应热(ΔH)___________ (填“增大”“减小”或“不变”)。
回答下列问题:
(1)科技工作者用甲烷将氮氧化物还原为 N2和 H2O,涉及的反应如下:
CH4(g)+4NO2(g) =4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ/mol
CH4(g)+2NO2(g) =CO2(g)+2H2O(g)+N2(g) ΔH2=-867 kJ/mol
则 CH4(g)还原 NO(g)生成 N2(g)的热化学方程式为
(2)使用氢能源可以减少汽车尾气中有害气体的排放。利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g) =CO2(g)+3H2(g) ΔH,该反应过程中的能量变化如图:

①ΔH
②途径(Ⅰ)的活化能 E=
③途径(Ⅰ)变为途径(Ⅱ):改变的条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察图象,然后回答问题。

(1)图中所示反应是______ (填“吸热”或“放热”)反应,该反应的△H =_______ (用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+ O2(g) =H2O(g) △H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为
O2(g) =H2O(g) △H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为______ 。

(1)图中所示反应是
(2)已知热化学方程式:H2(g)+
 O2(g) =H2O(g) △H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为
O2(g) =H2O(g) △H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为
您最近一年使用:0次
【推荐1】有机物是生命产生的物质基础,其种类繁多。下列各组物质:① 与
与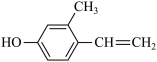 ②CH3CH2CH2CHO与CH3COCH2CH3;③淀粉和纤维素;④正戊烷和2-甲基丁烷;⑤
②CH3CH2CH2CHO与CH3COCH2CH3;③淀粉和纤维素;④正戊烷和2-甲基丁烷;⑤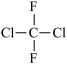 和
和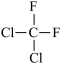 ;⑥
;⑥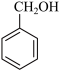 和
和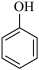 ;⑦2-甲基-1,3-丁二烯和1,3-丁二烯
;⑦2-甲基-1,3-丁二烯和1,3-丁二烯
(1)互为同系物的是_________________ ;(填序号,下同);互为同分异构体的是____________ ;
(2)物质 的含氧官能团名称为
的含氧官能团名称为_______________ ;
(3)某单烯烃与足量氢气反应后能生成2-甲基丁烷,已知该烯烃分子中含有 3 个甲基,该烯烃的系统命名为______________ ;该烯烃在催化剂作用下,发生加聚反应产生高分子物质的化学方程式为_____________ ;
(4)某烃为正戊烷的同系物,其相对分子质量为114,其一氯代物只有一种,该烃的系统命名为_________ 。
(5)已知烯烃能够被臭氧氧化,其过程为: ,若将②中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为
,若将②中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为_________________________ 。
 与
与 ②CH3CH2CH2CHO与CH3COCH2CH3;③淀粉和纤维素;④正戊烷和2-甲基丁烷;⑤
②CH3CH2CH2CHO与CH3COCH2CH3;③淀粉和纤维素;④正戊烷和2-甲基丁烷;⑤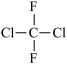 和
和 ;⑥
;⑥ 和
和 ;⑦2-甲基-1,3-丁二烯和1,3-丁二烯
;⑦2-甲基-1,3-丁二烯和1,3-丁二烯(1)互为同系物的是
(2)物质
 的含氧官能团名称为
的含氧官能团名称为(3)某单烯烃与足量氢气反应后能生成2-甲基丁烷,已知该烯烃分子中含有 3 个甲基,该烯烃的系统命名为
(4)某烃为正戊烷的同系物,其相对分子质量为114,其一氯代物只有一种,该烃的系统命名为
(5)已知烯烃能够被臭氧氧化,其过程为:
 ,若将②中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为
,若将②中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.有下列各组微粒或物质,请按要求填空(填序号):
A. 和
和
B.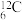 和
和
C. 和
和
D. 和
和
E. 和
和
(1)_________ 组中两种物质互为同素异形体。
(2)_________ 组中两种物质属于同系物。
(3)_________ 组中两种物质互为同分异构体。
Ⅱ.现有A、B、C三种烃,其球棍模型如图:

(4)等质量的以上物质完全燃烧时耗去 的量最多的是
的量最多的是_________ (填序号)。
(5)将 和适量的
和适量的 混合后光照,充分反应后生成的
混合后光照,充分反应后生成的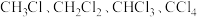 四种有机产物的物质的量依次增大
四种有机产物的物质的量依次增大 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为_________  。
。
(6)将 通入溴的四氯化碳溶液中可使溴的四氯化碳溶液褪色,请写出该反应的化学方程式:
通入溴的四氯化碳溶液中可使溴的四氯化碳溶液褪色,请写出该反应的化学方程式:_________ 。
A.
 和
和
B.
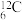 和
和
C.
 和
和
D.
 和
和
E.
 和
和
(1)
(2)
(3)
Ⅱ.现有A、B、C三种烃,其球棍模型如图:

(4)等质量的以上物质完全燃烧时耗去
 的量最多的是
的量最多的是(5)将
 和适量的
和适量的 混合后光照,充分反应后生成的
混合后光照,充分反应后生成的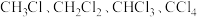 四种有机产物的物质的量依次增大
四种有机产物的物质的量依次增大 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为 。
。(6)将
 通入溴的四氯化碳溶液中可使溴的四氯化碳溶液褪色,请写出该反应的化学方程式:
通入溴的四氯化碳溶液中可使溴的四氯化碳溶液褪色,请写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】有机物种类繁多,现有以下九种有机物:①CH3CH2OH ②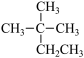 ③
③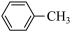 ④CH3CH2CH2CH3 ⑤CH3CH2CH2COOH ⑥
④CH3CH2CH2CH3 ⑤CH3CH2CH2COOH ⑥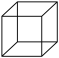 ⑦
⑦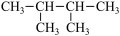 ⑧C2H4 ⑨CH3COOCH2CH3。请从上述有机物中选择适当物质按要求回答下列问题:
⑧C2H4 ⑨CH3COOCH2CH3。请从上述有机物中选择适当物质按要求回答下列问题:
(1)⑤中含有的官能团名称_______ 。
(2)与②互为同系物的是_______ (填序号),用系统命名法命名②为_______ 。某烯烃与1molH2反应可得到②,则该烯烃可能的结构有_______ 种。
(3)③与液氯在FeCl3作催化剂条件下反应生成一氯代物的方程式:_______ (写其中一种即可),③与足量H2反应得到的产物,其一氯代物有_______ 种。
(4)⑥的二氯代物有_______ 种。
(5)在120℃,1.01×105Pa条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是_______ (填序号)。
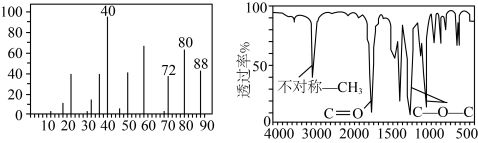
(6)若准确称取4.4g样品X(只含C、H、O三种元素),经充分燃烧后产物依次通过浓硫酸和碱石灰,二者质量分别增加3.6g和8.8g。又知有机物X的质谱图和红外光谱分别如下图所示,则该有机物的分子式为_______ ,结构简式可能为_______ (填序号)。
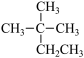 ③
③ ④CH3CH2CH2CH3 ⑤CH3CH2CH2COOH ⑥
④CH3CH2CH2CH3 ⑤CH3CH2CH2COOH ⑥ ⑦
⑦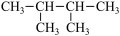 ⑧C2H4 ⑨CH3COOCH2CH3。请从上述有机物中选择适当物质按要求回答下列问题:
⑧C2H4 ⑨CH3COOCH2CH3。请从上述有机物中选择适当物质按要求回答下列问题:(1)⑤中含有的官能团名称
(2)与②互为同系物的是
(3)③与液氯在FeCl3作催化剂条件下反应生成一氯代物的方程式:
(4)⑥的二氯代物有
(5)在120℃,1.01×105Pa条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是
(6)若准确称取4.4g样品X(只含C、H、O三种元素),经充分燃烧后产物依次通过浓硫酸和碱石灰,二者质量分别增加3.6g和8.8g。又知有机物X的质谱图和红外光谱分别如下图所示,则该有机物的分子式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某有机物的结构简式为HO-CH2—CH=CH—CH=CH-CHO。
(1)请你写出下列官能团:
“ ”、“HO-”、“-CHO”的名称:
”、“HO-”、“-CHO”的名称:____ 、____ 、_____ 。
(2)验证该有机物中含有“-CHO”,常采用的试剂是___ ,产生的现象为___ 。
(3)该有机物的性质描述正确的有_______
A.与金属Na反应放出O2 B.能与新制Cu(OH)2反应,产生红色沉淀
C.不能发生银镜反应 D.一定条件下能与H2发生加成反应
(4)1mol该有机物完全与溴水发生加成反应时,需要Br2_______ mol
(1)请你写出下列官能团:
“
 ”、“HO-”、“-CHO”的名称:
”、“HO-”、“-CHO”的名称:(2)验证该有机物中含有“-CHO”,常采用的试剂是
(3)该有机物的性质描述正确的有
A.与金属Na反应放出O2 B.能与新制Cu(OH)2反应,产生红色沉淀
C.不能发生银镜反应 D.一定条件下能与H2发生加成反应
(4)1mol该有机物完全与溴水发生加成反应时,需要Br2
您最近一年使用:0次
【推荐2】完成下列方程式的书写(若有几种有机产物只写主要产物):
(1)丙烯与HBr反应:
____________________________________________________ 。
(2)1,3—丁二烯常温下与Br2等物质的量反应:
_____________________________________________________ 。
(3)2—溴丁烷发生消去反应:
_____________________________________________________ 。
(4)甲苯与Cl2光照条件下等物质的量反应:
___________________________________________________ 。
(1)丙烯与HBr反应:
(2)1,3—丁二烯常温下与Br2等物质的量反应:
(3)2—溴丁烷发生消去反应:
(4)甲苯与Cl2光照条件下等物质的量反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】石油裂化可得到有机物(CH3)2C=C(CH3)2(以下用A表示)。
(1)A的官能团名称为________ ;A在通常状况下呈________ (填“气”“液”或“固”)态。
(2)A与Br2的加成产物B与NaOH的乙醇溶液共热可生成二烯烃C,则C的结构简式为:___________________ ;B生成C的反应类型为______________ 。
(3)C与一定量Br2反应可能生成D、E和G,而D与HBr的加成产物只有F,则D形成高分子化合物的化学方程式为__________________________________________ 。
(4)C的同分异构体中不可能为________ (填字母)
a.芳香烃 b.炔烃 c.环烯烃 d.二烯烃
若C的一种同分异构体H与KMnO4酸性溶液生成己二酸,则H的结构简式为________ ;
(1)A的官能团名称为
(2)A与Br2的加成产物B与NaOH的乙醇溶液共热可生成二烯烃C,则C的结构简式为:
(3)C与一定量Br2反应可能生成D、E和G,而D与HBr的加成产物只有F,则D形成高分子化合物的化学方程式为
(4)C的同分异构体中不可能为
a.芳香烃 b.炔烃 c.环烯烃 d.二烯烃
若C的一种同分异构体H与KMnO4酸性溶液生成己二酸,则H的结构简式为
您最近一年使用:0次



