CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为___________ (写离子符号);若所得溶液c(HCO )∶c(CO
)∶c(CO )=2∶1,溶液pH=
)=2∶1,溶液pH=___________ 。(室温下,H2CO3的K1=4×10−7;K2=5×10−11)
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g) 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。
已知上述反应中相关的化学键键能数据如下:
则该反应的ΔH=___________ 。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是___________ (填“A” 或“B”)。
(3)O2辅助的Al~CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。
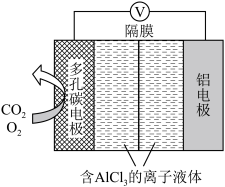
①电池的负极反应式:___________ 。
②电池的正极反应式:6O2+6e‑=6O 、6CO2+6O
、6CO2+6O =3C2O
=3C2O +6O2,反应过程中O2的作用是
+6O2,反应过程中O2的作用是___________ 。
③该电池的总反应式:___________ 。
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为
 )∶c(CO
)∶c(CO )=2∶1,溶液pH=
)=2∶1,溶液pH=(2)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)
 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。已知上述反应中相关的化学键键能数据如下:
| 化学键 | C-H | C=O | H-H | C≡O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
(3)O2辅助的Al~CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。

①电池的负极反应式:
②电池的正极反应式:6O2+6e‑=6O
 、6CO2+6O
、6CO2+6O =3C2O
=3C2O +6O2,反应过程中O2的作用是
+6O2,反应过程中O2的作用是③该电池的总反应式:
更新时间:2023-10-10 17:51:34
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氮是动植物生长不可缺少的元素,氨的制备及应用对农业生产及国防建设均有重大意义,反应如下:N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
(1)合成氨的反应中的能量变化如图所示。
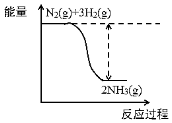
该反应是___ 反应(填“吸热”或“放热”),该热效应来源于反应过程中断裂旧化学键并形成新化学键时的能量变化。已知:断裂1molN≡N键需吸945.6kJ能量,断裂1molH—H键需吸收436kJ能量,形成1molH—N键可放出391kJ能量。试写出NH3的电子式___ ,若生成2molNH3(g),放出___ kJ热量。
(2)一种用于潜艇的液氨—液氧燃料电池原理示意图如图所示。
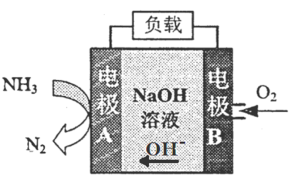
①电极A上,氮元素的化合价___ (填“升高”或“降低”),电极A是___ 极(填“正”或“负”)。
②电极B上发生的电极反应为___ 。
a.O2+H2O+2e-=4OH-
b.O2+2H2O+4e-=4OH-
c.O2+4H++4e-=2H2O
 2NH3(g)。
2NH3(g)。(1)合成氨的反应中的能量变化如图所示。

该反应是
(2)一种用于潜艇的液氨—液氧燃料电池原理示意图如图所示。

①电极A上,氮元素的化合价
②电极B上发生的电极反应为
a.O2+H2O+2e-=4OH-
b.O2+2H2O+4e-=4OH-
c.O2+4H++4e-=2H2O
您最近一年使用:0次
【推荐2】亚硝酰氯(ClNO)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+Cl2(g) 2ClNO(g)。
2ClNO(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:① 2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s)
NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g) 2ClNO(g) K3,则K1、K2、K3之间的关系为K3=
2ClNO(g) K3,则K1、K2、K3之间的关系为K3=_______________ (用K1和K2表示);
(2)已知几种化学键的键能数据如下表:(亚硝酰氯的结构为Cl—N==O)
则2NO(g)+Cl2(g) 2ClNO(g)的反应的 △H和a的关系为 △H =
2ClNO(g)的反应的 △H和a的关系为 △H = ___ kJ·mol-1。
(3)300℃时,2NO(g)+Cl2 (g) 2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:
n = ___ ;k = ____ 。
(4)若向绝热恒容密闭容器中充入物质的量之比为2 : 1的NO和Cl2进行反应2NO(g)+Cl2(g) 2ClNO(g),能判断反应已达到化学平衡状态的是
2ClNO(g),能判断反应已达到化学平衡状态的是__ (填标号)。
a.容器中的压强不变 b.2v正(NO) = v逆(Cl2)c.气体的平均相对分子质量保持不变 d.该反应平衡常数保持不变e.NO和Cl2的体积比保持不变
(5)25℃时,向体积为2 L且带气压计的恒容密闭容器中通入0.08 mol NO和0.04 mol Cl2发生反应:2NO(g)+Cl2 (g) 2ClNO(g)△H。
2ClNO(g)△H。
①若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图甲曲线a所示,则 △H__ (填“>”“<”或“不确定”)0;若其他条件相同,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图甲曲线b所示,则改变的条件是______ 。
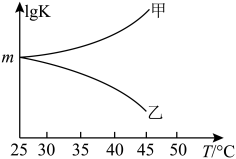
②图是甲、乙同学描绘上述反应平衡常数的对数值(lg K)与温度的变化关系,其中正确的曲线是____ (填“甲”或“乙”),m值为_____ 。
 2ClNO(g)。
2ClNO(g)。(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:① 2NO2(g)+NaCl(s)
 NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s)
NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g) 2ClNO(g) K3,则K1、K2、K3之间的关系为K3=
2ClNO(g) K3,则K1、K2、K3之间的关系为K3=(2)已知几种化学键的键能数据如下表:(亚硝酰氯的结构为Cl—N==O)
| 化学键 | N≡O | Cl-Cl | Cl-N | N==O |
| 键能/(kJ·mol-1) | 630 | 243 | a | 607 |
 2ClNO(g)的反应的 △H和a的关系为 △H =
2ClNO(g)的反应的 △H和a的关系为 △H = (3)300℃时,2NO(g)+Cl2 (g)
 2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:| 序号 | c(ClNO)/(mol·L-1) | v/(mol·L-1·s-l) |
| ① | 0. 30 | 3. 60×10-9 |
| ② | 0. 60 | 1. 44×10-8 |
| ③ | 0. 90 | 3. 24×10-8 |
(4)若向绝热恒容密闭容器中充入物质的量之比为2 : 1的NO和Cl2进行反应2NO(g)+Cl2(g)
 2ClNO(g),能判断反应已达到化学平衡状态的是
2ClNO(g),能判断反应已达到化学平衡状态的是a.容器中的压强不变 b.2v正(NO) = v逆(Cl2)c.气体的平均相对分子质量保持不变 d.该反应平衡常数保持不变e.NO和Cl2的体积比保持不变
(5)25℃时,向体积为2 L且带气压计的恒容密闭容器中通入0.08 mol NO和0.04 mol Cl2发生反应:2NO(g)+Cl2 (g)
 2ClNO(g)△H。
2ClNO(g)△H。①若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图甲曲线a所示,则 △H
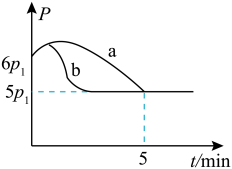
②图是甲、乙同学描绘上述反应平衡常数的对数值(lg K)与温度的变化关系,其中正确的曲线是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】2020年9月7日,我国在太原卫星发射中心用长征四号乙运载火箭,成功将高分十一号02星送入预定轨道。N2H4、NH3等均可用作火箭推进剂。请回答下列问题:
(1)某种运载火箭的推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢,一定量的N2H4(1)和H2O2(1)完全反应生成氮气和1mol气态水的过程中的能量变化如图所示。
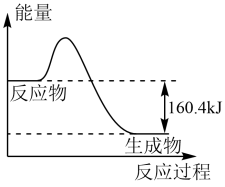
①该反应属于___ (填“吸热”或“放热”)反应。
②写出N2H4中含有的共价键类型:___ 。
③若该反应过程中N2H4中有8mol极性键发生断裂,则能量变化为___ kJ。
(2)已知下列数据:
则68g氨气完全燃烧生成氮气和气态水放出的热量为___ kJ。
(1)某种运载火箭的推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢,一定量的N2H4(1)和H2O2(1)完全反应生成氮气和1mol气态水的过程中的能量变化如图所示。

①该反应属于
②写出N2H4中含有的共价键类型:
③若该反应过程中N2H4中有8mol极性键发生断裂,则能量变化为
(2)已知下列数据:
| 物质 | NH3 | H2O | N2 | O2 |
| 断裂1mol化学键所需能量/kJ | 391 | 463 | 942 | 496 |
则68g氨气完全燃烧生成氮气和气态水放出的热量为
您最近一年使用:0次
【推荐1】乙醇是一种在生产、生活中应用广泛的产品,也是一种重要的工业原料。
(1)乙醇的获得:(工业上乙醇的获得方法很多)
①发酵法:淀粉或纤维素进行水解得到葡萄糖,葡萄糖在微生物或酶存在的条件下分解得到乙醇。
②合成法:
直接合成法:在有机磷或磷酸的催化下,乙烯与水反应得到乙醇,发生反应的化学方程式为_______ 。
间接合成法:首先乙烯与硫酸(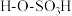 )反应得到硫酸氢乙酯(
)反应得到硫酸氢乙酯(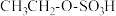 ),然后硫酸氢乙酯水解得到乙醇,写出第一步反应的化学方程式:
),然后硫酸氢乙酯水解得到乙醇,写出第一步反应的化学方程式:_______ ,该反应的反应类型为_______ 。
(2)乙醇还是制备乙酸乙酯的重要原料,请写出乙醇制备乙酸乙酯的化学方程式:_______ 。
(3)乙醇也是制作乙醇—氧气—KOH溶液的燃料电池(总反应为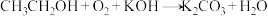 ,未配平),该燃料电池是一种将
,未配平),该燃料电池是一种将_______ (填“化学能转化成电能”或“电能转化成化学能”)的装置,正极通入的是_______ (填分子式),请写出负极的反应方程式_______ 。
(1)乙醇的获得:(工业上乙醇的获得方法很多)
①发酵法:淀粉或纤维素进行水解得到葡萄糖,葡萄糖在微生物或酶存在的条件下分解得到乙醇。
②合成法:
直接合成法:在有机磷或磷酸的催化下,乙烯与水反应得到乙醇,发生反应的化学方程式为
间接合成法:首先乙烯与硫酸(
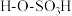 )反应得到硫酸氢乙酯(
)反应得到硫酸氢乙酯(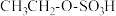 ),然后硫酸氢乙酯水解得到乙醇,写出第一步反应的化学方程式:
),然后硫酸氢乙酯水解得到乙醇,写出第一步反应的化学方程式:(2)乙醇还是制备乙酸乙酯的重要原料,请写出乙醇制备乙酸乙酯的化学方程式:
(3)乙醇也是制作乙醇—氧气—KOH溶液的燃料电池(总反应为
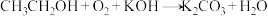 ,未配平),该燃料电池是一种将
,未配平),该燃料电池是一种将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表中的一部分。
根据A—J在周期表中的位置,用元素符号、化学式或反应式 回答下列问题:
(1)氧化性最强的单质是___ ,用一个化学反应证明H单质的氧化性强于G单质__________ 。
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为_________ 。
(3)B、C、G、H离子半径由大到小的顺序是_________ 。
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为______ 。若以氢氧化钾溶液为电解质溶液时,电池的总反应式为____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | A | |||||||
| 2 | E | F | G | H | J | |||
| 3 | B | C | D | I |
(1)氧化性最强的单质是
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为
(3)B、C、G、H离子半径由大到小的顺序是
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】电解原理和原电池原理是电化学的两个重要内容,引起了人们的研究兴趣。
(1)现有以下三种乙醇燃料电池(DEFC)。
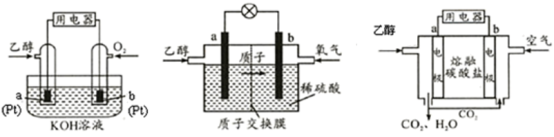
①碱性乙醇燃料电池中,电极a上发生的电极反应式为____ 。
②酸性乙醇燃料电池中,电极b上发生的电极反应式为___ 。
③熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电极b上发生的电极反应式为___ 。
(2)0.4mol CuSO4和0.4molNaCl溶于水,配成1L溶液,用惰性电极进行电解,当一个电极得到0.3molCu时,另一个电极上生成的气体在标准状况下的体积为___ L。
(3)新型绿色硝化剂N2O5可以N2O4为原料用电解法制备,实验装置如图所示,则电极B接直流电源的___ 极,电解池中生成N2O5的电极反应式为___ 。

(1)现有以下三种乙醇燃料电池(DEFC)。

①碱性乙醇燃料电池中,电极a上发生的电极反应式为
②酸性乙醇燃料电池中,电极b上发生的电极反应式为
③熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电极b上发生的电极反应式为
(2)0.4mol CuSO4和0.4molNaCl溶于水,配成1L溶液,用惰性电极进行电解,当一个电极得到0.3molCu时,另一个电极上生成的气体在标准状况下的体积为
(3)新型绿色硝化剂N2O5可以N2O4为原料用电解法制备,实验装置如图所示,则电极B接直流电源的

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】25℃时,部分物质的电离平衡常数如下表所示:
(1)25℃时,物质的量浓度为 的氨水中,
的氨水中,
___________  (列出算式即可)。
(列出算式即可)。
(2)25℃时,pH与体积均相同的醋酸溶液A与盐酸B分别与足量镁条充分反应,下列说法不正确 的是___________ (填字母序号)
a.开始反应时的速率:A<B b.放出等量氢气所需要的时间A=B
c.生成氢气的总体积:A>B
(3)常温下, 溶液中离子浓度由大到小的顺序是
溶液中离子浓度由大到小的顺序是___________ 。
(4)25℃时,物质的量浓度相等的 溶液和NaClO溶液pH大小关系是:
溶液和NaClO溶液pH大小关系是:
___________ NaClO(填“>”“<”或“=”),请结合题目有关信息说明原因___________ 。
(5)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是___________ 。
(6)用蒸馏水稀释 的醋酸,则下列各式表示的数值随水量的增加而增大的是_______。
的醋酸,则下列各式表示的数值随水量的增加而增大的是_______。
| 化学式 |  |  | HClO |  |
| 电离平衡常数 |  |  , , |  |  |
 的氨水中,
的氨水中,
 (列出算式即可)。
(列出算式即可)。(2)25℃时,pH与体积均相同的醋酸溶液A与盐酸B分别与足量镁条充分反应,下列说法
a.开始反应时的速率:A<B b.放出等量氢气所需要的时间A=B
c.生成氢气的总体积:A>B
(3)常温下,
 溶液中离子浓度由大到小的顺序是
溶液中离子浓度由大到小的顺序是(4)25℃时,物质的量浓度相等的
 溶液和NaClO溶液pH大小关系是:
溶液和NaClO溶液pH大小关系是:
(5)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是
(6)用蒸馏水稀释
 的醋酸,则下列各式表示的数值随水量的增加而增大的是_______。
的醋酸,则下列各式表示的数值随水量的增加而增大的是_______。A.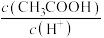 | B. | C.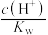 | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知CH3COOH是常见的弱酸,现有常温下0.lmol·L-1的CH3COOH溶液。
(1)取0.10molCH3COOH作导电性实验,测得其导电率随加入的水量变化如图所示。
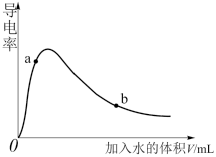
①n(H+):a___________ b(填“>”、“<”或“=”,下同)。
②c(CH3COO-):a___________ b。
③完全中和时消耗NaOH的物质的量:a___________ b。
(2)若向醋酸中加入氢氧化钠溶液,使醋酸恰好被中和,所得溶液的pH___________ 7(填“大于”“小于”或“等于”),用离子方程式表示其原因___________ ;中和后所得溶液中离子浓度由大到小的顺序为___________ 。
(3)25℃时,部分物质的电离平衡常数如表所示:
CH3COOH、H2CO3、HCN的酸性由强到弱的顺序为___________ 。
(1)取0.10molCH3COOH作导电性实验,测得其导电率随加入的水量变化如图所示。

①n(H+):a
②c(CH3COO-):a
③完全中和时消耗NaOH的物质的量:a
(2)若向醋酸中加入氢氧化钠溶液,使醋酸恰好被中和,所得溶液的pH
(3)25℃时,部分物质的电离平衡常数如表所示:
| CH3COOH | H2CO3 | HCN |
| 1.7×10-5 | Ka1=4.3×10-7、Ka2=5.6×10-11 | 4.9×10-10 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】乙酰水杨酸(用HA表示)商品名为阿司匹林,具有解热镇痛的作用,可以由水杨酸(用H2B表示)合成。
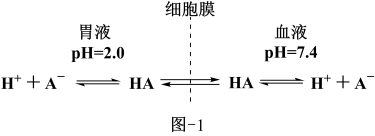
(1)阿司匹林的效率主要取决于其被血液吸收的程度。阿司匹林分子可以自由穿过细胞膜而离子不能,膜两侧HA的平衡浓度相等,示意图如图-1所示。
①胃液中的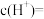
_______  。
。
②细胞膜两侧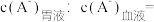
_______ 。
(2)室温下,水杨酸水溶液中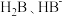 和
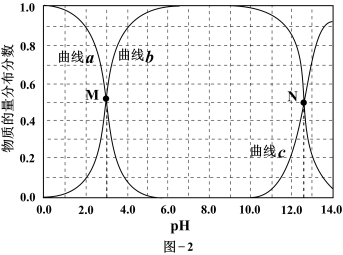
和 的物质的量分布分数随pH变化的曲线如图-2所示。
的物质的量分布分数随pH变化的曲线如图-2所示。
①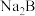 水解的离子方程式为
水解的离子方程式为_______ 。
②曲线c代表的微粒是_______ ;M点横坐标为3.0,则水杨酸的Ka1=_______ 。
③已知图中N点横坐标为12.7。当溶液pH=8.0时,溶液中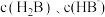 和
和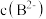 由大到小的顺序为
由大到小的顺序为_______ 。
(1)阿司匹林的效率主要取决于其被血液吸收的程度。阿司匹林分子可以自由穿过细胞膜而离子不能,膜两侧HA的平衡浓度相等,示意图如图-1所示。

①胃液中的
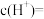
 。
。②细胞膜两侧
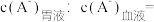
(2)室温下,水杨酸水溶液中
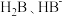 和
和 的物质的量分布分数随pH变化的曲线如图-2所示。
的物质的量分布分数随pH变化的曲线如图-2所示。
①
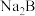 水解的离子方程式为
水解的离子方程式为②曲线c代表的微粒是
③已知图中N点横坐标为12.7。当溶液pH=8.0时,溶液中
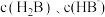 和
和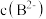 由大到小的顺序为
由大到小的顺序为
您最近一年使用:0次



