下列叙述不正确 的是
| A.纯锌与稀硫酸反应产生氢气的速率较慢;再加入少量固体CuSO4,加快速率 |
| B.在稀硫酸中加入铜粉,铜粉不溶解;再加入KNO3固体,铜粉溶解 |
| C.向FeCl3溶液中滴加氨水,产生红褐色沉淀;再加入NaHSO4溶液,沉淀消失 |
| D.将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2,产生沉淀 |
更新时间:2023-10-15 16:34:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】能正确表示下列变化的离子方程式是
| A.FeCl3溶液中加入少量Zn粉,溶液黄色褪去:2Fe3++3Zn=2Fe+3Zn2+ |
| B.四氧化三铁溶于稀硝酸:Fe3O4+8H+=2Fe3++Fe2++4H2O |
| C.用铁电极电解NaCl溶液的阳极反应:2Cl−−2e−=Cl2↑ |
D.SO2通入与溴水:SO2+Br2+2H2O=4H++2Br−+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】铁是人类较早使用的金属之一。据有关报道,目前已能冶炼出纯度高达99.999 9%的铁。以下是有关这种铁的叙述,其中不正确的是( )
| A.韧性比生铁好 | B.在冷的浓硫酸中钝化 |
| C.不能与盐酸反应 | D.在冷的浓硝酸中因钝化而被使用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室现有含硫酸和硝酸的混合溶液100mL,其中硫酸的浓度为2mol/L,硝酸的浓度为1mol/L。现向混合溶液中加入16g铜粉,充分反应后(假设只生成NO气体),最多可收集到标准状况下的气体的体积为
| A.448mL | B.896mL | C.1120mL | D.2240mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式能用来解释相应实验操作或现象,且操作和现象均描述正确的是
| 实验操作或现象 | 离子方程式 | |
| A | 用酸化的硝酸铁溶液腐蚀铜箔 | 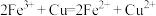 |
| B | 在稀硫酸中加入铜粉,铜粉不溶解,再加入 固体,铜粉溶解 固体,铜粉溶解 |  |
| C | 用浓氢氧化钠溶液反萃取法提取碘 | 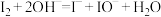 |
| D | 氧化亚铁溶于稀硝酸 | 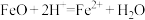 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】少量铁粉与100mL0.01mol·L-1的稀硫酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O ②加NaOH固体 ③滴入几滴浓硫酸 ④加CuO固体 ⑤加NaCl溶液 ⑥升高温度 ⑦改用10mL18.3mol·L-1的硫酸
①加H2O ②加NaOH固体 ③滴入几滴浓硫酸 ④加CuO固体 ⑤加NaCl溶液 ⑥升高温度 ⑦改用10mL18.3mol·L-1的硫酸
| A.①④⑦ | B.③⑥ | C.②④⑥ | D.③⑥⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】把在空气中久置的铝片5g投入到装有500mL0.5mol/L稀硫酸烧杯中,该铝片与稀硫酸反应产生的氢气的速率与反应的时间关系可用如图曲线表示,下列说法正确的是
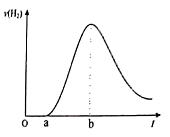

| A.Oa段表示没有反应发生 |
| B.ab段速率上升的主要原因是反应放热导致溶液温度升高 |
| C.b点表示产生的氢气总量最多 |
| D.b点以后速率下降的原因主要是温度降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作和现象及解释均正确的是
| 选项 | 操作和现象 | 解释 |
| A | Cu和稀硝酸反应制取NO时,改用69%的浓硝酸,产生NO的速率加快 | 反应物浓度增大,反应速率加快 |
| B | 向鸡蛋清中加入几滴醋酸铅溶液,产生白色沉淀,加水,沉淀溶解 | 蛋白质的变性可以逆转 |
| C | 锌与稀硫酸反应,滴入少量硫酸铜溶液,生成氢气的速率加快 | 锌置换出铜,形成原电池,反应速率加快 |
| D | 在试管中加入0.5g淀粉和   溶液,加热,待溶液冷却后向其中滴加少量银氨溶液,加热未观察到光亮的银镜生成 溶液,加热,待溶液冷却后向其中滴加少量银氨溶液,加热未观察到光亮的银镜生成 | 淀粉未发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列操作或结论正确的是
| A.测定中和热时,每次实验均应测量两次温度:起始温度和反应后最高温度 |
| B.实验室制氢气使用粗锌比使用纯锌反应速率快 |
| C.凹液面均与“0”刻度线相切,25mL滴定管液体体积为50mL滴定管的一半 |
| D.为使实验现象明显,中和滴定时加入5mL酚酞或甲基橙 |
您最近一年使用:0次

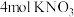 和
和 ,向其中加入
,向其中加入 ,充分反应(已知
,充分反应(已知 被还原为NO),最终溶液体积为
被还原为NO),最终溶液体积为 ,下列说法正确的是
,下列说法正确的是 、
、
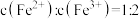
 (标准状况下)
(标准状况下)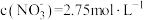
 反应,当Cu反应完全时,共收集到气体
反应,当Cu反应完全时,共收集到气体 和NO(标准状况,不考虑
和NO(标准状况,不考虑 转化为
转化为 ),则反应中消耗
),则反应中消耗 2NO(g),下列措施不能改变化学反应速率的是
2NO(g),下列措施不能改变化学反应速率的是

