如图是一个实验室制取氯气并以氯气为原料进行特定反应的装置:
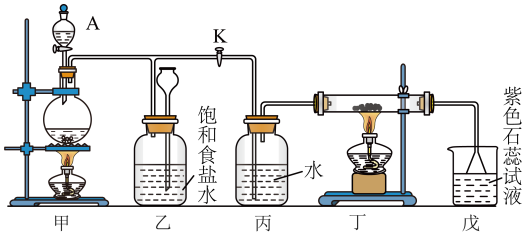
(1)仪器A的名称为___________ 。
(2)甲是氯气发生装置,其中反应的离子方程式为___________ 。
(3)实验开始时,先点燃甲处的酒精灯,打开旋塞K,让 充满整个装置,再点燃丁处酒精灯,连接上戊装置。
充满整个装置,再点燃丁处酒精灯,连接上戊装置。 通过丙瓶后再进入丁,丁装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为
通过丙瓶后再进入丁,丁装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为 和
和 。试写出丁中反应的化学方程式:
。试写出丁中反应的化学方程式:___________ 。装置丙的主要作用是___________ 。
(4)若将装置戊烧杯中溶液改为澄清石灰水,反应过程现象为___________ 。
A.无明显变化 B.有白色沉淀生成 C.先生成白色沉淀,而后白色沉淀消失
(5)丁处反应完毕后,关闭旋塞 ,移去酒精灯。但由于余热的作用,甲处仍有
,移去酒精灯。但由于余热的作用,甲处仍有 产生,此时乙中的现象是
产生,此时乙中的现象是___________ ,乙的作用是___________ 。

(1)仪器A的名称为
(2)甲是氯气发生装置,其中反应的离子方程式为
(3)实验开始时,先点燃甲处的酒精灯,打开旋塞K,让
 充满整个装置,再点燃丁处酒精灯,连接上戊装置。
充满整个装置,再点燃丁处酒精灯,连接上戊装置。 通过丙瓶后再进入丁,丁装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为
通过丙瓶后再进入丁,丁装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为 和
和 。试写出丁中反应的化学方程式:
。试写出丁中反应的化学方程式:(4)若将装置戊烧杯中溶液改为澄清石灰水,反应过程现象为
A.无明显变化 B.有白色沉淀生成 C.先生成白色沉淀,而后白色沉淀消失
(5)丁处反应完毕后,关闭旋塞
 ,移去酒精灯。但由于余热的作用,甲处仍有
,移去酒精灯。但由于余热的作用,甲处仍有 产生,此时乙中的现象是
产生,此时乙中的现象是
更新时间:2023-09-17 16:04:08
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
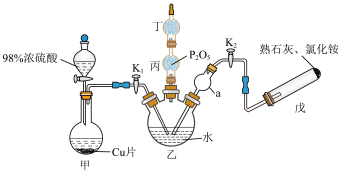
【推荐1】I.亚硫酸氢铵(NH4HSO3)可用作防腐剂、还原剂,也用于制造二氧化硫、保险粉等,某化学兴趣小组设计如图装置(加热和夹持装置已省略)制备亚硫酸氢铵,请回答下列问题:
(1)盛装浓硫酸的仪器名称为___________ ;实验开始时,先关闭K1,打开K2,先通氨气使溶液呈碱性的目的:___________ ;戊装置的试管内反应的化学方程式为___________ ;乙中仪器a的作用是___________ 。
(2)一段时间后,关闭K2,打开K1,甲装置圆底烧瓶内发生反应的化学方程式为___________ ;丙装置的作用是___________ ;丁装置用于吸收多余的SO2,则丁装置中的试剂为___________ 。
(3)设计实验检验亚硫酸氢铵中阳离子,写出操作、现象及相应的结论:___________ 。
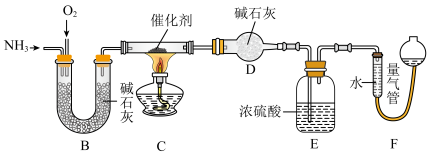
II.另一化学兴趣小组同学利用下图装置探究氨的催化氧化,并测定氯化铵的纯度。取10.0g氯化铵样品(杂质不参加反应)与足量消石灰反应,将产生的气体全部通入下图装置,待完全反应后,E中质量增加了1.02g,通过测量的数据进行计算得出C中反应生成的水为0.18 mol。___________ 。
(5)计算氯化铵样品的纯度___________ %(保留小数点后一位)。
(1)盛装浓硫酸的仪器名称为
(2)一段时间后,关闭K2,打开K1,甲装置圆底烧瓶内发生反应的化学方程式为
(3)设计实验检验亚硫酸氢铵中阳离子,写出操作、现象及相应的结论:
II.另一化学兴趣小组同学利用下图装置探究氨的催化氧化,并测定氯化铵的纯度。取10.0g氯化铵样品(杂质不参加反应)与足量消石灰反应,将产生的气体全部通入下图装置,待完全反应后,E中质量增加了1.02g,通过测量的数据进行计算得出C中反应生成的水为0.18 mol。
(5)计算氯化铵样品的纯度
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是一些中学常见的物质之间的转化关系(其中部分反应产物省略),其中A和B常温下都是气体,且水溶液都有漂白性;I是一种金属单质;F、M、N均为不溶于水的白色沉淀,其中M和N不溶于稀硝酸,C和D是两种常见的强酸。请回答下列问题:

(1)写出实验室制备A的离子方程式___________ 。
(2)写反应②的离子方程式___________ 。
(3)写出将A通入石灰乳的化学方程式___________ 。
(4)在①→⑥中,属于氧化还原反应的有___________ (填编号),将NaOH溶液加入到E中的现象为___________ 。
(5)写出分别将A、B通入石蕊试液中的现象:A___________ B___________ 。

(1)写出实验室制备A的离子方程式
(2)写反应②的离子方程式
(3)写出将A通入石灰乳的化学方程式
(4)在①→⑥中,属于氧化还原反应的有
(5)写出分别将A、B通入石蕊试液中的现象:A
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氯及其化合物在工业生产和人类生活中应用广泛。
(1)实验室利用将氯气通入碱液制备NaClO和 ,装置如图所示:
,装置如图所示:

①盛放浓盐酸的仪器名称是___________ ,A中发生反应的化学方程式为___________ 。
②用8.7g 与足量浓盐酸充分反应,生成
与足量浓盐酸充分反应,生成 的质量为
的质量为___________ 。
(2)C中试管内发生反应反应的离子方程式为:___________ 。
(3)实验室可以将氯气通入冷而稀的氢氧化钠溶液获得“84消毒液”,制备“84消毒液”的离子方程式___________ 。
(4)某同学设计实验探究84消毒液的漂白性。
I.在2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
II.在2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
III.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。
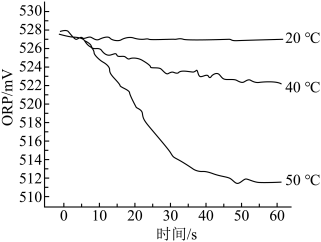
已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验I、II现象不同的原因是为___________ 。
②实验III中,随时间的变化ORP值不同的原因可能是___________ 。
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。已知某品牌84消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释为8%的溶液,需加水的质量为___________ g。
(1)实验室利用将氯气通入碱液制备NaClO和
 ,装置如图所示:
,装置如图所示:
①盛放浓盐酸的仪器名称是
②用8.7g
 与足量浓盐酸充分反应,生成
与足量浓盐酸充分反应,生成 的质量为
的质量为(2)C中试管内发生反应反应的离子方程式为:
(3)实验室可以将氯气通入冷而稀的氢氧化钠溶液获得“84消毒液”,制备“84消毒液”的离子方程式
(4)某同学设计实验探究84消毒液的漂白性。
I.在2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
II.在2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
III.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。

已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验I、II现象不同的原因是为
②实验III中,随时间的变化ORP值不同的原因可能是
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。已知某品牌84消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释为8%的溶液,需加水的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。

请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是________ ,其中发生反应的化学方程式为_____ 。
(2)实验过程中,装置B、C中发生的现象分别是_____ 、 ____ ,这些现象分别说明SO2具有的性质是____ 和____ 。
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象_________ 。
(4)尾气可采用________ 溶液吸收。(写化学式)

请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是
(2)实验过程中,装置B、C中发生的现象分别是
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象
(4)尾气可采用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】探究在常温下氢氧化钡晶体与氯化铵晶体反应过程中能量变化的实验方案和实验步骤如图所示,根据下面的实验方案和步骤回答下列问题:

下表是某学生根据上述实验方案和步骤列表整理的实验事实和结论:
(1)请你根据实验现象得出相应的实验结论填入上表中。_________________ 。
(2)用化学方程式表示上述反应为_______________________ 。

下表是某学生根据上述实验方案和步骤列表整理的实验事实和结论:
| 实验步骤 | 实验现象 | 得出结论 |
| 将晶体混合后立即用玻璃棒快速搅拌混合物 | 有刺激性气味的气体产生,该气体能使湿润的紫色石蕊试纸变蓝 | |
| 用手触摸烧杯下部 | 感觉烧杯变凉 | |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片(或小木板)粘到了烧杯底部 | |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上一会儿再拿起 | 玻璃片脱离上面烧杯底部 | |
| 反应完后移走烧杯上的多孔塑料Q片,观察反应物 | 混合物成糊状 |
(2)用化学方程式表示上述反应为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】某实验小组用工业上废渣 主要成分Cu2S和Fe2O3制取纯铜和绿矾(FeSO4∙7H2O)产品,设计流程如下:
主要成分Cu2S和Fe2O3制取纯铜和绿矾(FeSO4∙7H2O)产品,设计流程如下:

(1)在实验室中,欲用98%的浓硫酸(密度为1.84g/mL)配制500mL1.0mol/L的硫酸,需要的仪器除量筒、烧杯、玻璃棒、胶头滴管,还有_______ 。
(2)该小组同学设计如下装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素。
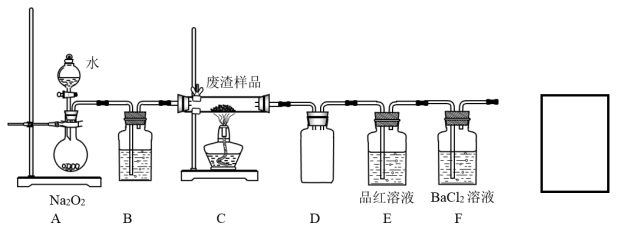
①A中盛有Na2O2的仪器名称为_______ ;装置A中反应的化学方程式为_______
②E装置中品红褪色,F装置盛放的BaCl2溶液中出现白色沉淀,写出生成白色沉淀的离子方程式为_______
③反应装置不完善,为避免空气污染,在方框中补全装置图,并注明试剂名称_______ 。
(3)从下列图中选择合适的装置,写出步骤⑤中进行的操作顺序_______ (填序号)

(4)步骤⑥中由粗铜得到纯铜的方法为_______ (填写名称)
(5)为测定产品中绿矾的质量分数,称取30.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O,实验所得数据如下表所示:
①第1组实验数据出现异常,造成这种异常的原因可能是_______ (填代号)
a.锥形瓶洗净后未干燥
b.滴定终点时俯视读数
c.滴定前尖嘴有气泡,滴定后气泡消失
②根据表中数据,计算所得产品中绿矾的质量分数为_______ (保留3位有效数字)
 主要成分Cu2S和Fe2O3制取纯铜和绿矾(FeSO4∙7H2O)产品,设计流程如下:
主要成分Cu2S和Fe2O3制取纯铜和绿矾(FeSO4∙7H2O)产品,设计流程如下:
(1)在实验室中,欲用98%的浓硫酸(密度为1.84g/mL)配制500mL1.0mol/L的硫酸,需要的仪器除量筒、烧杯、玻璃棒、胶头滴管,还有
(2)该小组同学设计如下装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素。

①A中盛有Na2O2的仪器名称为
②E装置中品红褪色,F装置盛放的BaCl2溶液中出现白色沉淀,写出生成白色沉淀的离子方程式为
③反应装置不完善,为避免空气污染,在方框中补全装置图,并注明试剂名称
(3)从下列图中选择合适的装置,写出步骤⑤中进行的操作顺序

(4)步骤⑥中由粗铜得到纯铜的方法为
(5)为测定产品中绿矾的质量分数,称取30.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O,实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
 溶液体积 溶液体积 | 19.10 | 20.02 | 19.98 | 20.00 |
①第1组实验数据出现异常,造成这种异常的原因可能是
a.锥形瓶洗净后未干燥
b.滴定终点时俯视读数
c.滴定前尖嘴有气泡,滴定后气泡消失
②根据表中数据,计算所得产品中绿矾的质量分数为
您最近一年使用:0次



