氮可以形成多种离子,如N3-, ,
,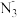 ,
, ,
, ,
,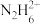 等,已知
等,已知 与
与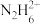 是由中性分子结合质子形成的,类似于
是由中性分子结合质子形成的,类似于 ,因此有类似于
,因此有类似于  的性质。
的性质。
(1)写出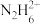 在碱性溶液中反应的离子方程式
在碱性溶液中反应的离子方程式_________________________________ 。
(2) 的电子式为
的电子式为_________________________ 。
(3)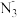 有
有_________________ 个电子。
(4)写出二种由多个原子组成的含有与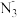 电子数相同的物质的化学式
电子数相同的物质的化学式___________ 。
(5)等电子数的微粒往往具有相似的结构,试预测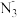 的构型
的构型____________________ 。
(6)据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是____________ 。
 ,
,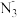 ,
, ,
, ,
,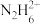 等,已知
等,已知 与
与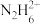 是由中性分子结合质子形成的,类似于
是由中性分子结合质子形成的,类似于 ,因此有类似于
,因此有类似于  的性质。
的性质。(1)写出
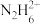 在碱性溶液中反应的离子方程式
在碱性溶液中反应的离子方程式(2)
 的电子式为
的电子式为(3)
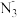 有
有(4)写出二种由多个原子组成的含有与
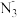 电子数相同的物质的化学式
电子数相同的物质的化学式(5)等电子数的微粒往往具有相似的结构,试预测
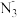 的构型
的构型(6)据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是
11-12高二上·四川雅安·期中 查看更多[7]
河南省开封市兰考县第一高级中学2018-2019学年高二下学期3月月考化学试题人教版2017-2018学年高一化学必修1:2.2 离子反应 同步测试(已下线)2011-2012学年四川省雅安中学高二上学期期中考试化学试卷2015-2016学年山西省运城市康杰中学高二上学期测试4化学试卷2014-2015学年湖北省部分重点高中高二下期末考试化学试卷(已下线)2013-2014学年湖北省孝感市七校联考高二下学期期中考试化学试卷2016-2017学年四川省成都市石室佳兴外国语学校高二下学期第一次月考化学试卷
更新时间:2016-12-09 05:52:14
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增加。回答下列问题:
(l)2016年IUPAC确认了四种新元素,其中一种为Mc,中文为“镆”。元素Mc可由反应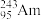 +
+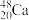 →288Mc+3
→288Mc+3 得到。该元素的质子数为
得到。该元素的质子数为_______ ,287Mc与288Mc互为________ 。
(2)Mc位于元素周期表中第VA族,同族元素N的一种氢化物为NH2NH2,写出该化合物分子的电子式__________ ,该分子内存在的共价键类型有_________ 。
(3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的分子式为_________ ,该氧化物对应的水化物为H3PO3,已知该酸与足量NaOH溶液反应所得产物化学式为Na2HPO3,则Na2HPO3是________ (填“正盐”或“酸式盐”)。
(l)2016年IUPAC确认了四种新元素,其中一种为Mc,中文为“镆”。元素Mc可由反应
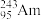 +
+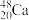 →288Mc+3
→288Mc+3 得到。该元素的质子数为
得到。该元素的质子数为(2)Mc位于元素周期表中第VA族,同族元素N的一种氢化物为NH2NH2,写出该化合物分子的电子式
(3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的分子式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】
(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
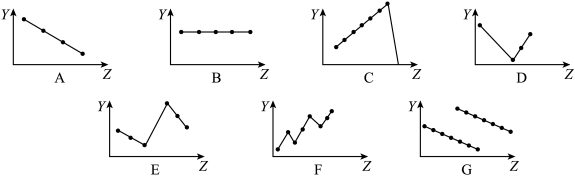
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
①第ⅡA族元素的最外层电子数_____________ 。
②第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径_______ 。
③第二、三周期主族元素随原子序数递增原子半径的变化___________ 。
(2)已知某单核粒子的结构示意图为:
①当x-y=10时,该粒子为______ (填“原子”、“阳离子”或“阴离子”)。
②当y=8时,若该微粒的氧化性很弱,得一个电子后变为原子,该微粒的符号是_______ 。
(3)已知A、B、C、D是中学化学中常见的四种10电子微粒,它们之间存在如图中转化关系。
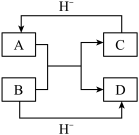
请写出:A的化学式_______ (写一种);D的化学式________ 。
(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
①第ⅡA族元素的最外层电子数
②第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径
③第二、三周期主族元素随原子序数递增原子半径的变化
(2)已知某单核粒子的结构示意图为:

①当x-y=10时,该粒子为
②当y=8时,若该微粒的氧化性很弱,得一个电子后变为原子,该微粒的符号是
(3)已知A、B、C、D是中学化学中常见的四种10电子微粒,它们之间存在如图中转化关系。

请写出:A的化学式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】有①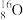 、
、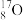 、
、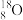 ②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:
②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:
(1)分别写出氢元素三种同位素的名称:______ 、_______ 、______ 。写出用做制造氢弹原料的同位素原子:______ (填原子符号)。
(2)互为同位素的是________ (填编号,下同)。
(3)互为同素异形体的是_______ 。
(4)由①和④中微粒能结合成三原子化合物,写出这些化合物的相对分子质量的最大值和最小值是_____________ 。
(5)质量相同的H216O 和D216O 所含质子数之比为_______ ,中子数之比为_______ 。
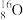 、
、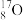 、
、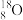 ②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:
②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:(1)分别写出氢元素三种同位素的名称:
(2)互为同位素的是
(3)互为同素异形体的是
(4)由①和④中微粒能结合成三原子化合物,写出这些化合物的相对分子质量的最大值和最小值是
(5)质量相同的H216O 和D216O 所含质子数之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】有①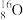 、
、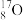 、
、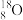 ②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:
②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:
(1)分别写出氢元素三种同位素的名称:______ 、_______ 、______ 。写出用做制造氢弹原料的同位素原子:______ (填原子符号)。
(2)互为同位素的是________ (填编号,下同)。
(3)互为同素异形体的是_______ 。
(4)由①和④中微粒能结合成三原子化合物,写出这些化合物的相对分子质量的最大值和最小值是_____________ 。
(5)质量相同的H216O 和D216O 所含质子数之比为_______ ,中子数之比为_______ 。
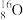 、
、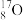 、
、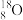 ②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:
②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:(1)分别写出氢元素三种同位素的名称:
(2)互为同位素的是
(3)互为同素异形体的是
(4)由①和④中微粒能结合成三原子化合物,写出这些化合物的相对分子质量的最大值和最小值是
(5)质量相同的H216O 和D216O 所含质子数之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】铁矿石是重要的金属矿物资源,我省攀西地区有丰富的钒钛磁铁矿。
(1)在自然界中,钛(Ti)、钒(V)存在多种核素,其中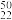 Ti与
Ti与 V相同的是
V相同的是______ 。
A.质子数 B.中子数 C.质量数 D.核外电子数
(2)通过下列方法可以测定磁铁矿中铁的含量:将磁铁矿溶于较浓的盐酸中,用SnCl2将Fe3+还原为Fe2+,最后用已知浓度的K2Cr2O7溶液滴定生成的Fe2+。
①磁铁矿中Fe3O4溶于盐酸时发生反应的离子方程式为______________ 。
② 配平K2Cr2O7溶液滴定FeCl2溶液时发生反应的离子方程式:
Fe2++Cr2O +H+=Fe3++Cr3++H2O
+H+=Fe3++Cr3++H2O
_______________________________________________
③现有磁铁矿样品0.500 g,经上述各步反应后,共用去0.0200 mol/L的K2Cr2O7溶液24.5 mL。计算该样品中铁的质量分数____ (计算结果保留1位小数)。
(1)在自然界中,钛(Ti)、钒(V)存在多种核素,其中
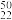 Ti与
Ti与 V相同的是
V相同的是A.质子数 B.中子数 C.质量数 D.核外电子数
(2)通过下列方法可以测定磁铁矿中铁的含量:将磁铁矿溶于较浓的盐酸中,用SnCl2将Fe3+还原为Fe2+,最后用已知浓度的K2Cr2O7溶液滴定生成的Fe2+。
①磁铁矿中Fe3O4溶于盐酸时发生反应的离子方程式为
② 配平K2Cr2O7溶液滴定FeCl2溶液时发生反应的离子方程式:
Fe2++Cr2O
 +H+=Fe3++Cr3++H2O
+H+=Fe3++Cr3++H2O③现有磁铁矿样品0.500 g,经上述各步反应后,共用去0.0200 mol/L的K2Cr2O7溶液24.5 mL。计算该样品中铁的质量分数
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】按要求填空:
(1)原子核外有3个电子层,其价电子数为7的元素其最高价氧化物对应水化物化学式________ ,其单质与NaOH反应的化学方程式为____________________________________________________ 。
(2)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子序数由大到小的顺序是___________________ ,原子半径由大到小的顺序是__________________ 。
(3) A+、Bˉ、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ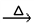 C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:_____________ ,______________ ;比较C和D的稳定性的强弱:_____________________ (用化学式表示)。
(4)①NH4NO3 ②NaF ③CO2 ④K2O2 ⑤NaOH ⑥CH4
以上只含有极性键的是_______ (填序号),既有离子键又有非极性键的是______ (填序号);既有离子键又有极性键的是______ (填序号)。
(5)下列原子: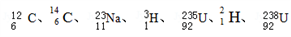 中共有
中共有____ 种元素,__ 种核素。
(6)写出下列物质或微粒的电子式:
①CO2__________ ②KCl_____________ ③H2O2_______________ ④N2_____________ ;
⑤用电子式表示MgCl2的形成过程_________________________________________________ 。
(1)原子核外有3个电子层,其价电子数为7的元素其最高价氧化物对应水化物化学式
(2)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子序数由大到小的顺序是
(3) A+、Bˉ、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ
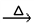 C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:(4)①NH4NO3 ②NaF ③CO2 ④K2O2 ⑤NaOH ⑥CH4
以上只含有极性键的是
(5)下列原子:
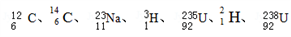 中共有
中共有(6)写出下列物质或微粒的电子式:
①CO2
⑤用电子式表示MgCl2的形成过程
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】
(1)菠菜营养丰富,素有“蔬菜之王”之称,在营养价值上是一种高效的补铁剂。某化学小组欲设计实验方案,探究菠菜中是否存在铁元素与草酸及可溶性草酸盐。甲同学查阅资料得知:草酸又名乙二酸,化学式为H2C2O4,是一种二元有机弱酸,具有较强的还原性。甲同学依据上述信息推测,菠菜中铁元素呈____ 价,其理由是____________________ 。甲同学同时设计实验方案,验证其推测是否正确。请简述实验方案_______________________________________ 。
(2)乙炔是有机合成工业的一种原料。工业上曾用 与水反应生成乙炔。
与水反应生成乙炔。
① 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为_______________ ;1mol 中含有的
中含有的 键数目为
键数目为________ 。
②乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是___________________ ;分子中处于同一直线上的原子数目最多为_____ 。
(1)菠菜营养丰富,素有“蔬菜之王”之称,在营养价值上是一种高效的补铁剂。某化学小组欲设计实验方案,探究菠菜中是否存在铁元素与草酸及可溶性草酸盐。甲同学查阅资料得知:草酸又名乙二酸,化学式为H2C2O4,是一种二元有机弱酸,具有较强的还原性。甲同学依据上述信息推测,菠菜中铁元素呈
(2)乙炔是有机合成工业的一种原料。工业上曾用
 与水反应生成乙炔。
与水反应生成乙炔。①
 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为 中含有的
中含有的 键数目为
键数目为②乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】【化学—物质结构与性质】
电石(CaC2)发生如下反应合成尿素[CO(NH2)2],可进一步合成三聚氰胺。

(1)CO(NH2)2分子中含有σ键的个数为______ 。CaCN2中阴离子为CN22-,与CN22-离子互为等电子体的分子的化学式为_______ ,可推知CN22-的空间构型为_________ 。
(2)三聚氰胺在动物体内可转化为三聚氰酸( ),三聚氰酸分子中N原子采取
),三聚氰酸分子中N原子采取______ 杂化。三聚氰胺与三聚氰酸的分子相互之间通过________ 结合,在肾脏内易形成结石。
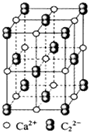
(3)下图是电石的晶胞示意图,则一个晶胞中含有___ 个Ca2+离子,研究表明,C22-的存在使晶胞呈长方体,该晶胞中一个Ca2+周围距离相等且最近的C22-有___ 个。
电石(CaC2)发生如下反应合成尿素[CO(NH2)2],可进一步合成三聚氰胺。

(1)CO(NH2)2分子中含有σ键的个数为
(2)三聚氰胺在动物体内可转化为三聚氰酸(
 ),三聚氰酸分子中N原子采取
),三聚氰酸分子中N原子采取(3)下图是电石的晶胞示意图,则一个晶胞中含有

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】铜及其化合物在生产生活中有着广泛的用途。
(1)基态铜原子的核外电子排布式为_____________ 。其晶体的堆积方式为__________________ ,
其中铜原子的配位数为_____________ 。
(2)向硫酸铜溶液中滴氨水,首先形成蓝色沉淀;继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液;继续向溶液中加入乙醇,会析出深蓝色晶体[Cu(NH3)4SO4·H2O]。
①氨水中各元素原子的电负性由大到小的顺序为_______________ (用元素符号表示)。
②NH3中N原子的杂化轨道类型为_____________ ,与其互为等电子体的阳离子为__________ 。
③向蓝色沉淀中继续滴加氨水,沉淀溶解是因为生成了四氨合铜络离子,四氨合铜络离子的结构式
为____________ ;加入乙醇后析出晶体的原因为________________ 。
(3) CuCl2和CuCl是铜的两种常见的氯化物。
①下图表示的是________________ (填“CuCl2”或“CuCl”)的晶胞。
②原子坐标参数,表示晶胞内部各原子的相对位置,上图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为____________ 。
③上图晶胞中C、D两原子核间距为298 pm,阿伏伽德罗常数为NA,则该晶体密度为______ g·cm-3(列出计算式即可)。
(1)基态铜原子的核外电子排布式为
其中铜原子的配位数为
(2)向硫酸铜溶液中滴氨水,首先形成蓝色沉淀;继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液;继续向溶液中加入乙醇,会析出深蓝色晶体[Cu(NH3)4SO4·H2O]。
①氨水中各元素原子的电负性由大到小的顺序为
②NH3中N原子的杂化轨道类型为
③向蓝色沉淀中继续滴加氨水,沉淀溶解是因为生成了四氨合铜络离子,四氨合铜络离子的结构式
为
(3) CuCl2和CuCl是铜的两种常见的氯化物。
①下图表示的是
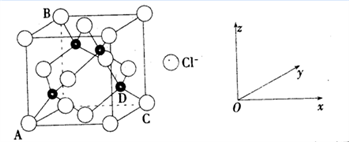
②原子坐标参数,表示晶胞内部各原子的相对位置,上图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为
③上图晶胞中C、D两原子核间距为298 pm,阿伏伽德罗常数为NA,则该晶体密度为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】完成表中的空白:
| 原子总数 | 粒子 | 中心原子孤电子对数 | 中心原子的杂化轨道类型 | 空间结构 |
| 3 |  | |||
 | ||||
 | ||||
| HCN | ||||
| 4 |  | |||
 | ||||
 | ||||
| 5 |  | |||
 |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】在含砷废水中,砷元素多以+3和+5价的形式存在。工业上常利用 磁性纳米盘等吸附剂处理含砷废水,实现水体达标排放。
磁性纳米盘等吸附剂处理含砷废水,实现水体达标排放。
(1) 水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图1所示。
水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图1所示。
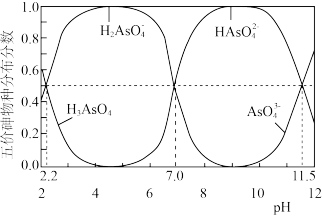
图1
① 分子中
分子中 的空间构型为
的空间构型为_______ ,将NaOH溶液滴入 溶液中,初始反应的离子方程式为
溶液中,初始反应的离子方程式为_______ 。
② 第一步电离方程式
第一步电离方程式 ,其电离常数为
,其电离常数为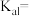
_______ 。
(2)① 磁性纳米盘制备:在一定条件,将
磁性纳米盘制备:在一定条件,将 的
的 和PVP溶于水中并加热,滴加过量NaOH溶液生成
和PVP溶于水中并加热,滴加过量NaOH溶液生成 ,再加入amL
,再加入amL 的
的 溶液。充分反应后(
溶液。充分反应后(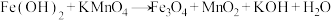 ,未配平),可制得
,未配平),可制得 磁性纳米盘。制备过程中需严格控制
磁性纳米盘。制备过程中需严格控制 溶液的用量,则a=
溶液的用量,则a=_______ 。
② 磁性纳米盘对酸性水中三价砷的去除能力远比五价砷的弱,可利用其中的
磁性纳米盘对酸性水中三价砷的去除能力远比五价砷的弱,可利用其中的 将酸性废水中的
将酸性废水中的 氧化成
氧化成 除去,反应过程中生成
除去,反应过程中生成 ,则反应的离子方程式为
,则反应的离子方程式为_______ 。
③ 磁性纳米盘处理含砷废水时,水中
磁性纳米盘处理含砷废水时,水中 、
、 、
、 和
和 对
对 的吸附率的影响如图2。
的吸附率的影响如图2。 对
对 吸附去除几乎没有影响,
吸附去除几乎没有影响, 对
对 吸附去除影响较大。请解释
吸附去除影响较大。请解释 抑制
抑制 吸附去除的可能原因
吸附去除的可能原因_______ 。

 磁性纳米盘等吸附剂处理含砷废水,实现水体达标排放。
磁性纳米盘等吸附剂处理含砷废水,实现水体达标排放。(1)
 水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图1所示。
水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图1所示。
图1
①
 分子中
分子中 的空间构型为
的空间构型为 溶液中,初始反应的离子方程式为
溶液中,初始反应的离子方程式为②
 第一步电离方程式
第一步电离方程式 ,其电离常数为
,其电离常数为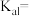
(2)①
 磁性纳米盘制备:在一定条件,将
磁性纳米盘制备:在一定条件,将 的
的 和PVP溶于水中并加热,滴加过量NaOH溶液生成
和PVP溶于水中并加热,滴加过量NaOH溶液生成 ,再加入amL
,再加入amL 的
的 溶液。充分反应后(
溶液。充分反应后(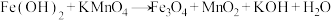 ,未配平),可制得
,未配平),可制得 磁性纳米盘。制备过程中需严格控制
磁性纳米盘。制备过程中需严格控制 溶液的用量,则a=
溶液的用量,则a=②
 磁性纳米盘对酸性水中三价砷的去除能力远比五价砷的弱,可利用其中的
磁性纳米盘对酸性水中三价砷的去除能力远比五价砷的弱,可利用其中的 将酸性废水中的
将酸性废水中的 氧化成
氧化成 除去,反应过程中生成
除去,反应过程中生成 ,则反应的离子方程式为
,则反应的离子方程式为③
 磁性纳米盘处理含砷废水时,水中
磁性纳米盘处理含砷废水时,水中 、
、 、
、 和
和 对
对 的吸附率的影响如图2。
的吸附率的影响如图2。 对
对 吸附去除几乎没有影响,
吸附去除几乎没有影响, 对
对 吸附去除影响较大。请解释
吸附去除影响较大。请解释 抑制
抑制 吸附去除的可能原因
吸附去除的可能原因
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】回答下列问题:
(1)原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为______ 。
(2)某同学画的基态Be原子电子排布图 ,分析其违背了什么原理:
,分析其违背了什么原理:______ 。
(3)橄榄石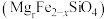 中各元素电负性由大到小顺序为:
中各元素电负性由大到小顺序为:______ 。
(4) 的沸点为
的沸点为 的沸点为
的沸点为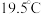 ,试从氢键角度解释这一现象:
,试从氢键角度解释这一现象:______ 。
(5)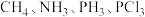 键角由大到小的顺序为:
键角由大到小的顺序为:______ 。
(6)碱金属熔点如下表
试用金属键相关理论解释该递变现象:______ 。
(7)往 溶液中逐滴加入氨水,直到生成的沉淀恰好溶解,得到深蓝色溶液,再加入乙醇后,析出深蓝色晶体。加乙醇的作用是
溶液中逐滴加入氨水,直到生成的沉淀恰好溶解,得到深蓝色溶液,再加入乙醇后,析出深蓝色晶体。加乙醇的作用是______ 。
(1)原子中电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为(2)某同学画的基态Be原子电子排布图
 ,分析其违背了什么原理:
,分析其违背了什么原理:(3)橄榄石
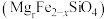 中各元素电负性由大到小顺序为:
中各元素电负性由大到小顺序为:(4)
 的沸点为
的沸点为 的沸点为
的沸点为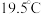 ,试从氢键角度解释这一现象:
,试从氢键角度解释这一现象:(5)
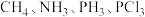 键角由大到小的顺序为:
键角由大到小的顺序为:(6)碱金属熔点如下表
| 碱金属 |  |  |  |  |  |
| 熔点/℃ | 180.5 | 97.8 | 63.6 | 38.9 | 28.4 |
(7)往
 溶液中逐滴加入氨水,直到生成的沉淀恰好溶解,得到深蓝色溶液,再加入乙醇后,析出深蓝色晶体。加乙醇的作用是
溶液中逐滴加入氨水,直到生成的沉淀恰好溶解,得到深蓝色溶液,再加入乙醇后,析出深蓝色晶体。加乙醇的作用是
您最近一年使用:0次



