Ⅰ.铁的化合物在实际中应用广泛,如氯化铁可用于五金蚀刻、污水处理及作催化剂、凝聚剂等,Na2FeO4可用作净水剂等。
(1)氯化铁溶液用于五金蚀刻时的反应产物是氯化亚铁,反应后再通入氯气,又可将氯化亚铁转化为氯化铁,则通入氯气后反应的离子方程式为_________________ 。
(2)氯化铁常用于净水,是因为铁离子转化为Fe(OH)3胶体,使水中悬浮物聚沉,Fe(OH)3胶体分散质微粒直径的范围是____________ ,实验室利用饱和氯化铁溶液制备Fe(OH)3胶体的离子方程式为:_________________ 。
(3)氯化铁还可以充当双氧水分解的催化剂,2个H2O2分子发生分解时反应中转移的电子数是__________ 。
(4)Na2FeO4是一种新型的净水消毒剂,可以通过下列反应制得:Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O(未配平)。上述反应中氧化产物为___________ 。
Ⅱ.2017年,中国科学家在利用二氧化碳直接制备液体燃料领域取得了突破性进展。其中用二氧化碳制甲醇(CH3OH)的反应如图所示:
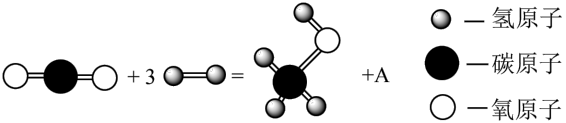
(5)如图所示的反应中,A的化学式是__________ 。
(6)该反应说明CO2具有______ 性。若有3 分子甲醇生成, 转移电子个数为________ 。
(1)氯化铁溶液用于五金蚀刻时的反应产物是氯化亚铁,反应后再通入氯气,又可将氯化亚铁转化为氯化铁,则通入氯气后反应的离子方程式为
(2)氯化铁常用于净水,是因为铁离子转化为Fe(OH)3胶体,使水中悬浮物聚沉,Fe(OH)3胶体分散质微粒直径的范围是
(3)氯化铁还可以充当双氧水分解的催化剂,2个H2O2分子发生分解时反应中转移的电子数是
(4)Na2FeO4是一种新型的净水消毒剂,可以通过下列反应制得:Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O(未配平)。上述反应中氧化产物为
Ⅱ.2017年,中国科学家在利用二氧化碳直接制备液体燃料领域取得了突破性进展。其中用二氧化碳制甲醇(CH3OH)的反应如图所示:

(5)如图所示的反应中,A的化学式是
(6)该反应说明CO2具有
更新时间:2023-10-26 13:20:38
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】按要求回答下列问题:
(1)对于 稀溶液、
稀溶液、 胶体、
胶体、 悬浊液,三者的本质区别是
悬浊液,三者的本质区别是___________ 。
(2) 胶体的胶团结构如图所示,则
胶体的胶团结构如图所示,则 胶粒
胶粒___________ (“带正”或“带负”或“不带”)电; 胶体能够稳定存在,是因为
胶体能够稳定存在,是因为___________ 。

(3)将 溶液加到沸水中,加热至整个体系呈
溶液加到沸水中,加热至整个体系呈___________ 色,即制得 胶体。证明
胶体。证明 胶体已经制备成功,可以利用
胶体已经制备成功,可以利用___________ (最简单的方法)进行鉴别。
(4)向 胶体中滴入足量稀盐酸,写出发生的化学反应方程式
胶体中滴入足量稀盐酸,写出发生的化学反应方程式___________ 。
(1)对于
 稀溶液、
稀溶液、 胶体、
胶体、 悬浊液,三者的本质区别是
悬浊液,三者的本质区别是(2)
 胶体的胶团结构如图所示,则
胶体的胶团结构如图所示,则 胶粒
胶粒 胶体能够稳定存在,是因为
胶体能够稳定存在,是因为
(3)将
 溶液加到沸水中,加热至整个体系呈
溶液加到沸水中,加热至整个体系呈 胶体。证明
胶体。证明 胶体已经制备成功,可以利用
胶体已经制备成功,可以利用(4)向
 胶体中滴入足量稀盐酸,写出发生的化学反应方程式
胶体中滴入足量稀盐酸,写出发生的化学反应方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)将 饱和溶液滴入煮沸的蒸馏水中,继续加热至液体变为
饱和溶液滴入煮沸的蒸馏水中,继续加热至液体变为_______ ,得到的是 胶体;
胶体; 胶体与
胶体与 溶液的本质区别在于
溶液的本质区别在于______ ,用____________ 可以区别二者。
(2)将(1)中得到的分散系装入U形管内,用石墨棒作电极,接通直流电源,通电一段时间后发现与电源负极相连的电极附近颜色加深,这个过程称为____ ,证明_____ 。
(3)将(1)中得到的分散系装入用鸡蛋内膜制成的袋子内,并将此袋子浸入盛水的烧杯中,此操作进行一段时间后,取少量袋子内的液体加入试管中,逐滴滴加盐酸直至过量,__ (填实验现象)。若取一部分烧杯内的水溶液,向其中滴加 溶液,
溶液,_____ (填实验现象)。
 饱和溶液滴入煮沸的蒸馏水中,继续加热至液体变为
饱和溶液滴入煮沸的蒸馏水中,继续加热至液体变为 胶体;
胶体; 胶体与
胶体与 溶液的本质区别在于
溶液的本质区别在于(2)将(1)中得到的分散系装入U形管内,用石墨棒作电极,接通直流电源,通电一段时间后发现与电源负极相连的电极附近颜色加深,这个过程称为
(3)将(1)中得到的分散系装入用鸡蛋内膜制成的袋子内,并将此袋子浸入盛水的烧杯中,此操作进行一段时间后,取少量袋子内的液体加入试管中,逐滴滴加盐酸直至过量,
 溶液,
溶液,
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】有以下物质;①石墨②铁③蔗糖④一氧化碳⑤氯化铁固体⑥碳酸氢钠固体⑦氢氧化钡溶液⑧纯醋酸⑨熔融氯化钠⑩液态氯化氢
(1)其中能导电的是___________ ;属于非电解质的是___________ ;属于弱电解质的是___________ 。
(2)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:___________ 。
(3)写出用⑤的饱和溶液制备 胶体的离子方程式:
胶体的离子方程式:___________ 。
(4)磷酸( )、亚磷酸(
)、亚磷酸( )来次磷酸(
)来次磷酸( )都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则
)都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则 、
、 、
、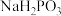 中属于正盐的是
中属于正盐的是___________ (填化学式)。
(1)其中能导电的是
(2)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:
(3)写出用⑤的饱和溶液制备
 胶体的离子方程式:
胶体的离子方程式:(4)磷酸(
 )、亚磷酸(
)、亚磷酸( )来次磷酸(
)来次磷酸( )都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则
)都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则 、
、 、
、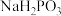 中属于正盐的是
中属于正盐的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】铜能与浓硝酸反应,化学方程式为:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
(1)用单线桥标出电子转移的方向和数目_______ 。
(2)上述反应中发生还原反应的物质是_______ ,被氧化的元素是_______ ,化合价降低的元素是_______ 。
(3)3个Cu被硝酸完全溶解后,Cu失去的电子数是_______ 个,产生气体_______ 个
(4)写出该反应的离子方程式_______ 。
(1)用单线桥标出电子转移的方向和数目
(2)上述反应中发生还原反应的物质是
(3)3个Cu被硝酸完全溶解后,Cu失去的电子数是
(4)写出该反应的离子方程式
您最近一年使用:0次
【推荐2】亚硝酸钠(NaNO2)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生Na2O、N2和O2,亚硝酸钠水溶液呈碱性,能与AgNO3溶液反应生成难溶于水、易溶于酸的AgNO2。回答下列问题:
(1)下列方法不能用来区分固体NaNO2和NaCl的是____ (填序号)。
(2)误食NaNO2会导致人体血红蛋白中的Fe2+转化为Fe3+而中毒,该过程中NaNO2表现出的性质与下列____ (填序号)反应中H2O2表现出的性质相同。
A.2H2O2 2H2O+O2↑
2H2O+O2↑
B.H2O2+Cl2=2HCl+O2↑
C.H2O2+H2SO4+2KI=2H2O+I2+K2SO4
D.5H2O2+2KMnO4+6HCl=2MnCl2+2KCl+5O2↑+8H2O
服用维生素C可将Fe3+转化为Fe2+从而解毒,维生素C的作用是____ (填“氧化剂”“还原剂”或“既是氧化剂又是还原剂”)。
(3)亚硝酸钠受热分解的化学方程式为4NaNO2 2Na2O+2N2↑+3O2↑,若反应中有12.4gNa2O固体生成,则转移电子的物质的量为
2Na2O+2N2↑+3O2↑,若反应中有12.4gNa2O固体生成,则转移电子的物质的量为____ mol。
(4)可用Cl2将溶液中的NO 氧化为NO
氧化为NO ,同时生成Cl-,已知Cl2+NaNO2+H2O=2HCl+NaNO3,则该反应的离子方程式为
,同时生成Cl-,已知Cl2+NaNO2+H2O=2HCl+NaNO3,则该反应的离子方程式为_____ 。
(1)下列方法不能用来区分固体NaNO2和NaCl的是
| A.分别溶于水并滴加酚酞试液 | B.分别溶于水并滴加HNO3酸化的AgNO3溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
A.2H2O2
 2H2O+O2↑
2H2O+O2↑B.H2O2+Cl2=2HCl+O2↑
C.H2O2+H2SO4+2KI=2H2O+I2+K2SO4
D.5H2O2+2KMnO4+6HCl=2MnCl2+2KCl+5O2↑+8H2O
服用维生素C可将Fe3+转化为Fe2+从而解毒,维生素C的作用是
(3)亚硝酸钠受热分解的化学方程式为4NaNO2
 2Na2O+2N2↑+3O2↑,若反应中有12.4gNa2O固体生成,则转移电子的物质的量为
2Na2O+2N2↑+3O2↑,若反应中有12.4gNa2O固体生成,则转移电子的物质的量为(4)可用Cl2将溶液中的NO
 氧化为NO
氧化为NO ,同时生成Cl-,已知Cl2+NaNO2+H2O=2HCl+NaNO3,则该反应的离子方程式为
,同时生成Cl-,已知Cl2+NaNO2+H2O=2HCl+NaNO3,则该反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(6分)我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:KIO3+5KI+3H2SO4====3K2SO4+3I2+3H2O
(1)用“双线桥”表示出上述反应中电子转移的方向和数目
________________________________________ 。
(2)如果反应中转移0.2mol电子,则生成I2的物质的量为_________________ 。
(3)利用上述反应检验食盐中是否加碘,所需试剂是______________ (填下列选项的序号)
①碘水②KI溶液③淀粉溶液④稀硫酸⑤AgNO3溶液
(1)用“双线桥”表示出上述反应中电子转移的方向和数目
(2)如果反应中转移0.2mol电子,则生成I2的物质的量为
(3)利用上述反应检验食盐中是否加碘,所需试剂是
①碘水②KI溶液③淀粉溶液④稀硫酸⑤AgNO3溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)难溶物PbSO4溶于CH3COONH4溶液可制得易溶于水的(CH3COO)2Pb,发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是________ (填“强”或“弱”)电解质。
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是_____ 元酸(填“一”、“二”或“三”)。
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式,并用双线桥法标出电子转移方向及数目______ 。
____Fe(OH)3+____ClO-+____OH-=__FeO +___Cl-+______
+___Cl-+______
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是___________ ;当有2mol H3PO4生成,转移的电子数目为____ e-
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式,并用双线桥法标出电子转移方向及数目
____Fe(OH)3+____ClO-+____OH-=__FeO
 +___Cl-+______
+___Cl-+______(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾(K2FeO4)在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的 KOH,使高铁酸钾析出。
(1)方法一:可利用固体反应物反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①生成物 Na2FeO4 中铁元素的化合价为_________ 。
②该反应中的还原剂是_________ ,每生成1mol Na2FeO4 转移_________ mol 电子。
(2)方法二:
反应:Fe(OH)3+ClO-+OH-—FeO +Cl- +H2O(未配平)
+Cl- +H2O(未配平)
① 配平离子反应方程式:_________ 。
②若反应过程中转移了 3mol 电子,则还原产物的物质的量为_________ mol。
③用双线桥标出电子转移的方向和数目_________ 。
(3)向 Na2FeO4 溶液中加入适量饱和的 KOH 溶液,有 K2FeO4 析出,请写出该反应的化学方程式_________ 。
(1)方法一:可利用固体反应物反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①生成物 Na2FeO4 中铁元素的化合价为
②该反应中的还原剂是
(2)方法二:
反应:Fe(OH)3+ClO-+OH-—FeO
 +Cl- +H2O(未配平)
+Cl- +H2O(未配平)① 配平离子反应方程式:
②若反应过程中转移了 3mol 电子,则还原产物的物质的量为
③用双线桥标出电子转移的方向和数目
(3)向 Na2FeO4 溶液中加入适量饱和的 KOH 溶液,有 K2FeO4 析出,请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知MnO2与浓盐酸反应的化学方程式为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:
(1)该反应的离子方程式为_______ 。
(2)用单线桥表示出电子的转移和数目_______
(3)该反应中HCl体现的性质是_______ ,氧化产物是_______ ,反应中氧化剂和还原剂的物质的量之比_______ 。
(4)当有1molCl2生成时,则被氧化的HCl的质量是_______ g,该反应转移的电子数为_______ (设NA为阿伏加德罗常数的值)。
 MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:(1)该反应的离子方程式为
(2)用单线桥表示出电子的转移和数目
(3)该反应中HCl体现的性质是
(4)当有1molCl2生成时,则被氧化的HCl的质量是
您最近一年使用:0次



