对于反应CaH2+2H2O=Ca(OH)2+2H2↑有下列判断:①H2只是氧化产物;②H2只是还原产物;③H2O是氧化剂;④CaH2中H元素被还原;⑤此反应中的氧化产物和还原产物的分子个数之比为1:1。上述判断正确的是
| A.②④ | B.③⑤ | C.①③⑤ | D.①④⑤ |
更新时间:2023-09-24 09:32:10
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】O2F2可以发生反应:H2S+4O2F2═SF6+2HF+4O2,下列说法错误的是( )
| A.O2是该反应的还原产物 |
| B.H2S还原剂,在反应中失去电子 |
| C.若生成4.48L HF,则转移0.8mol电子 |
| D.还原剂与氧化剂的物质的量之比为1:4 |
您最近一年使用:0次
单选题
|
适中
(0.64)
名校
【推荐2】已知反应KClO3+ 6HCl = KCl + 3Cl2↑+ 3H2O,若用K35ClO3与H37Cl作用,下列说法中正确的是
| A.生成的Cl2相对分子质量约为73.3 | B.该反应转移电子数为6 |
| C.KCl中只含有35Cl | D.KCl中同时含有35Cl和37Cl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向含有Fe2+、Br-、I-各0.1 mol 的溶液中通入Cl2。通入Cl2的体积(标准状况)与溶液中某种离子(用Q表示)的物质的量的关系如图所示,下列说法中正确的是


| A.Q是I- |
| B.a点时溶液中的阳离子有Fe2+和Fe3+(不考虑H+) |
| C.b点时溶液中的阴离子只有Cl-(不考虑OH-) |
| D.ab区间发生的反应:2Fe2++Cl2=2Fe3++2Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,在下列溶液中发生如下反应:
(1)
(2)
(3)
由此判断.下列说法错误的是
(1)

(2)

(3)

由此判断.下列说法错误的是
A. 是 是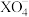 还原产物 还原产物 |
B.氧化性由强到弱顺序是 |
C.还原性由强到弱顺序是 |
D.溶液中可能发生反应 |
您最近一年使用:0次
【推荐1】次氯酸钠具有强氧化性,强碱性溶液中可将Fe3+氧化为一种常见的高效水处理剂,离子方程式为2Fe(OH)3+3ClO−+4OH−=2FeO +3Cl−+5H2O。下列说法中
+3Cl−+5H2O。下列说法中错误 的是
 +3Cl−+5H2O。下列说法中
+3Cl−+5H2O。下列说法中| A.还原性:Fe(OH)3>Cl− |
| B.由反应可知每2molFe(OH)3完全反应时,反应中转移6mol电子 |
| C.Na2FeO4能杀菌消毒,是由于它有强氧化性 |
| D.反应中氧化剂与还原剂的物质的量之比为2:3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一定条件下,RO3﹣与R﹣可发生反应:RO3﹣+5R﹣+6H+═3R2+3H2O,下列关于R元素的叙述中,正确的是( )
| A.元素R位于周期表中第ⅤA族 |
| B.R只能被还原 |
| C.R2在常温常压下一定是气体 |
| D.若1mol RO3﹣参与该反应,则转移的电子的物质的量为5 mol |
您最近一年使用:0次

 、N2、ClO-、CNO-(C+4价,N-3价)、Cl-等微粒。下列说法错误的是(
、N2、ClO-、CNO-(C+4价,N-3价)、Cl-等微粒。下列说法错误的是(

 K2S+3CO2↑+N2↑。下列说法正确的是
K2S+3CO2↑+N2↑。下列说法正确的是

