完成下列计算:
(1)已知工业上制取硫酸需要发生以下反应
Ⅰ. ;Ⅱ.
;Ⅱ.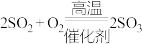 ;Ⅲ.
;Ⅲ.
①假设在生产中所有反应完全进行,则每生产1.00吨98%的浓硫酸需要
______ 吨。(保留2位小数)
②实际生产中可能会有损耗(即存在反应物没有发生反应),假设反应Ⅰ中 损耗率为20%,反应Ⅱ中
损耗率为20%,反应Ⅱ中 损耗率为10%,则实际生产1吨98%浓硫酸需要
损耗率为10%,则实际生产1吨98%浓硫酸需要
______ 吨。(保留2位小数)
(2)取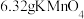 固体,加热一段时间后,剩余固体5.84g。该剩余固体与足量的浓盐酸在加热条件下充分反应生成氯气,产物中所有Mn元素均转化为
固体,加热一段时间后,剩余固体5.84g。该剩余固体与足量的浓盐酸在加热条件下充分反应生成氯气,产物中所有Mn元素均转化为 。
。
① 分解生成氧气的物质的量
分解生成氧气的物质的量
______ mol
② 分解的百分率为
分解的百分率为______ %;
③第二步反应中生成氯气的物质的量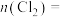
______ mol
(1)已知工业上制取硫酸需要发生以下反应
Ⅰ.
 ;Ⅱ.
;Ⅱ.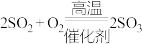 ;Ⅲ.
;Ⅲ.
①假设在生产中所有反应完全进行,则每生产1.00吨98%的浓硫酸需要

②实际生产中可能会有损耗(即存在反应物没有发生反应),假设反应Ⅰ中
 损耗率为20%,反应Ⅱ中
损耗率为20%,反应Ⅱ中 损耗率为10%,则实际生产1吨98%浓硫酸需要
损耗率为10%,则实际生产1吨98%浓硫酸需要
(2)取
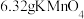 固体,加热一段时间后,剩余固体5.84g。该剩余固体与足量的浓盐酸在加热条件下充分反应生成氯气,产物中所有Mn元素均转化为
固体,加热一段时间后,剩余固体5.84g。该剩余固体与足量的浓盐酸在加热条件下充分反应生成氯气,产物中所有Mn元素均转化为 。
。①
 分解生成氧气的物质的量
分解生成氧气的物质的量
②
 分解的百分率为
分解的百分率为③第二步反应中生成氯气的物质的量
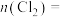
更新时间:2023-11-06 15:33:24
|
相似题推荐
计算题
|
较易
(0.85)
【推荐1】取50.0mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51g白色沉淀,用过量稀盐酸处理后沉淀质量减少9.85g,并有气体放出。试计算:
(1)写出Na2SO4和BaCl2溶液反应的方程式_______ ;
(2)原混合溶液中Na2CO3和Na2SO4的物质的量浓度为_______ 、______ ;
(3)产生的气体在标准状况下的体积为_______ 。
(1)写出Na2SO4和BaCl2溶液反应的方程式
(2)原混合溶液中Na2CO3和Na2SO4的物质的量浓度为
(3)产生的气体在标准状况下的体积为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】常温下 为气体,具有强氧化性,易溶于水且不与水反应,可作为自来水的消毒剂与食品漂白剂。
为气体,具有强氧化性,易溶于水且不与水反应,可作为自来水的消毒剂与食品漂白剂。 可通过如下反应制备:
可通过如下反应制备: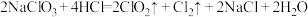 。现往足量
。现往足量 中通入
中通入 (标准状况下)气体制
(标准状况下)气体制 ,请计算:
,请计算:
(1)通入的HCl气体物质的量为___________ mol。
(2)充分反应后,转移电子数目为___________ 个。
(3)若将生成的混合气体通过装有亚氯酸钠( )的干燥管,可吸收
)的干燥管,可吸收 并生成
并生成 。通过两步制备共产生
。通过两步制备共产生 质量为
质量为___________ g。
 为气体,具有强氧化性,易溶于水且不与水反应,可作为自来水的消毒剂与食品漂白剂。
为气体,具有强氧化性,易溶于水且不与水反应,可作为自来水的消毒剂与食品漂白剂。 可通过如下反应制备:
可通过如下反应制备: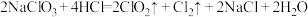 。现往足量
。现往足量 中通入
中通入 (标准状况下)气体制
(标准状况下)气体制 ,请计算:
,请计算:(1)通入的HCl气体物质的量为
(2)充分反应后,转移电子数目为
(3)若将生成的混合气体通过装有亚氯酸钠(
 )的干燥管,可吸收
)的干燥管,可吸收 并生成
并生成 。通过两步制备共产生
。通过两步制备共产生 质量为
质量为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐1】1774年,瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。现将含MnO2的质量为17.4g的软锰矿石与足量浓盐酸完全反应(杂质不参加反应)。计算:
MnCl2+Cl2↑+2H2O。现将含MnO2的质量为17.4g的软锰矿石与足量浓盐酸完全反应(杂质不参加反应)。计算:
(1)生成的Cl2的体积___________ (标准状况下)。
(2)参加反应的浓盐酸中被氧化HCl的物质的量___________ 。
 MnCl2+Cl2↑+2H2O。现将含MnO2的质量为17.4g的软锰矿石与足量浓盐酸完全反应(杂质不参加反应)。计算:
MnCl2+Cl2↑+2H2O。现将含MnO2的质量为17.4g的软锰矿石与足量浓盐酸完全反应(杂质不参加反应)。计算:(1)生成的Cl2的体积
(2)参加反应的浓盐酸中被氧化HCl的物质的量
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】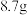 二氧化锰与足量的浓盐酸反应,则被氧化的氯化氢的物质的量是多少
二氧化锰与足量的浓盐酸反应,则被氧化的氯化氢的物质的量是多少______ ;产生的氯气在标准状况下的体积是多少_______ 。
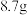 二氧化锰与足量的浓盐酸反应,则被氧化的氯化氢的物质的量是多少
二氧化锰与足量的浓盐酸反应,则被氧化的氯化氢的物质的量是多少
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:
(1)被还原的硝酸的物质的量是_______ ;
(2)NO的体积为_______ L, 的体积为
的体积为_______ L。
(3)产生的气体全部与氧气混合,将混合气体溶于水,若全部恰好溶解需要通入的氧气在标准状况下的体积是_______ 。
 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:(1)被还原的硝酸的物质的量是
(2)NO的体积为
 的体积为
的体积为(3)产生的气体全部与氧气混合,将混合气体溶于水,若全部恰好溶解需要通入的氧气在标准状况下的体积是
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐2】将32.0g铜与100mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2的混合气体在标准状况下的体积为11.2L。请回答:
(1)NO气体的体积为_______ L,NO2气体的体积为_______ L。
(2)待产生的气体全部逸出后,向溶液中加入VmLamol•L‒1NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为_______ mol•L‒1。
(1)NO气体的体积为
(2)待产生的气体全部逸出后,向溶液中加入VmLamol•L‒1NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
您最近一年使用:0次

 MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。

