完成下列问题。
(1)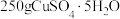 溶于水得到1 L溶液,所得CuSO4溶液中溶质的物质的量浓度为
溶于水得到1 L溶液,所得CuSO4溶液中溶质的物质的量浓度为___________ 。
(2)98 gH2SO4的物质的量是___________ mol;其中含有___________ mol O,含有___________ 个H。
(3)28 g N2的体积(标准状况下)为___________ L。
(4)15.6 g Na2X中含有0.4 mol Na+,则X的相对原子质量为___________ 。
(5)100 mL1 mol/L的碳酸钠溶液所含碳酸钠的质量是___________ g。
(1)
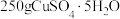 溶于水得到1 L溶液,所得CuSO4溶液中溶质的物质的量浓度为
溶于水得到1 L溶液,所得CuSO4溶液中溶质的物质的量浓度为(2)98 gH2SO4的物质的量是
(3)28 g N2的体积(标准状况下)为
(4)15.6 g Na2X中含有0.4 mol Na+,则X的相对原子质量为
(5)100 mL1 mol/L的碳酸钠溶液所含碳酸钠的质量是
更新时间:2023-11-09 17:47:35
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】按国家规定,每千克食用碘盐中碘的含量在20-50 mg之间,现对某品牌碘盐中碘(以KIO3形式加入)含量的测定:①准确称取食盐100 g,配制成250 mL溶液;②量取上述溶液25.00 mL于锥形瓶中,硫酸酸化后加入足量的KI充分反应;③经调节pH后,用0.001 mol·L-1Na2S2O3溶液滴定,消耗Na2S2O3溶液的体积为18.00 mL。
已知:KIO3+5KI+3H2SO4=3I2+K2SO4+3H2
I2+2Na2S2O3=2NaI+Na2S4O6
(1)所配制的食盐溶液的物质的量浓度为____ mol·L-1。
(2)该品牌食盐中碘的含量为___ mg·kg-1(写出简要的计算过程)。
已知:KIO3+5KI+3H2SO4=3I2+K2SO4+3H2
I2+2Na2S2O3=2NaI+Na2S4O6
(1)所配制的食盐溶液的物质的量浓度为
(2)该品牌食盐中碘的含量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)3.4gNH3中含有________ molH。
(2)标准状况下,等体积的CO和CO2的质量比为________ 。
(3)100mLAl2(SO4)3溶液中c(Al3+)=0.20mol•Lˉ1,则c(SO42-)=_______ 。
(4)物质的量浓度相同的NaCl、MgCl2、AlCl3溶液中分别加入足量的AgNO3溶液中,生成沉淀的质量相等,三种溶液的体积比为____________ 。
(5)标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,则该溶液的溶质的物质的量浓度为__________ 。
(1)3.4gNH3中含有
(2)标准状况下,等体积的CO和CO2的质量比为
(3)100mLAl2(SO4)3溶液中c(Al3+)=0.20mol•Lˉ1,则c(SO42-)=
(4)物质的量浓度相同的NaCl、MgCl2、AlCl3溶液中分别加入足量的AgNO3溶液中,生成沉淀的质量相等,三种溶液的体积比为
(5)标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,则该溶液的溶质的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】用NA表示阿伏加 德罗常数的数值,按要求完成下列填空。
(1)1个CO2分子含有________ 个电子,1 mol CO2含有______ molO ,_____ mol e-。
(2)1.204x1024个NH3分子含有原子_______ mol,含有N________ mol ,含H______ mol 。
(3)0.5 mol H2O中含有________ 个水分子,含有原子________ 个。
(4)质量都是50 g的 HCl、NH3、SO3、O2四种气体,含原子个数最多的是_______ 。
(5)写出NaHCO3在水溶液中的电离方程式:__________________ 。
(1)1个CO2分子含有
(2)1.204x1024个NH3分子含有原子
(3)0.5 mol H2O中含有
(4)质量都是50 g的 HCl、NH3、SO3、O2四种气体,含原子个数最多的是
(5)写出NaHCO3在水溶液中的电离方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】在0.5molH2S中,约含有________________ 个氢原子,共有_________ mol原子,其质量为____________ 克,在标况下体积为_____________ L。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】计算题
(1)3.6g H2O的物质的量是________ ,约含有____________________________ 个水分子,含有________ mol H。
(2)3.01×1023个H2O分子的物质的量为________ ,质量为________ ,含有质子的物质的量为________ ,含有电子的数目为________ ,这些H2O分子所含的H原子数目与________ mol CH4所含的H原子数目相同,和________ g CO2含有的分子数相同。
(3)质量为3.9g的Na2X中含有Na+的物质的量为0.1mol,则Na2X的摩尔质量为___________________ 。
(1)3.6g H2O的物质的量是
(2)3.01×1023个H2O分子的物质的量为
(3)质量为3.9g的Na2X中含有Na+的物质的量为0.1mol,则Na2X的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在标准状况下,有CH4和CO的混和气体共6.72L,其质量为6g,该混和气体中CH4的物质的量是_____ , CO的质量是_____ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】计算
(1)物质的量是高中化学常用的物理量,请完成以下各空:
①标准状况下,0.4克H2的体积为___________ L。
②100 mL硫酸铝溶液中,c(A13+)=0.2 mol/L,则c( )=
)=___________ mol/L;将该溶液稀释至150mL,稀释后溶液中的Al2(SO4)3的物质的量为___________ 。
(2)同温同压下,同体积的甲烷(CH4)和CO2气体∶所含物质的量之比为___________ ,密度之比为___________ 。
(3)室温下,某容积固定的密闭容器由可移动的活塞(忽略摩擦力)隔成A、B两室,向A室中充入H2和O2的混合气体,向B室中充入3 mol空气,此时活塞的位置如图所示:

已知A室混合气体的质量为102 g,若将A室中H2与O2的混合气体点燃引爆,恢复室温后,最终活塞停留的位置在___________ (填数字)刻度,反应后容器内气体压强与反应前气体压强之比为___________ 。
(1)物质的量是高中化学常用的物理量,请完成以下各空:
①标准状况下,0.4克H2的体积为
②100 mL硫酸铝溶液中,c(A13+)=0.2 mol/L,则c(
 )=
)=(2)同温同压下,同体积的甲烷(CH4)和CO2气体∶所含物质的量之比为
(3)室温下,某容积固定的密闭容器由可移动的活塞(忽略摩擦力)隔成A、B两室,向A室中充入H2和O2的混合气体,向B室中充入3 mol空气,此时活塞的位置如图所示:

已知A室混合气体的质量为102 g,若将A室中H2与O2的混合气体点燃引爆,恢复室温后,最终活塞停留的位置在
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】向1L恒容密闭容器中加入12g活性炭和NO,发生反应: ∆H。在
∆H。在 下,反应进行到不同时刻测得各物质浓度的部分数据如下:
下,反应进行到不同时刻测得各物质浓度的部分数据如下:
(1)10min时,混合气体的平均摩尔质量为_______ 。
(2)T1℃时,该反应的平衡常数K=_______ 。
(3)30min后,若只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是_______ (填字母)。
a.加入一定量的活性炭 b.改变反应体系的温度
c.缩小容器的体积 d.通入一定量的NO
(4)若30min后升高温度至 ,重新达到平衡时,容器中NO、
,重新达到平衡时,容器中NO、 、
、 的浓度之比为7:3:3,则该反应的∆H
的浓度之比为7:3:3,则该反应的∆H______ (填“<”、“=”或“>”)0
 ∆H。在
∆H。在 下,反应进行到不同时刻测得各物质浓度的部分数据如下:
下,反应进行到不同时刻测得各物质浓度的部分数据如下:
(1)10min时,混合气体的平均摩尔质量为
(2)T1℃时,该反应的平衡常数K=
(3)30min后,若只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是
a.加入一定量的活性炭 b.改变反应体系的温度
c.缩小容器的体积 d.通入一定量的NO
(4)若30min后升高温度至
 ,重新达到平衡时,容器中NO、
,重新达到平衡时,容器中NO、 、
、 的浓度之比为7:3:3,则该反应的∆H
的浓度之比为7:3:3,则该反应的∆H
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】计算下列各数值。
(1)3.1g Na2X含有Na+ 为0.1mol,则Na2X的摩尔质量为__ ,X的相对原子质量为__ 。
(2)8.5g氢氧根离子含有的电子数目为_______ 。
(3)14g C2H4与C4H8的混合物所含质子的物质的量为__ 。
(4)1.43g Na2CO3·10H2O溶于水配成100mL溶液,则c(Na2CO3)为__ mol/L;取20mL该溶液,加入__ mL水得到0.004mol/L的Na2CO3溶液(设稀释时对溶液体积的影响忽略不计)。
(1)3.1g Na2X含有Na+ 为0.1mol,则Na2X的摩尔质量为
(2)8.5g氢氧根离子含有的电子数目为
(3)14g C2H4与C4H8的混合物所含质子的物质的量为
(4)1.43g Na2CO3·10H2O溶于水配成100mL溶液,则c(Na2CO3)为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】设用NA表示阿伏伽德罗常数的值,其计算近似值为6.02×1023,按要求完成下列填空:
(1)0.5 mol NH3共含有_______________ 个原子。
(2)6 mol H2O与标准状况下_____________ L NH3所含氢原子数相等。
(3)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42﹣的物质的量是_________________ 。
(4)标准状况下11.2 L NO和__________________ g NO2所含有的氧原子数相等。
(5)8 g某物质含有3.01×1023个分子,该物质的相对分子质量约为__________________ 。
(1)0.5 mol NH3共含有
(2)6 mol H2O与标准状况下
(3)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42﹣的物质的量是
(4)标准状况下11.2 L NO和
(5)8 g某物质含有3.01×1023个分子,该物质的相对分子质量约为
您最近一年使用:0次




