向一定量的Fe、FeO、Fe2O3的混合物中,加入100mL1.0mol·L-1的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,假设溶液体积不变,所得溶液中加入KSCN溶液无血红色出现。请回答下列问题:
(1)生成气体的物质的量为___________ ;
(2)所得溶液中溶质的物质的量浓度为___________ ;
(3)若向溶液中加入氢氧化钠溶液震荡,现象是___________ ;原因是(用方程式表示)___________ ;
(4)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为___________ ;
(5)原混合物的总质量为___________ 。
(1)生成气体的物质的量为
(2)所得溶液中溶质的物质的量浓度为
(3)若向溶液中加入氢氧化钠溶液震荡,现象是
(4)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为
(5)原混合物的总质量为
更新时间:2023-10-04 21:11:14
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】金属与人类的生产生活密切相关,牢固掌握金属的知识十分必要。
(1)将锌粉加入到含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤。
①若滤液中只含一种溶质,请分析则滤渣的成分______________ ;
②若滤渣中含有两种金属,请分析滤液的成分______________ 。
(2)合金的用途十分广泛。某化学小组欲测定黄铜片(铜锌合金)的组成进行如下实验:取黄铜片30g放入烧杯,将250g稀硫酸分5次加入烧杯中,充分反应后,测得剩余固体的质量记录如下。请计算:
(1)黄铜片中铜的含量______________ 。
(2)稀硫酸中溶质的质量分数______________ 。
(1)将锌粉加入到含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤。
①若滤液中只含一种溶质,请分析则滤渣的成分
②若滤渣中含有两种金属,请分析滤液的成分
(2)合金的用途十分广泛。某化学小组欲测定黄铜片(铜锌合金)的组成进行如下实验:取黄铜片30g放入烧杯,将250g稀硫酸分5次加入烧杯中,充分反应后,测得剩余固体的质量记录如下。请计算:
| 次 数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 23.5 | 17 | 11.5 | 9.6 | 9.6 |
(1)黄铜片中铜的含量
(2)稀硫酸中溶质的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】为了测定黄铜(铜、锌合金)中铜的质量分数,取20g黄铜样品加入大烧杯中,把200g稀盐酸分四次加入,实验所得数据如下表:
计算:
(1)表中m=______ 。
(2)黄铜样品中铜的质量分数为多少?(写出计算过程)______
(3)反应总共产生气体的物质的量是多少?(写出计算过程)_______
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀盐酸质量/g | 50 | 50 | 50 | 50 |
剩余固体的质量/g | 16.75 | 13.5 | m | 12.2 |
计算:
(1)表中m=
(2)黄铜样品中铜的质量分数为多少?(写出计算过程)
(3)反应总共产生气体的物质的量是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】取50.0mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66g,并有气体放出。
(1)写出混合溶液中加入过量BaCl2后反应的化学方程式__________ ,_________________
(2)求原混合液中Na2SO4的物质的量浓度为___________ ;
(3)产生的气体在标准状况下的体积为___________ 。
(1)写出混合溶液中加入过量BaCl2后反应的化学方程式
(2)求原混合液中Na2SO4的物质的量浓度为
(3)产生的气体在标准状况下的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】Cl2与NaOH溶液反应可生成NaCl、NaClO和NaClO3、c(Cl-)和c(ClO-)的比值与反应温度有关。用48 g NaOH配成的500 mL溶液,与Cl2恰好完全反应(忽略Cl2与水的反应、盐类的水解及溶液体积变化)。
(1)NaOH溶液的物质的量浓度___ mol/L
(2)某温度下,反应后溶液中c(Cl-)=3c(ClO-), 则溶液在c(ClO-)=_____ mol/L。
(1)NaOH溶液的物质的量浓度
(2)某温度下,反应后溶液中c(Cl-)=3c(ClO-), 则溶液在c(ClO-)=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】有下列物质的溶液:①CH3COOH ②HCl ③H2SO4 ④NaHSO4
(1)若四种溶液的物质的量浓度相同,其c(H+)的大小比较为____________ (用序号表示,下同)。
(2)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为___________ ,经测定溶液中c(CH3COO-)为1.4×10-3 mol/L,此温度下醋酸的电离常数Ka=____________ ,温度升高,Ka将_____ (填“变大”“不变”或“变小”,下同),加入少量CH3COONa后c(H+)______ ,Ka______ 。
(1)若四种溶液的物质的量浓度相同,其c(H+)的大小比较为
(2)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某项目学习小组设计实验确定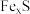 的组成,将一定量的
的组成,将一定量的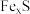 与
与 的盐酸恰好完全反应,生成
的盐酸恰好完全反应,生成 溶液、
溶液、 和
和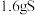 单质,过滤后向滤液中滴加足量
单质,过滤后向滤液中滴加足量 溶液,得到的沉淀经过滤洗涤,充分灼烧后称量至恒重得
溶液,得到的沉淀经过滤洗涤,充分灼烧后称量至恒重得 固体。计算:
固体。计算:
(1)盐酸的浓度为___________  。
。
(2)x的值为___________ 。(写出简要的计算过程,保留2位有效数字)
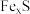 的组成,将一定量的
的组成,将一定量的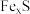 与
与 的盐酸恰好完全反应,生成
的盐酸恰好完全反应,生成 溶液、
溶液、 和
和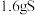 单质,过滤后向滤液中滴加足量
单质,过滤后向滤液中滴加足量 溶液,得到的沉淀经过滤洗涤,充分灼烧后称量至恒重得
溶液,得到的沉淀经过滤洗涤,充分灼烧后称量至恒重得 固体。计算:
固体。计算:(1)盐酸的浓度为
 。
。(2)x的值为
您最近一年使用:0次

 体积为1.12L(已折算成标况)。反应后加入足量NaOH溶液,过滤,将沉淀灼烧至恒重。
体积为1.12L(已折算成标况)。反应后加入足量NaOH溶液,过滤,将沉淀灼烧至恒重。

