2.80g某常见金属与足量盐酸在烧杯中反应,产生 体积为1.12L(已折算成标况)。反应后加入足量NaOH溶液,过滤,将沉淀灼烧至恒重。
体积为1.12L(已折算成标况)。反应后加入足量NaOH溶液,过滤,将沉淀灼烧至恒重。
(1)写出该金属的化学式________ ;
(2)计算沉淀灼烧至恒重的质量_______ 。(以上均需要必要过程,保留必要的有效数字位数)
 体积为1.12L(已折算成标况)。反应后加入足量NaOH溶液,过滤,将沉淀灼烧至恒重。
体积为1.12L(已折算成标况)。反应后加入足量NaOH溶液,过滤,将沉淀灼烧至恒重。(1)写出该金属的化学式
(2)计算沉淀灼烧至恒重的质量
更新时间:2020-09-08 18:12:31
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】① HNO3的摩尔质量是_______ ,0.5mol HNO3的质量是_________ ,1.5mol HNO3含有_____ mol氧原子。
② 标准状况下11.2L CO2的物质的量是____ 。
② 标准状况下11.2L CO2的物质的量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】32.5 g的锌与50 mL 18.4 mol/L浓硫酸充分反应,锌完全溶解,同时收集到标准状况下的混合气体V L。将反应后的溶液稀释到500 mL,测得溶液中氢离子的浓度为0.08 mol/L。
(1)反应过程中消耗的H2SO4的物质的量是___________ mol。
(2)反应过程中转移的电子的物质的量为___________ mol。
(3)混合气体中的成分及体积比为___________ 。
(1)反应过程中消耗的H2SO4的物质的量是
(2)反应过程中转移的电子的物质的量为
(3)混合气体中的成分及体积比为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将3.9 g Mg、Al合金溶于一定物质的量浓度的HCl溶液400 mL中,刚好完全反应,经检测合金和盐酸都无剩余,再向反应后的溶液中加入1mol/L的NaOH溶液后,生成沉淀。如果加入一定量的NaOH溶液至沉淀量最大时,溶液的总体积刚好为合金溶解时体积的两倍,假设完全反应(不考虑体积变化),试求:
(1)生成的沉淀的最大值是多少_________ ?
(2)原合金中Mg的质量百分含量_________ (计算结果保留一位小数点)。
(1)生成的沉淀的最大值是多少
(2)原合金中Mg的质量百分含量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】125g黄铜(铜锌合金)粉末可以跟250g硫酸溶液恰好完全反应,称得未溶物质量为92.5g。(可能涉及到元素的相对原子质量:Zn65 H1 S32 O16 Cu64)
(1)写出该反应的化学方程式_______ 。
(2)若将反应后的溶液蒸发1g水,温度降到室温,溶液正好饱和。求在室温时硫酸锌的溶解度_______ 。
(1)写出该反应的化学方程式
(2)若将反应后的溶液蒸发1g水,温度降到室温,溶液正好饱和。求在室温时硫酸锌的溶解度
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某研究小组通过以下方法测定某铁矿石样品(主要成分为 )中铁元素的质量分数:取20.0g铁矿石样品,粉碎后加入足量盐酸,充分反应后过滤,向滤液中加入足量氢氧化钠溶液,过滤、洗涤,将所得的沉淀灼烧,冷却后称得固体质量为16.0g。请根据以上信息计算该铁矿石样品中铁元素的质量分数
)中铁元素的质量分数:取20.0g铁矿石样品,粉碎后加入足量盐酸,充分反应后过滤,向滤液中加入足量氢氧化钠溶液,过滤、洗涤,将所得的沉淀灼烧,冷却后称得固体质量为16.0g。请根据以上信息计算该铁矿石样品中铁元素的质量分数___________ 。(假设杂质不与盐酸反应)
 )中铁元素的质量分数:取20.0g铁矿石样品,粉碎后加入足量盐酸,充分反应后过滤,向滤液中加入足量氢氧化钠溶液,过滤、洗涤,将所得的沉淀灼烧,冷却后称得固体质量为16.0g。请根据以上信息计算该铁矿石样品中铁元素的质量分数
)中铁元素的质量分数:取20.0g铁矿石样品,粉碎后加入足量盐酸,充分反应后过滤,向滤液中加入足量氢氧化钠溶液,过滤、洗涤,将所得的沉淀灼烧,冷却后称得固体质量为16.0g。请根据以上信息计算该铁矿石样品中铁元素的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】把2.0mol/L CuSO4溶液和2.0mol/L H2SO4溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和)。则:
(1)混合溶液中H+、Cu2+、 的物质的量浓度分别为:
的物质的量浓度分别为:____________ ;
(2)向溶液中加入铁粉,足够长的时间后,铁粉有剩余,过滤,此时滤液中的Fe2+的物质的量浓度为___________ ;
(3)取100mL该滤液,向其中加入适量硝酸,再加入足量氢氧化钠溶液,有红褐色沉淀生成。过滤,加热沉淀物至质量不再变化,得到红棕色的残渣。写出残渣的化学式______ ,并计算残渣的质量__________ (不计操作带来的损失)。
(1)混合溶液中H+、Cu2+、
 的物质的量浓度分别为:
的物质的量浓度分别为:(2)向溶液中加入铁粉,足够长的时间后,铁粉有剩余,过滤,此时滤液中的Fe2+的物质的量浓度为
(3)取100mL该滤液,向其中加入适量硝酸,再加入足量氢氧化钠溶液,有红褐色沉淀生成。过滤,加热沉淀物至质量不再变化,得到红棕色的残渣。写出残渣的化学式
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】向一定量的Fe、FeO、Fe2O3的混合物中,加入100mL1.0mol·L-1的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,假设溶液体积不变,所得溶液中加入KSCN溶液无血红色出现。请回答下列问题:
(1)生成气体的物质的量为___________ ;
(2)所得溶液中溶质的物质的量浓度为___________ ;
(3)若向溶液中加入氢氧化钠溶液震荡,现象是___________ ;原因是(用方程式表示)___________ ;
(4)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为___________ ;
(5)原混合物的总质量为___________ 。
(1)生成气体的物质的量为
(2)所得溶液中溶质的物质的量浓度为
(3)若向溶液中加入氢氧化钠溶液震荡,现象是
(4)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为
(5)原混合物的总质量为
您最近一年使用:0次

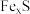 的组成,将一定量的
的组成,将一定量的 的盐酸恰好完全反应,生成
的盐酸恰好完全反应,生成 溶液、
溶液、 和
和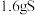 单质,过滤后向滤液中滴加足量
单质,过滤后向滤液中滴加足量 溶液,得到的沉淀经过滤洗涤,充分灼烧后称量至恒重得
溶液,得到的沉淀经过滤洗涤,充分灼烧后称量至恒重得 固体。计算:
固体。计算: 。
。

